Symtom
Rekommendationer:
- Identifiera tidigt vilket mål vården har samt i vilken palliativ fas barnet befinner sig. Detta ska styra vårdens inriktning och val av behandlingar.
- Läkemedelsordinationer kan behöva avvika från standarddoser eller förskrivas för så kallad "off-label"-användning. Sådan förskrivning ska göras av läkare med särskild hänsyn till barnets behov och evidensläge.
- Minimera smärta och obehag i samband med läkemedelsadministration. Överväg alternativa administreringssätt såsom: transdermalt (via huden), buckalt (mellan kind och tandkött), nasalt (via näsan), rektalt (via ändtarmen), sublingualt (under tungan) och subkutant (under huden).
- Överväg användning av PCA-pump (Patient Controled Analgesia) för kontinuerlig smärtlindring. Pumpen kan kopplas till subkutan venport, central venkateter eller subkutan nål, och kan styras av barnet eller närstående.
- I sen palliativ fas kan vissa biverkningar och komplikationer av symtomlindrande behandling behöva accepteras om målet är att optimera symtomlindring och välbefinnande.
Begreppet ”total pain” omfattar fysisk, psykisk, social och existentiell smärta och kan användas som utgångspunkt vid smärtlindring och annan symtomhantering vid livshotande sjukdom. Det handlar om att se hela människan och hela summan av de olika smärtaspekterna 11.
Det är en etisk skyldighet att i möjligaste mån lindra barnets symtom och lidande. Utan god symtomlindring kan inte barnet eller de närstående tillgodogöra sig övrig palliativ vård. De närstående kan också påverkas negativt i många år efter dödsfallet om inte barnet symtom lindras på bästa sätt 134.
Oavsett vilket eller vilka symtom barnet uppvisar bör följande initiala frågor ställas inom teamet:
- Vad är målet med vården i stort och i den aktuella situationen? Definiera det tillsammans med barnet och de närstående.
- Vad är viktigt för barnet och de närstående?
- Vad är rimligt?
- Var i det palliativa vårdförloppet befinner vi oss?
- Hur kan vi maximera livskvaliteten?
I tidig palliativ fas behöver man tänka på de mer långsiktiga konsekvenserna av en lindrande behandling. I sen palliativ fas, framför allt vid vård i livets slut, fokuserar man allt mindre på eventuella sena biverkningar.
Vid symtomlindring bör både icke-farmakologiska och farmakologiska metoder användas. Ofta behövs flera behandlingsmodaliteter som kan komplettera och förstärka varandra. Syftet är att undvika onödiga biverkningar och samtidigt hitta en balans mellan lindring och sedering, utifrån barnets symtom och palliativa fas. Barnet ska, med stöd av familjen, i så stor utsträckning som möjligt erbjudas att vara delaktig i beslut om symtomlindrande behandling. Det finns också en tydlig förstärkningseffekt (”spill-over”-effekt) mellan olika symtom, det är viktigt med en samlad bedömning av symtombilden för en effektiv behandling och konstruktiv utvärdering.
Vid vård av barn kan läkemedel behöva förskrivas för en indikation och ålder som inte är angiven i Fass. Läkaren kan då få stöd i att dosera och använda läkemedel via till exempel databasen ePed, som är en erfarenhets- och evidensbaserad databas för barnläkemedel 135. Det finns också olika internationella rekommendationer såsom The Association of Pediatric Palliative Medicin Master Formulary 136.
Se bilaga Läkemedelsbehandling vid palliativ vård av barn.
Strukturerad symtomlindring följer denna process:
- Identifiera symtom.
- Skatta och dokumentera nivå på symtomen och på det besvär barnet har av ett specifikt symtom.
- Identifiera möjliga orsaker till symtomen och möjliga metoder för att lindra dem.
- Behandla symtomen.
- Utvärdera och ompröva behandlingen:
a. Uppnådde vi målet, var administrationsvägen optimal (tillräckligt men inte överdimensionerat)?
b. Finns det anledning att justera behandlingen?
Stöd för att identifiera, skatta, bedöma och följa upp symtom och behov
Använd om möjligt, symtomskattningsinstrument som är utvecklade för och testade på barn med rätt ålder och funktionsnivå, för att barnet ska ha optimala förutsättningar för att ge sin bild av symtomet. Vårdnadshavare och vårdpersonal skattar inte alltid ett barns symtom på samma sätt som barnet gör, därför bör självskattning vara förstahandsvalet i alla sjukdomsskeden 137 138 139 .
Det finns i dagsläget inget validerat instrument för att göra en samlad bedömning av barns palliativa behov. The Edmonton Symtom Assessment System (ESAS-r) [140] och Integrated Palliative care Outcome Scale (IPOS) palliativtutvecklingscentrum.se är skattningsinstrument som är relevanta för palliativ vård för vuxna. De kan med viss försiktighet användas i samtal med barn och närstående.
Administrationssätt för läkemedel
Valet av administrationssätt beror på vad som passar bäst för barnet i stunden, det behöver kontinuerligt omprövas. Flera alternativ kan vara lämpliga.
Läs mer om symtomkontroll här:
Se bilaga Läkemedelsbehandling vid palliativ vård av barn.
Introduction to children’s palliative care – Together for short lives togetherforshortlives.org.uk/changing-lives/supporting-care-professionals/introduction-childrens-palliative-care.
Enteral administrering
Läkemedel kan ges via munnen, nasogastrisk sond, gastrostomi (sond genom bukväggen till magsäcken) eller en jejunostomi (sond till den övre delen av tunntarmen). På Läkemedelsverkets webbsida Beskrivning av läkemedelsadministrering via enteral infart eller sond finns information om vilka tabletter som kan krossas eller lösas i vatten. Vissa injektionslösningar kan ges i sond eller rektalt.
Intravenös administrering
När läkemedel ges intravenöst finns olika centrala och perifera infarter såsom; subkutan venport, central venkateter, perifer venkateter, Picc-line och Midline.
Om barnet behöver kontinuerlig intravenös behandling i hemmet eller på sjukhus, kan man överväga en Patient-Controlled Analgesia pump (PCA) som barnet sköter själv, med eventuellt stöd av vårdnadshavare. Pumpen kan ge bolusdoser som är ordinerade och förutbestämda. Dessa pumpar och tillhörande kassetter med läkemedel kan tas med i en ryggsäck för att förenkla vardagen.
Transdermal administrering
Långtidsverkande bassmärtlindring kan ges via huden i form av plåster. Det bör då sitta så att det inte av misstag kan klias bort eller ramla av. Sätt gärna genomskinligt förband eller liknande över.
Buckal administrering
Fettlösliga substanser i liten volym kan ges i munnen via kindslemhinnan. Vid krampanfall kan buckal administrering vara lättare än andra administrationssätt. När barnet har mycket slem i munnen, är administrationssättet mindre lämpligt.
Nasal administrering
Fettlösliga läkemedel kan ges via näsan med hjälp av en adapter, exempelvis Mucosal Atomization Device (MAD), där en konformad topp av skumgummi sätts på en spruta och ger en finfördelad spraydusch. Via näsan kan man även ge mycket små barn kort- och långtidsverkande opioider samt sederande och lugnande läkemedel.
Rektal administrering
De läkemedel som ges buckalt eller nasalt kan även ges rektalt, vilket kan passa små barn med kraftig slembildning. Rektal administrering bör undvikas vid neutropeni, trombocytopeni. och diarré.
Subkutan administrering
Via en subkutan kateter (NeriaGuard, I-port, Neoflon) kan man ge injektioner eller koppla en subkutan infusion. Den ska sättas i områden där det finns rikligt med underhudsfett och kan sitta i upp till en vecka. Subkutan administrering innebär aningen långsammare anslagstid jämfört med intravenös, vilket ibland är en fördel. Det är lättare för barnet och de närstående att självständigt ge läkemedel subkutant jämfört med intravenöst.
Sublingual administrering
Det finns läkemedel i form av munlösliga tabletter som administreras under tungan med i princip lika snabb effekt som vid intravenös administrering 141 .
Andningspåverkan
Barn i palliativ vård kan få en rad symtom från andningsvägarna såsom andnöd, kraftig slemproduktion och rosslighet. Målet med den samlade icke-farmakologiska och farmakologiska behandlingen är att åtgärda orsaken till besvären, och om det inte är möjligt är målet att lindra symtomen och minska besvären, med minsta möjliga biverkningar för barnet.
Andnöd är en plågsam upplevelse, och särskilt vanlig i livets slutskede. Känslan är att andningsbehovet överstiger andningsfunktionen 113142.
Andra symtom såsom oro kan tyda på dyspné. Barnet kan beskriva sin upplevelse med hjälp av en skala, till exempel 0-10. Saturationsmätning kan vara av värde som del i en kartläggning av orsakerna till dyspné.
Icke-farmakologisk behandling
Känslan av att ha svårt att andas är separerad från det objektiva andningsarbetet, och barnet kan lära sig tekniker för att minska känslan av andnöd. Det handlar alltså om att öka barnets egen förmåga att kompensera för känslan.
Oro och ångest kan förvärra känslan av andnöd och tvärt om, så det är viktigt att skapa en lugn miljö med trygghet och närhet. Olika avslappnings- och andningsövningar kan vara till hjälp. Med en god andningsteknik kan barnet få ett ökat välbefinnande med mindre ångest, stress och smärta. Att distrahera och avleda är också ofta till god hjälp 76143144145.
Andningsgymnastik är viktigt för barn med stor slemproblematik. Den ges av en fysioterapeut men kan även utföras av närstående och vårdpersonal efter given instruktion. Andningsgymnastiken bygger på kunskap om slemproblematikens grundproblem, och målet är fria luftvägar och effektiv andning. Insatserna kan också syfta till att maximera syreupptaget, avlasta andningsmuskulaturen, minska energiåtgången och förstärka känslan av kontroll. Barnets fysiska och kognitiva förutsättningar avgör valet av insatser, tillsammans med andra omgivande faktorer såsom miljö och hjälpmedel. Närstående, och om möjligt även barnet, behöver också information och stöd för att använda individuellt anpassade hjälpmedel.
Barn med kronisk respiratorisk svikt har ofta andningsstöd som CPAP/BiPAP/Högflödesgrimma och hostmaskin sedan tidigare. Använd det som ger bäst lindring.
Vid livets slutskede kan andningsgymnastik, s.k. slemmobilisering behöva modifieras om insatserna är obehagliga för barnet eller om man har omvärderat tidigare mål om att undvika lunginflammation eller bibehålla viss andningskapacitet. Det är viktigt att optimera välbefinnandet för dagen och stötta de närstående i att ändra den vanliga andningsgymnastiken till en mer anpassad slemmobilisering i livets slut. När det fungerar bör man fortsätta med de slemmobiliserande åtgärder som barnet tidigare haft såsom andningsgymnastik och eventuell hostmaskin, i den utsträckning barnet orkar 7576143144146.
Åtgärder vid andnöd och annan andningspåverkan:
- Förmedla lugn, trygghet och närhet.
- Att använda taktil massage kan vara ett sätt att minska oro och ångest 147 .
- Se till att det finns frisk luft.
- Öppna t.ex. ett fönster.
- Erbjud en handhållen fläkt nära ansiktet 148 .
- Positionering och lägesförändring.
- Ge barnet en bekväm ställning i sängen med hjälp av avlastande kuddar
- Hoststöd, erbjud manuellt stöd eller en hostmaskin, eller träna hostteknik.
- Testa mobilisering eller fysisk aktivitet, med eller utan hjälpmedel såsom boll och studsmatta.
- Testa motstånds- och djupandning (Positive Expiratory Pressure, PEP). Motståndet kan skapas av att andas ut med slutna läppar.
Åtgärder vid slembesvär eller minskad andningsmuskulär förmåga:
- Testa motstånds- och djupandning (PEP). Motståndet kan skapas av sluten läppandning eller så kallad PEP-mask.
- Gör regelbundna lägesförändringar.
- Positionering.
- Se till att det finns frisk luft, öppna t.ex. ett fönster.
- Testa mobilisering eller fysisk aktivitet, med eller utan hjälpmedel, t.ex. boll och studsmatta.
- Hoststöd, erbjud manuellt stöd eller hostmaskin eller träna hostteknik, såsom att ”huffa”.
Åtgärder vid ångest, oro och stress:
- Testa andningstekniker såsom diafragmaandning och fyrkantsandning.
- Testa mobilisering eller fysisk aktivitet.
- Öva avslappningstekniker såsom avspänning och vila.
Farmakologisk behandling
Innan man sätter in farmakologisk behandling är det viktigt att utreda eventuella bakomliggande orsaker till andningsbesvären såsom slem, oro, anemi (blodbrist) och övervätskning.
Opioider
Vid läkemedelsbehandling mot andnöd rekommenderas i första hand opioider, t.ex. morfin. Barn som tidigare inte har behandlats med opioid behöver starta med en låg dos som titreras upp till önskad behandlingseffekt 148 .
Bensodiazepiner
Oro och ångest förstärker ofta känslan av andnöd, och tvärt om. Då kan bensodiazepiner vara värdefullt, framför allt i kombination med opioider. Midazolam är ett vanligt val 148.
Syrgas
Det finns svag vetenskaplig och erfarenhetsmässig grund för att ge syrgas vid livets slut. Behandlingen kan dock fortsätta om barnet upplever en lindring av den. Barnets välbefinnande får då styra och behandlingen behöver inte följas upp med kontroll av saturation (mätning av syrenivå i blodet). Vissa barn kan uppleva obehag av masken eller grimman, vilket i sin tur kan leda till ökad andnöd. Möjligen är det den ”blåst” som syrgasen åstadkommer som ger mest lindring 148149150.
Antikolinergika
Om barnet har besvär av slem och rosslig andning kan man använda antikolinergika, exempelvis glykopyrronium. Det kan ges vid behov eller regelbundet via munnen, subkutant och intravenöst. Man kan också överväga att ge atropindroppar under tungan.
Undvik hyoscin eftersom det passerar blodhjärnbarriären, med risk för mental påverkan 151.
Slemlösande och luftrörsvidgande
Andnöd kan behandlas genom inhalation av natriumkloridlösning och/eller luftvägsvidgande läkemedel när barnet tycker att det ger lindring.
Pleuradränage och pleuratappning
Luft eller vätska i lungsäcken (pneumotorax respektive pleuravätska) kan ge andnöd och smärta. Diagnosen fastställs med lungröntgen. Ibland behöver luft eller vätska evakueras med hjälp av ett dränage. Att tappa ut vätskan kan ge god symtomlindring för stunden, vätskan återkommer dock oftast efter en tid.
Man kan överväga att framkalla en inflammatorisk reaktion för att löda ihop lungsäcken (pleurodes), men få barn har behov av denna åtgärd 143152153154. Utöver detta bör möjlighet ges till kvarliggande dränage (PleurX).
Diuretika
Vid besvärande ödem, till exempel lungödem med behov av diuretika, ges i första hand furosemid (se nedan under Cirkulation). Det är viktigt att återkommande se över barnets vätskebalans för att optimera mängden vätska i förhållande till var i det palliativa skedet barnet befinner sig 143 148 .
Cirkulation (inklusive blödning)
Cirkulationspåverkan kan förkomma i både tidig och sen palliativ fas och beror på barnets grundsjukdom, allmäntillstånd eller behandling samt var i det palliativa vårdförloppet som barnet befinner sig. Barn med hjärtsjukdom kan ha cirkulationsproblem som i tidigt skede av sjukdomen sköts enligt utarbetade riktlinjer inom barnhjärtsjukvård, men successivt skiftar behandlingens fokus till att undvika onödig sjukhusvård och onödiga biverkningar.
Barn med nedsatt rörlighet och långvarig immobilisering kan ha försämrad perifer cirkulation och därmed ökad risk för svullnad och hudproblem.
Barn med cancersjukdom kan ha tumörer som trycker på blod- och lymfkärl och därmed orsakar svullnad i en kroppsdel eller mer generellt. Vid livets slut kan diuretika behövas, men det viktigaste är att undvika vätsketillförsel som kroppen inte kan tillgodogöra sig och som riskerar att orsaka ödem och andnöd.
I tidig palliativ fas är blödningar mindre ofta ett problem, men blod- och trombocyttransfusioner kan behövas. Vid avancerad leversjukdom eller blodsjukdom kan koagulationsförmågan vara rubbad, med ökad blödningsrisk som följd. Även blödning från mag-tarmkanalen kan förekomma liksom lungblödningar vid exempelvis lungaspergillos 143 153 154 .
Vid livets slut förlorar kroppen förmågan att reglera puls, blodtryck och temperatur. Blodtrycket sjunker och pulsen blir oregelbunden. När cirkulationen försämras kan barnets händer och fötter bli kalla. Kroppstemperaturen kan pendla mellan att vara låg och hög, och huden kan kännas klibbig. Den ökande kroppstemperaturen bör behandlas med febernedsättande läkemedel samt exempelvis svalkande avtvättningar, svala lakan, öppet fönster, svala kläder, lägesändringar eller extra filtar.
Huden kan bli marmorerad blåaktig eller fläckigt lila. Mot slutet får ansiktet ofta en grågul vitaktig färg. Näsan kan bli smalare och spetsigare 113 142 . Se även kapitel 11 Det döende barnet.
Icke-farmakologisk behandling
Vid svullnadsproblematik kan åtgärder som positionering, högläge och regelbundna lägesändringar vara till hjälp. Patienten bör uppmuntras till aktiva rörelser, och om detta inte är möjligt kan närstående med stöd och vägledning bistå med passiva eller avlastande rörelser.
Det är viktigt att förvarna närstående om att det är möjligt med en större eller förvärrad blödning eftersom synligt blod är ett så påtagligt och oroande symtom. Man kan vid behov använda mörka textilier för att det inte ska se så dramatiskt ut. Vid akut större blödning är det viktigt att stoppa blödningen och ge adekvat ångestlindring.
Farmakologisk behandling
Målet är som alltid god symtomlindring till minsta möjliga besvär. Endast nödvändiga läkemedel bör användas, och de som har använts sedan tidigare bör omvärderas för att se om nyttan inte längre överväger riskerna. Detsamma gäller vätskebehandling och blod- och trombocyttransfusioner.
Se bilaga Läkemedelsbehandling vid palliativ vård av barn.
Behandlingsförslag vid blödningar:
- Vid mindre hudsår kan kompresser indränkta med tranexamsyra eller adrenalin prövas direkt på såret. Tranexamsyra kan även ges peroralt eller intravenöst.
- Slemhinneblödningar kan hanteras på motsvarande vis.
- Vid koagulationsrubbningar kan K-vitamin ges.
- Protonpumpshämmare kan användas vid magblödningar.
- Sederande och smärtlindrande läkemedel kan också användas, se avsnitt 14.14 Smärta 143153154.
Elimination (urin och avföring)
Symtom från tarmar och/eller urinvägar hos ett barn som tidigare har varit kontinent kan orsaka oro hos barn och vårdnadshavare, och det är viktigt att informera om dessa symtom 155 156 . Svårigheter att styra tarm och blåsa kan uppstå till följd av sjukdomsprogress och/eller given behandling. I livets slutskede kan förstoppning eller diarré uppstå till följd av sjukdomsprogress och/eller given behandling. Besvären kan förvärras på grund av smärtstillande läkemedel med opiodier. Smärta, oro och rastlöshet kan vara symtom på förstoppning eller en mycket fylld urinblåsa. Därför behövs regelbundna observationer av barnets avförings- och urinproduktion 157 .
Förstoppning
Vanliga orsaker
Vanliga orsaker till förstoppning är:
- behandling med läkemedel som minskar tarmens rörelser, till exempel opioider eller antikolinergika
- tumörsjukdom som ger en obstruktion av tarmen
- neurologisk påverkan
- minskat vätskeintag
- fiberfattig kost
- immobilisering
- rubbningar i ämnesomsättning eller elektrolyter
- urinretention (oförmåga att tömma urinblåsan).
155.
Behandling vid förstoppning
Icke-farmakologisk behandling kan omfatta:
- åtgärder för att optimera mat och vätskeintag
- fysisk aktivitet och mobilisering
- taktil massage
- lägesändringar om barnet inte själv kan röra sig
- värme och massage på buken.
10.
Farmakologisk behandling:
- Vid start av opioidbehandling ges i förebyggande syfte:
- laxantia i form av det motorikstimulerande läkemedlet natriumpikosulfat
- peroral behandling med extempore mixtur Naloxon (beredning från Apotek Produktion & Laboratorier) 4 gånger per dag. Om det gäller ett äldre barn kan man överväga att använda naloxegol, se Riktlinjer för smärtbehandling (karolinska.se).
- Vid behov ges osmotiskt verkande läkemedel:
- peroral administration av kaliumklorid och makrogol eller enbart makrogol
- rektal administration av läkemedel såsom natriumcitrat, dihydrat eller natriumlaurylsulfoacetat eller bisakodyl, som bara fungerar om det finns avföring i rektum.
Övriga behandlingsalternativ är:
Diarré
Vanliga orsaker till diarré är:
- förstoppning
- läkemedelsbiverkan
- alltför intensiv laxering
- infektion
- bakomliggande sjukdom
- strålbehandling mot buken eller bäckenet.
Behandling vid diarré
Icke-farmakologisk behandling kan omfatta att:
- hjälpa barnet att vara ren och torr
- vädra rummet vid behov
- bädda med engångsdraglakan eller lägga blöjor eller bäddskydd i sängen
- använda barriärsskydd för att skydda huden
- minska mängden mat och ersätta mat med klara vätskor eller vätskeersättning
- ge kostråd för vad som kan vara stoppande eller lösande.
Farmakologisk behandling kan omfatta:
- läkemedel som normaliserar tarmens rörelse, motverkar vätskeförluster och ökar förmågan att hålla avföringen
- symtomatiskt kan diarré behandlas med motilitetshämmande läkemedel, loperamid, i första hand som munsönderfallande tablett.
Urinretention
Urinretention kan uppstå som en biverkan av opioidbehandling, vid förstoppning eller vid tryck på ryggmärgen 155 156 .
Eventuell urinretention bedöms genom att göra en ”bladder scan”, vilket innebär att volymen i urinblåsan mäts med ultraljudsapparat och genom att försiktigt palpera urinblåsan.
Medicinering med smärtlindrande läkemedel, och en avslappnande miljö, kan göra det lättare för barnet att kissa 156 . Vid urinretention kan det bli aktuellt att tappa urin med kateter, och i vissa fall behövs en kvarliggande urinkateter, vilket är en läkarordination.
Hud och vävnad
Kontakta arbetsterapeut i god tid så att hen kan hjälpa till att förskriva hjälpmedel som till exempel vårdsäng, tryckavlastande madrass, tryckavlastande dyna till stol och rullstol, positioneringskuddar.
Hudens tillstånd är beroende av en god cirkulation i kroppens alla delar. Personer som inte kan röra sig får sämre cirkulation, vilket ökar risken för trycksår, särskilt på utsatta ställen såsom höftkam, korsrygg, sittbensknölar, fotknölar och hälar 76. Mindre aktiva barn har också ökad risk för trycksår, delvis på grund av deras kroppskonstitution och relation mellan fett- och muskelmassa159 160 . Det är därför viktigt att även observera bakhuvudet och öronen. Huden ska hållas varm, torr och mjuk så att inte sprickor eller sår uppstår, som i sin tur kan vara en inkörsport för olika infektioner 161 . För att tidigt upptäcka trycksår rekommenderas regelbunden strukturerad bedömning av huden 162 .
Risken för trycksår gör att man behöver vara observant på neurologiskt sjuka barn som använder personliga hjälpmedel av olika slag, till exempel korsett och fothylsor. Dessutom kan medicinteknisk apparatur ge upphov till tryck i ansiktet och på halsen. Barn som har begränsad kommunikativ förmåga och svårt att själva påkalla uppmärksamhet kräver en observant omgivning och förebyggande rutiner enligt tidigare beskrivning 159 163 .
Vid livets slutskede bör besvärande lägesändringar minimeras, för de kan vara väldigt påfrestande för barnet och ge upphov till smärta. Man kan i stället göra små lägesändringar av exempelvis en arm och ett ben, snarare än att flytta hela kroppen från sida till sida.
För mer information om maligna tumörsår, se Regionalt vårdprogram för maligna tumörsår.
Illamående och kräkningar
Illamående och kräkningar är vanliga symtom i alla skeden av sjukdom och det är många olika faktorer som påverkar symtomutvecklingen 164 och livskvaliteten 165 Barn reagerar ibland på stress med illamående och kräkningar 143. Dessa symtom bör utredas med hjälp av anamnes och barnets aktuella status. För att finna rätt behandling behöver man förstå komplexiteten bakom symtomutvecklingen och det enskilda barnets problematik. Behandlingen inkluderar ofta en kombination av olika icke-farmakologiska och farmakologiska behandlingar som delvis överlappar 157.
Kräkcentrum i hjärnstammen (medulla oblongata) har en överordnad roll vid utveckling av illamående och kräkningar. Detta kontrollcentrum tar emot impulser från kemoreceptorer i fjärde ventrikeln, högre hjärncentrum och mag-tarmkanalen samt vestibulära signaler från innerörat. Kräkcentrum kan alltså aktiveras av flera olika orsaker samtidigt: substanser som transporteras via blodet (till exempel läkemedel och neurotransmittorer), lägesändringar och faktorer som aktiverar högre hjärncentrum (till exempel oro, ångest, smärta och synintryck) 157.
Det finns många specifika orsaker till illamående vid svår sjukdom. Besvären kan vara relaterade till tumörer i mag-tarmkanalen, grav njursvikt (uremi), leversvikt, metabola orsaker, hyponatremi, hyperkalcemi, hyperglykemi, obstipation, kostfaktorer, ökat intrakraniellt tryck (störd likvorcirkulation, hjärntumör eller hjärnmetastas), antitumoralbehandling (cytostatika och strålbehandling) och läkemedelsbehandling såsom opioider, antiinflammatoriska preparat (NSAID) och antibiotika 157.
Icke-farmakologisk behandling
Icke-farmakologisk behandling kan omfatta:
- akupressurarmband
- aromaterapi, för fördjupning se 166
- avledning
- avslappning
- fläkt som blåser mot ansiktet
- frisk luft på rummet
- massage
- små matportioner
- vissa dofter, exempelvis mentol och citron, som kan minska besvär.
Starka dofter, exempelvis parfym eller matrester, kan ge ett ökat illamående 153 157 .
Farmakologisk behandling
Det finns svag evidens för optimal läkemedelsbehandling av illamående (antiemetika) 167 . Den kliniska erfarenheten av läkemedelsbehandlingar är däremot stor, i synnerhet inom barncancervård 168 och vid postoperativt illamående hos barn 169.
Antihistaminbehandling
Antihistaminbehandling som har en vestibulär effekt, kan fungera väl vid till exempel opioidutlöst illamående. I första hand rekommenderas meklozinbehandling.
Antikolinerga
Antikolinerga läkemedel såsom hyoscin, hyoscinbutylbromid och glykopyrronium kan dämpa illamående vid subileus och ileus, eftersom de kan minska tarmsekretion. Hyoscin finns som plåster. Substansen passerar dock blodhjärnbarriären och kan ha effekt på rörelseutlöst illamående, har en sederande effekt och kan ge upphov till förvirring. Butylskopolamin saknar förmåga att passera blodhjärnbarriären och har därför ingen central effekt 167 .
Bensodiazepiner
Bensodiazepiner har en uttalad sederande effekt och kan även användas för att behandla illamående.
D2-receptorantagonister
D2-receptorantagonister är så kallade prokinetiska läkemedel som bland annat stimulerar motiliteten i övre mag-tarmkanalen och relaxerar pylorus, med både central och perifer verkan 167 . Behandling med denna grupp av läkemedel kan utlösa extrapyramidala biverkningar. Metoklopramid används ofta och kan ges intravenöst, subkutant, oralt eller rektalt men bör undvikas vid totalt tarmhinder. Andra behandlingsalternativ vid genombrottsillamående är kombinationspreparat (D2-receptorantagonister och acetylkolin- och histaminreceptorantagonister) 167.
5HT3-receptorantagonister
5HT3-receptorantagonister såsom ondansetron och granisetron, används ofta för att förebygga illamående vid onkologisk behandling 168 . Dessa läkemedel kan ha god effekt på illamående vid palliativ vård men behöver ofta kombineras med andra preparat.
Kortikosteroider
Kortikosteroider ger ofta effektiv symtomlindring, särskilt vid hjärntumörer och metastaserande sjukdomar, även om verkningsmekanismen är oklar. Kortikosteroidbehandling kan också ha flera andra positiva effekter såsom att motverka trötthet, stimulera aptit och lindra smärta. Kortisonbehandling innebär dock ökad risk för gastrit och refluxesofagit. Det är viktigt att överväga behovet av lämpligt syrahämmande medel, dvs. protonpumpshämmare 167.
Neuroleptika
Neuroleptika är en grupp av läkemedel som i första hand används för att behandla psykotiska tillstånd och svår oro och förvirring. Levomepromazin och haloperidol har primärt en rogivande effekt men kan också användas för att behandla illamående och kräkningar 170. Precis som vid behandling med D2-receptorantagonister finns risk för extrapyramidala biverkningar. Olanzapin är ett annat läkemedel som bland annat blockerar dopamin-, serotonin- och histaminreceptorer och är ett atypiskt antipsykotiskt läkemedel. Det kan också användas vid behandling av illamående 167 168 .
NK1-receptorantagonistbehandling
NK1-receptorantagonistbehandling med aprepitant är ett effektivt läkemedel vid behandling av cytostatikautlöst illamående 167 .
Mobilisering och fysisk aktivitet
Fysisk aktivitet inbegriper all kroppsrörelse och syftar till att förbättra alternativt bibehålla kroppens funktioner och minska känslor av trötthet, stress och oro. Fysisk aktivitet kan komplettera medicinsk behandling och öka livskvaliteten, bland annat genom minskad smärta och förbättrad sömn 171 172 173 174 .
Immobilisering (orörlighet) har negativ inverkan på flera kroppsliga funktioner och kan öka risken för andningsproblematik och trycksår. Dessutom minskar känslan av självständighet och välmående om barnet inte kan ändra sitt läge i sittande eller liggande ställning 171 172 174 .
Immobilisering är vanligt förekommande vid allvarlig sjukdom. Ofta har barnet negativa erfarenheter av smärta som tilläggsproblematik, och situationen blir ännu mer komplicerad om barnet inte känner motivation eller lust att röra sig eller känner oro och rädsla. Barnets grad av vakenhet och medverkan kan också göra det svårt att genomföra insatser. Vidare kan de närståendes önskemål vara svåra att möta, särskilt om de inte överensstämmer med det som barnet uttrycker eller önskar. Det är därför viktigt att möta problematiken med respekt och stor lyhördhet för barnets och dess närståendes specifika farhågor och önskemål. Insatser ska erbjudas utifrån ett brett perspektiv med följsamhet och god timing. Barnets närstående behöver involveras tidigt i processen.
Fysisk träning kan ske på många olika sätt, exempelvis lek, vardagsaktiviteter eller individuellt utformade träningssituationer. Rörelser kan ske av egen kraft, eller med hjälp om barnets egen rörelseförmåga inte räcker till. Träningen kan bli en stund av rörelseglädje och en möjlighet att uppleva välbefinnande och njutning i kroppen. Barnet kan genom fysisk aktivitet också få en möjlighet till autonomi och närma sig en önskad självbild 171 172 173 174 .
Barn med svåra funktionsnedsättningar är beroende av andra personer för sin rörelserepertoar och insatser bör erbjudas barnet oavsett funktionsnedsättning, på likvärdig grund 173 .
Fysioterapi kan stödja barnet och de närstående att få balans mellan aktivitet och träning och vila 171 172 174. Det är också viktigt att samtliga i barnets närhet är uppmärksamma på barnets signaler och reaktioner. Mobiliseringsåtgärder ska i första hand öka livskvaliteten och välbefinnandet, och det kan finnas situationer i livets slutskede då det är bättre att avstå än att genomföra exempelvis träningsprogram och lägesförändringar.
Mobilisering kan ske aktivt i olika anpassade former med bland annat funktionell träning, men också i aktivt avlastad form om barnet har nedsatt fysisk funktion och passivt om barnet saknar egen rörelseförmåga.
Positiva effekter av fysisk aktivitet:
- Förbättrad eller bibehållen fysisk funktion.
- Förbättrad sömn.
- Minskad oro och stress.
- Minskad smärta.
- Minskad trötthet.
- Möjlighet att bibehålla sin självbild eller omformulera sitt jag.
- Upplevd autonomi.
- Upplevd njutning, välbehag och rörelseglädje.
- Ökad livskvalitet.
Arbetsterapeuten kan stötta barnet och föräldrarna genom att till exempel upprätta en struktur kring vardagen och lekaktiviteterna och även ge familjen tid för rutiner och egentid 78 .
Munvård och munhälsa
Att ha en god munhälsa är betydelsefullt för välbefinnandet och livskvaliteten. Muntorrhet är vanligt förekommande bland barn med allvarlig sjukdom, och kan göra det svårt att kommunicera och svälja.
Svamp i munnen, i form av en vitaktig beläggning och rodnad munslemhinna, kan svida och förändra smakupplevelser.
Munvård
En god, försiktig munhygien motverkar dålig andedräkt och känns ofta uppfriskande. Munvård kan också innebära en betydelsefull närkontakt mellan de närstående och det döende barnet 15 175176 177.
Gör gärna så här:
- Berätta för barnet vad du ska göra, även om barnet är medvetslöst.
- Inspektera munhålan med ficklampa och spatel, och observera skador, sår, rodnader och beläggningar på tungan och slemhinnan.
- Borsta tänderna med mjuk tandborste alternativt använd munsvabb 1–2 gånger per dygn.
- Torka ur hela munhålan och håll munhålan fuktig med fuktbevarande gel eller saliversättning. Munhålan bör fuktas 1–2 gånger i timmen.
- Smörj läpparna med cerat.
- Ge isbitar, fryst saft eller isglass om barnet fortfarande kan svälja.
- Vid tecken på munsmärta, pröva lokalt smärtstillande läkemedel 15 175176 177.
Mukosit
Mukosit är en form av inflammatorisk slemhinneskada som kan vara mycket smärtsam. Den är vanlig vid viss läkemedelsbehandling och i livets slutskede. Mukosit kan göra det svårt att tala, dricka, äta och utföra munvård. Slemhinnepåverkan kan yttra sig som allt från en lätt rodnad till en kraftig inflammation med sårbildningar. God munhygien och smorda läppar är viktigt för att om möjligt förebygga mukosit. Det är även viktigt med smärtskattning för att kunna ge optimal smärtlindring, eftersom mukositbesvär kan läka långsamt och pågå i flera veckor.
Smärtlindring vid mukosit kräver ofta en kombination av lokala och generellt verkande preparat. Med lokalbehandling kan det bli lättare att utföra munvård, och lättare för barnet att dricka och äta. Många barn, särskilt de yngre, har dock svårt att acceptera lokal smärtlindring och det är viktigt att hela tiden försöka individanpassa behandlingen.
Icke-farmakologisk behandling
Kalla produkter såsom isbitar, isvatten och glass kan ge tillfällig smärtlindring.
Farmakologisk behandling
Lokal behandling:
- Afta Clear (receptfritt) fungerar som skyddshinna på munslemhinnan och finns som munsköljvätska, gel eller munspray. Preparatet innehåller hyaluronsyra som ska påskynda läkning. Det kan användas av alla åldrar och innehåller ingen aktiv bedövningssubstans.
- Lidokain 5 % munhålepasta (receptbelagd) appliceras direkt på området i munnen som behöver bedövas, förslagsvis med hjälp av en öronpinne. Preparatet kan med fördel användas vid enstaka blåsor.
- Morfingel 1 mg/ml (extempore läkemedel) appliceras lokalt på munslemhinnan.
- Andolex (receptbelagt) har en antiinflammatorisk effekt och kan användas som smärtlindrande lösning genom att skölja munhålan eller svabba slemhinnorna i områden som gör ont. Den smärtlindrande effekten är begränsad eftersom preparatet kan ge uttalad sveda i munnen och alkoholhalten är hög (80 %). Detta begränsar preparatets användbarhet.
Generell behandling
För generell behandling av mukosit kan barnet få paracetamol och/eller opioider intravenöst 178.
Nutrition
Palliativ nutritionsvård är en viktig del i den vården av barn med allvarlig sjukdom. Nutritionsbehandlingen varierar beroende på barnets palliativa fas. God nutritionsvård förutsätter ett välfungerande teamarbete där alla yrkesgrupper bidrar med sin kompetens och där alla i teamet känner till målsättningen med behandlingen 119 153 179.
Dietisten i det palliativa teamet har djupgående kunskaper om näringslära och kostbehandling av olika sjukdomar och sjukdomstillstånd samt förståelse för det palliativa vårdförloppet. Dietisten översätter nutritionsåtgärder till konkreta råd och anvisningar som är anpassade efter barnets behov, tidigare matvanor och kulturella och sociala situation.
I tidig palliativ fas syftar åtgärderna ofta till att barnet ska uppnå sitt individuella energi- och näringsbehov. I senare skede kan målsättningen behöva justeras och nutritionsinsatserna vara av mer symtomlindrande karaktär, med mer fokus på måltidernas betydelse för livskvalitet och social samvaro.
Barnets nutritionssvårigheter kan vara påfrestande för hela familjen, så samtal med barnet och de närstående om dessa svårigheter är en viktig del av teamets arbete 179.
Sambanden mellan sjukdom, aptitlöshet och ämnesomsättning måste förklaras på ett begripligt sätt för barnet och de närstående, för att alla ska kunna se till barnets bästa genom hela vårdförloppet. Få saker är så känsliga som mat och dryck till ett svårt sjukt barn 180.
Tidig palliativ fas
Den tidiga palliativa fasen kan vara lång, beroende på barnets tillstånd och grundsjukdom. Det är dock viktigt att starta nutritionsbehandlingen tidigt i sjukdomsförloppet, enligt diagnosspecifika vårdprogram eller riktlinjer. Verksamheten ska ha rutiner för att upptäcka och förebygga undernäring 182 183 .
Det finns screeningverktyg för barn som underlättar nutritionsbedömningen, till exempel: Nutritional risk screeningtool for children aged month-18 years on admission to the hospital (STRONGkids) (screening för risk för undernäring), Screening tool for the assessment of malnutrition in paediatrics (STAMP) och Paediatric Yorkhill Malnutriation score (PYMS) 182 183 .
Vid risk för undernäring bör en dietist kopplas in för individuellt utformad nutritionsbehandling. Målet är också att barnet ska bibehålla ork och styrka för att kunna leva ett så aktivt liv som möjligt, och exempelvis kunna gå i förskola eller skola samt leka och umgås med vänner. Behandlingen syftar till att tillgodose energi-, protein- och näringsbehovet för att stimulera normal tillväxt, förebygga viktnedgång och trycksår, och förstärka immunförsvaret 184 . God nutritionsbehandling kan också bidra till att barnet klarar av medicinska behandlingar utan avbrott. Eftersom tillståndet kan förändras är det viktigt att regelbundet screena barnet för undernäring under hela vårdförloppet.
Viktförlust är vanligt hos barn i palliativ vård och kan bland annat bero på:
- illamående
- aptitlöshet
- smärta
- oro
- förstoppning
- svampinfektion eller sår och blåsor i munnen
- smak- och luktförändringar.
Dessa tillstånd ska om möjligt behandlas men kan också vara ett resultat av sjukdomsförloppet 153 185 .
Figur 3.Principer för nutritionsbehandling
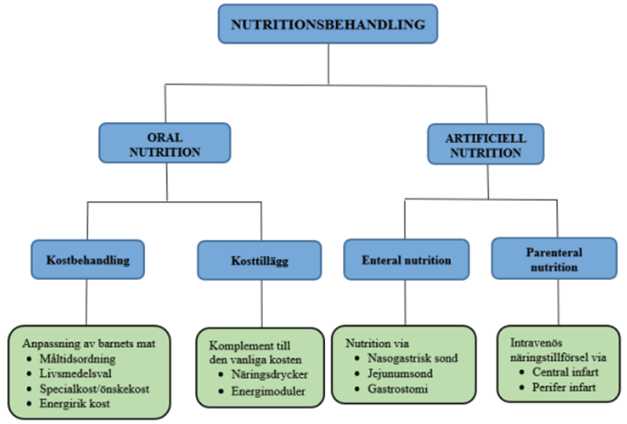
Källa: Regional medicinsk riktlinje för prevention och behandling av undernäring hos barn och ungdomar inom slutenvården, Region Skåne.
Nutritionsbehandlingen bygger på den vanliga maten, eller på bröstmjölk till ett litet barn. Amning eller bröstmjölk bör uppmuntras och stöttas i enlighet med WHO:s amningsråd 186 187 188 189 under alla skeden av sjukdomen. Bröstmjölk och/eller mat kan behöva kompletteras med modersmjölksersättning, kosttillägg eller berikning. Om det orala intaget inte är tillräckligt bör enteral eller parenteral tillförsel övervägas, där enteral nutrition är förstahandsval vid fungerande mag-tarmkanal.
Sen palliativ fas
I den sena palliativa fasen är målsättningen inte längre att tillgodose barnets energi- och näringsbehov, utan nutritionsbehandlingen syftar i stället till att lindra symtom och optimera välbefinnande och autonomi. Om möjligt bör barnet själv vara med och fatta beslut om nutrition i denna fas. Har barnet en välfungerande nutritionsbehandling (med enteral nutrition eller parenteral nutrition) kan den i de flesta fall fortsätta, men behandlingen behöver utvärderas kontinuerligt och omdefinieras beroende på barnets önskningar och situation 119190.
I livets slutskede
Behovet av näring och vätska avtar i livets slutskede. Det är naturligt men kan vara stressande för familj och närstående. Nutritionsåtgärder i livets slutskede handlar oftast om att hjälpa barnet att välja mat och dryck som är lämplig med tanke på aktuella symtom, och att minska stressen och oron runt matsituationen. Barnet kan uppmuntras att äta och dricka det hen vill och kan. Om man har startat nutritionsbehandling i någon form behöver barnet och de närstående informeras om fördelar och nackdelar med att fortsätta den 191 . Beslutet att avsluta behandling med artificiell vätske- och näringstillförsel ska inkludera flera teammedlemmar, men läkaren har det övergripande ansvaret.
Tillförsel av vätska eller näring på artificiell väg kan leda till ödem, andnöd, övervätskning, ökad slemproduktion och aspiration 118 119 192. Det tillhör det naturliga döendet att barnets intag av mat och dryck successivt minskar och till slut upphör helt. I normalfallet innebär det inte att barnet känner obehag i form av hunger eller törst. God munvård är viktigt oavsett om barnet äter eller inte 193 .
Se även Kapitel 11 Det döende barnet.
Oro, ångest och förvirring
Oro, rädsla och förtvivlan är normala krisreaktioner vid allvarlig sjukdom, för både barn och vuxna. Känslorna aktiverar kroppens fysiologiska reglering av stress och medför ofta fysiska symtom samt skärpt uppmärksamhet i syfte att hantera det hot som utlöst stressreaktionen 194. Vanliga symtom vid oro är till exempel; hjärtklappning, hyperventilering, motorisk rastlöshet och sömnstörningar 157 .
Forskning har visat att oro, ångest och nedstämdhet hos barn med livshotande sjukdom kan minska, om vårdnadshavarna och vårdpersonalen talar öppet med barnet om diagnosen och prognosen 47 . För vårdpersonal är det därför viktigt att se och bemöta individen, och att lyssna och föra samtal med öppna frågeställningar om barnet vill.
Stark oro är energikrävande och kan bland annat leda till; nedsatta neurokognitiva funktioner, försämrad livskvalitet och förstärkta fysiska symtom 157 . För sjukvårdspersonal är det viktigt att våga möta barnets och familjens oro, erbjuda mänsklig närvaro och ta reda på vilka behov familjen har.
Ångest kan upplevas som en fysisk smärta samt förstärka smärtupplevelsen, samtidigt som smärtupplevelsen kan utlösa ångest genom att barnet omedvetet upplever att den fysiska integriteten är hotad 195 . Ångest är en stark individuell reaktion på hot om att förlora centrala värden i tillvaron, till exempel relationer till personer (separationsångest) eller själva livet (dödsångest) 157 .
Barn med livshotande sjukdom kan få generell ångest, separationsångest, procedurrelaterad ångest eller dödsångest 196 , dessa typer kan ta sig olika utryck beroende på barnets ålder och utvecklingsnivå.
Påverkan av ångest är fysisk, psykisk och social samt kan beskrivas som en existentiell smärta. Utöver psykosocialt stöd, kan det vara aktuellt med läkemedelsbehandling alternativt att sätta ut läkemedel som kan bidra till ångestproblematik.
Barn uttrycker ofta sin oro eller ångest genom ett inåt- eller utåtagerande beteende 197 med exempelvis aggressivitet, ilska, rädsla, nedstämdhet och smärta. Det är viktigt att barnet blir delaktigt i beslut som rör hens hälsa och behandling. Enligt Patientlagen är sjukvårdspersonalen skyldig att ge information som är anpassad efter barnets ålder, mognad, erfarenhet, språkliga bakgrund samt andra individuella aspekter.
Förvirring (delirium) är ett vanligt symtom bland vuxna vid palliativ vård i livets slutskede 157 , men mindre vanligt för barn med livshotande sjukdom. Förvirring kan ses som en svikt av hjärnans funktion där yttre och inre orsaker kan bidra, till exempel sömnbrist, ny miljö, infektioner, elektrolytrubbningar, läkemedelspåverkan och sömnbrist. I livets slutskede kan även barn utveckla förvirring, och mentalt växla mellan kortare stunder av förvirring blandat med vakenhet. Ett barn som befinner sig i ett tillstånd av förvirring kan ha en ökad motorisk oro eller vara mycket stillsamt.
Icke-farmakologisk behandling
Ett döende barn kan påverkas av sina närståendes reaktioner i form av exempelvis ångest. Det är ytterst viktigt att skapa trygghet för barnet. Vårdnadshavarnas trygghetskänsla och mående påverkar barnets upplevelse av sjukdomen och sjukhusvistelsen, så samarbete med och stöd till hela familjen är betydelsefullt 198 199 .
För att initialt behandla ångest hos det döende barnet bör fokus ligga på kommunikation så att barnet får möjlighet att uttrycka sin oro, ångest och rädsla 196 . Barnets vård måste anpassas till barnets och familjens olika behov och önskemål 200.
Ångest som är associerad med smärta kan behandlas framgångsrikt med hypnos och akupunktur. Annan icke-farmakologisk behandling kan vara avslappning, massage, ”guided imagery” och musikterapi 196 201.
Farmakologisk behandling
Läkemedel vid oro och ångest
Klonidin är ett blodtryckssänkande läkemedel som har dåsighet som biverkan, vilket kan utnyttjas i behandling av svår oro och sömnsvårigheter. Bensodiazepiner har ofta en mycket god rogivande effekt. I valet av bensodiazepinpreparat kan midazolam har stora fördelar i det praktiska kliniska arbetet eftersom det kan administreras buckalt, oralt, intravenöst, subkutant och rektalt och är mer lättstyrt på grund av kortare halveringstid. Diazepambehandling kan ges oralt, rektalt och intravenöst.
Läkemedel som kan utlösa oro och ångest
Bensodiazepiner och opioider kan som biverkan ge ångestproblematik, särskilt om behandlingen sätts ut abrupt 157 . Ångestproblematik kan även ses vid behandling med kortikosteroider och behandling med antikolinergika.
Läkemedel vid förvirring
Neuroleptika fungerar ofta bra för att behandla förvirring. Om barnet är hypoaktivt kan behandling med risperidon öka vakenhetsgraden. Om barnet är hyperaktivt kan man prova haloperidolbehandling.
Palliativ sedering
Det finns avancerade metoder för symtomlindring i livets absoluta slutskede eller i oväntade akuta skeden. Det kan ändå förekomma att barn får otillräcklig lindring av outhärdliga symtom, vilket i sin tur kan leda till stegrad ångest hos både barnet och de närstående. Det kan exempelvis inträffa vid massiva blödningar, hastigt påkommande svår andnöd, agiterat delirium eller outhärdlig smärta, i ett sent palliativt skede. Om det finns stor risk för sådana symtom, bör vårdteamet diskutera möjlighet till palliativ sedering och ha en plan för behandling.
Beslutet att inleda sedering bör först diskuteras med specialister med erfarenhet av palliativ sedering och vara väl förankrat i vårdteamet. Beslut om sedering ska också förankras hos barnet (om det är möjligt) samt med vårdnadshavare. Målet att uppnå symtomlindring bör vara tydligt.
Palliativ sedering innebär kontinuerlig tillförsel av läkemedel till den gräns där barnet inte längre visar tecken på svåra symtom. Djupet på sederingen styrs helt av vad som behövs, för att åstadkomma tillräcklig lindring. Parallellt med sederingen fortsätter man att ge övriga läkemedel som riktar sig mot symtomet i fråga. Beslut om fortsatt nutrition eller vätsketillförsel ska baseras på vad som bedöms gagna barnet.
De två vanligaste läkemedlen som används vid sedering är midazolam och propofol. Sederingen ska inledas och titreras upp av läkare som har god vana av preparatet i fråga 202.
För mer information: Palliativ sedering i livets slutskede. Etiska riktlinjer 2025, Svenska Läkaresällskapet (pdf)
Palliativ strålbehandling
Barn med cancer kan ha tumörer som trycker på nerver och blod- och lymfkärl eller hotar luftvägarna. Tumörerna kan också orsaka svullnad, smärta, blödning och andra symtom. När bot inte längre är möjligt kan kortison, cytostatika och strålbehandling erbjuda symtomlindring, ibland även tumörreduktion. Speciellt skelettmetastaser brukar svara bra på strålbehandling i smärtlindrande syfte, det minskar även risken för patologiska frakturer. Vid ryggmärgspåverkan kan strålbehandling, tillsammans med kortison, vara av värde.
Vid kurativ strålbehandling måste man ta hänsyn till biverkningsrisken på lång sikt. Palliativ strålbehandling kan oftast ges mer koncentrerat under kortare tid, vilket kan underlätta för barnet genom att minska antalet behandlingstillfällen 152 153 154.
Flera studier visar att palliativ strålbehandling hos barn ofta ger god symtomlindring med lindriga biverkningar 203 204 205 206 207 208. Det finns också studier som talar för att strålbehandling av barn i palliativt syfte är ett underutnyttjat behandlingsalternativ 209. Det är därför viktigt att sprida kunskapen om strålbehandling som alternativ i palliativ vård. Målet med palliativ strålbehandling är främst att lindra symtom och förbättra livskvaliteten, det kan även minska behandlingsbördan eller förebygga hotande symtom 203 205.
För mer information: Palliativ strålbehandling av barn, Nationella riktlinjer, Svenska Barnradioterapigruppen, SBRG (pdf).
Smärta
Fysisk smärta är en central del av begreppet ”total pain” och definieras som ”en obehaglig sensorisk och känslomässig upplevelse förknippad med eller liknar den som är förknippad med faktisk eller potentiell vävnadsskada”. Smärta är därmed ett subjektivt symtom som påverkas av många faktorer 210 , optimal smärtlindring beskrivs som en humanitär rättighet.
All smärtbehandling innebär noggrann smärtanamnes, åtgärd, dokumentation och utvärdering. Om möjligt bör man utreda vad som orsakar smärtan. Ofta krävs en kombination av flera insatser och samverkan inom det multiprofessionella teamet. Inför särskilt invasiva utredningar behöver man noga tänka igenom om de kan ge mer information än en klinisk undersökning och om de behövs. Vilka utredningar som kan bli aktuella styrs även av i vilken palliativ fas barnet befinner sig i 211 212 213 .
Smärtanamnes bygger på följande frågor:
- På vilket sätt påverkas barnet av smärtan?
- Är smärtan akut eller långvarig?
- Är smärtan intermittent eller kontinuerlig?
- Är smärtan rörelserelaterad (inflammatorisk)?
- Var är smärtan lokaliserad?
- Hur skattar barnet sin smärta?
- Vilken typ av smärta? Det finns flera typer:
- nociceptiv vävnadssmärta (smärta som uppstår vid retning av nervändar)
- neuropatisk smärta (smärta som hör till nervsystemet), som kan vara central eller perifer neuropatisk smärta
- visceral smärta, dvs. från mage eller tarm, urinblåsa och lungor (viscera)
- visceral hyperalgesi (ökad smärtkänslighet) eller smärta som liknar neuropatisk smärta
- visceral smärta av organisk orsak såsom inflammation, liknar nociceptiv vävnadssmärta
- ”blandsmärta” bestående av flera olika smärttyper, vanlig vid palliativ vård.
Barn kan ha svårt att förmedla eller beskriva smärta, oavsett ålder. Därför bör smärtskattnings- och observationsinstrument ingå i smärtbedömningen. Resultatet går också att följa och utvärdera, och kan därmed bli ett viktigt underlag för dokumentation. Välj smärtskattningsinstrument som är anpassade efter barnets fysiska och kognitiva förmåga, och involvera barnet och de närstående i valet. Vad är de vana vid och vad har fungerat tidigare? Tekniska hjälpmedel kan ytterligare öka barnets möjligheter att uttrycka sin smärta.
Här nedan finns exempel på svenska validerade skalor för små barn och barn som saknar verbal kommunikation, för att bedöma barnets smärta:
- Face, Legs, Activity, Cry, Consolability revised (FLACC-r) 214 .
- Ansiktsuttryck, andningsmönster, extremitetstonus, hand-/fotmotorik, aktivitetsnivå (ALPS2) 215 .
- Beteende, observation & skattning av smärta (BOSS) 216 .
- NCCR-revised 217 .
För äldre barn finns skalor som mer direkt syftar till att ge ett mått på smärtupplevelsen:
- Coloured Analogue Scale (CAS).
- Faces Pain Scale – Revised (FPS-R).
- Numerisk skala (NRS).
- Visuell analog skala (VAS).
Icke-farmakologisk behandling och omvårdnad
Fysioterapi omfattar en mängd olika insatser med syfte att förebygga och lindra smärta 75, 218. Fysioterapeuter har kompetens att bedöma och analysera barnets motoriska beteende 75 173 213. Valet av insatser beror på smärtupplevelsens orsak, situationen och valet av perspektiv (kort- eller långsiktigt). Individuella och miljömässiga förutsättningar påverkar valet av metod och genomförandet. Ibland kan insatsen riktas direkt mot en känd grundorsak, exempelvis vid ledfelställning och trycksår. I övriga fall är det symtomen som är vägledande 219.
Vid smärta på grund av inaktivitet syftar insatserna till att; öka barnets aktivitetsnivå, ge fler möjlighet till lek och delaktighet samt finna balans mellan vila och aktivitet 173 220. Arbetsterapeuten kan stötta barnet och familjen med att prioritera bland alla aktiviteter. Insatserna kan till exempel syfta till att anpassa en aktivitet för att kunna genomföra den eller att fördela energin över en dag, för att orka med det som barnet önskar och uppnå aktivitetsbalans 78.
Vid smärta som är orsakad av muskelspänning, kan insatserna innehålla; avspänningsövningar, massage inklusive magmassage, behandling med värme och kyla, TENS (transkutan elektrisk nervstimulering), vibration 75 218.
Hjälpmedel såsom avlastnings- och positioneringsredskap är viktiga för att både lindra och förebygga smärta. Kunskap om och hjälp till en god positionering av barnet dygnet runt, kan i hög grad förebygga viss smärta 144 173.
Klinisk erfarenhet visar att olika former av sinnesstimulering i vissa fall kan ge distraktion och ha en smärtlindrande effekt. Insatsen kan exempelvis omfatta tyngdtäcke, sinnesrum, bad och musik.
Smärttyper och farmakologisk behandling
För att identifiera lämplig farmakologisk behandling, är det viktigt att skilja mellan nociceptiv vävnadssmärta, neuropatisk smärta och visceral smärta.
Nociceptiv vävnadssmärta
Nociceptiv smärta är en vävnadssmärta och en vanlig smärtorsak hos barn med livshotande sjukdom som exempelvis; onkologisk sjukdom, progressiv neurometabol sjukdom eller encefalopati.
Vid cerebral pares av komplex form, kan spasticitet ge svåra smärttillstånd på grund av; muskelspänningar, ledluxationer (framför allt i höft), snabb progress av skolios, skelettsmärta och skelettskörhet.
WHO:s rekommendation från 2013 innefattar en ”tvåstegstrappa”, framför allt för barn, med:
- Icke-opioider för mildare smärta.
- Starka opioider för moderat eller stark smärta:
Svaga opioider såsom kodein och tramadol rekommenderas inte 152 221.
Icke-opioider
I basbehandlingen ingår paracetamol, COX2-hämmare och klonidin vid nociceptiv smärta och kan administreras både oralt, rektalt och intravenöst.
- Regelbunden dosering 3–4 gånger per dygn vid mer kontinuerliga och svåra smärttillstånd. Anslagstiden är dock relativt lång, framför allt peroralt (cirka 2 timmar), rektalt (okänd tid) och intravenöst (cirka 1 timme).
- Upptag sker i tunntarmen. Det är viktigt att ventrikeltömningen fungerar normalt vid administrering via munnen eller via gastrostomi.
- Viss försiktighet krävs vid leversjukdom 213. En kortvarig högre dos kan behövas vid smärta varefter dosen sänks med cirka 20 % efter 3–4 dagar.
Cox-hämmare (NSAID) kombineras med fördel med paracetamol.
- Det är framför allt effektivt mot inflammatorisk och rörelseutlöst smärta. Vanligt förekommande NSAID-preparat för barn är ibuprofen, naproxen och diklofenak. Det finns risk för biverkningar såsom gastrit och blödning.
- Hos barn med ökad blödningsrisk och låga trombocytnivåer bör cox2-hämmare ges i stället för NSAID, till exempel celecoxib peroralt (kapsel där pulvret kan lösas upp och ges inom 30 minuter) eller parecoxib intravenöst. Var försiktig vid nedsatt njurfunktion 213.
Både paracetamol och cox-hämmare har en feberhämmande effekt.
Klonidin är en α2-adrenoreceptoragonist som hjälper vid; nociceptiv, neuropatisk och visceral hyperalgesi eller smärta samt vid spasticitet, oro och autonom dysfunktion. Trötthet är en biverkan som man kan dra nytta av, för att öka sederingen eller förbättra nattsömnen. Hos vuxna och äldre finns risk för blodtrycksfall, det ses dock mer sällan hos mindre barn 213. Klonidin har ingen andningspåverkan och kan administreras peroralt, intravenöst och nasalt.
Dexmedetomidin är en annan α2-adrenoreceptoragonist som har en ännu starkare sederande effekt än klonidin. Den används framför allt inom intensivvården 213.
Esketamin är ett potent analgetikum, men ett anestetikum vid högre doser. Den analgetiska effekten sker genom blockering av NMDA-receptorn, vilket gör att läkemedlet även fungerar vid neuropatisk smärta. Biverkningarna är oftast dosrelaterade och omfatta hallucinationer och mardrömmar samt högt blodtryck. Detta kan förebyggas eller lindras med hjälp av bensodiazepiner. Vid smärta kan esketamin användas som kontinuerlig lågdosinfusion för att förstärka effekten av andra läkemedel, exempelvis opioider. Esketamin kan även ges peroralt eller subkutant och har mindre biverkningar än ketamin. Det kan även användas för att minska så kallad ”wind-up”, det vill säga när smärtsystemet har fått en ökad känslighet mot smärta.
Starka opioider
Om paracetamol och eller cox-hämmare inte ger tillräcklig effekt, eller om det finns kontraindikationer, ger man en stark opioid. Starka opioider är en del av basbehandlingen vid medelsvår till stark nociceptiv smärta. De kan delas in i; kortverkande, medellångverkande och långtidsverkande utifrån tiden till analgetisk effekt. De kan även ges i många olika beredningsformer och administreras på olika sätt, utifrån barnets behov. Vid regelbunden eller kontinuerlig behandling, ska barnet ha tillgång till vid behovsdoser.
Valet av opioid beror på om man önskar någon särskild effekt eller om det finns särskild anledning till att undvika någon opioid.
När man sätter in en opioid är det viktigt att beakta följande frågor:
- lämplig opioid
- lämplig dos
- lämpligt administrationssätt
- byte av opioid, s.k. ”opioidrotation”.
Biverkningar såsom klåda och illamående bör behandlas med antihistamin och antiemetika.
Förstoppning behandlas med:
- bulkmedel, osmotiska laxantia och makrogol
- eventuell motorikstimulerare i form av natriumpikosulfat
- vid behov tarmtömning med hjälp av till exempel sorbitol rektalt
- vid regelbunden behandling – mixtur Naloxon x 4 per dygn, per os
- för äldre barn – Naloxegol (Moventig R) x 1 per dygn.
Andningsdepression är en ovanlig biverkan av opioider, framför allt om barnet har behandlats med opioider i över en vecka och därmed har utvecklat viss tolerans (inte är opioidnaiv).
Opioidrotation. Olika opioider har olika analgetisk effekt och biverkningsprofil, vilket kan utnyttjas för så kallad ”opioidrotation”. Det innebär att byta en opioid mot en annan för att; påverka biverkningsprofilen, åstadkomma bättre analgetisk effekt eller minska toleransutveckling 213. Det finns dock en inkomplett korstolerans mellan preparaten vid opioidrotation. Vid biverkningar eller toleransutveckling bör dosen sänkas med 25 % av ekvianalgetisk dos. Vid bristande effekt kan man behålla den ekvianalgestiska dosen. Opioidrotation ska ske i samråd med en erfaren läkare.
Vid byte av opioider ska en konverteringsguide för opioider användas
konverteringsguide-opioider-2023.pdf.
Se bilaga Läkemedelsbehandling vid palliativ vård av barn.
Toleransutveckling vid behandling med opioider kan uppstå, vilket kan innebära ökad smärta och behov av en doshöjning. Om man önskar minska dosen, måste det göras med hänsyn till risk för abstinens.
Opioiddoserna behöver anpassas till barnets ålder, vikt, smärttillstånd samt beroende på den opioid som används (analgetisk effekt) 222 223 .
Morfin är den opioid som har använts längst och är referenssubstans för övriga opioider. Morfin tolereras ofta väl av barn och väljs oftast i första hand, om barnet inte har njursvikt. Det är en medellångverkande opioid som kan administreras på många sätt. Vid övergång från intravenös till peroral behandling är ratio (kvoten) cirka 1:2-3, alltså 2-3 gånger högre vid peroral dos på grund av sämre biotillgänglighet 213 .
Oxikodon har en liknande farmakokinetisk profil som morfin och är medellångverkande. Substansen har bättre biotillgänglighet peroralt, vilket ger ratio cirka 1:1,5 vid övergång från intravenös till peroral oxikodon 213 . Oxikodon är att föredra framför morfin vid nedsatt njurfunktion, men för övrigt finns få fördelar jämfört med morfin. Det är dock en bra opioid att använda vid opioidrotation.
Ketobemidon är ett andrahandsalternativ till morfin eller oxikodon. Det är en medellångverkande opioid som inte bildar några metaboliter. Den har dock en mer fettlöslig profil och kan därmed ge en så kallad ”kickeffekt” vid intravenös dosering, den bör därför ges långsamt och användas med försiktighet. Ketobemidon kan vara aktuellt vid opioidrotation om barnet har besvärande biverkningar som illamående, klåda 213 och njursvikt.
Hydromorfon liknar morfin men är 5–7 gånger mer potent, används när man önskar ge mindre volymläkemedel, exempelvis vid subkutana injektioner.
Fentanyl är en mer fettlöslig och snabbverkande opioid än morfin. Den används exempelvis när det behövs mycket snabb lindring och intravenös infart saknas. Den kan även ges nasalt. Fentanyl finns också som smärtplåster vid mer kontinuerlig stabil nociceptiv smärtsituation, och ger då en jämn nivå i blodet. Vissa plåster (endast matrixplåster) kan klippas i mindre bitar 213. Plåstret ska bytas med 2–3 dygns mellanrum. Se till att det inte ramlar bort eller rivs av, eftersom det finns risk för allvarlig abstinens. Med tanke på det höga opioidinnehållet, kan det även vara farligt för syskon eller husdjur.
Metadon är en långverkande opioid som även blockerar NMDA-receptorn (som är en del i neuropatisk smärta). Metadon har mycket god biotillgänglighet peroralt, rektalt, nasalt och buckalt. Substansen används framför allt tillsammans med en annan opioid för att potentiera effekten, kan även användas som enda opioid och som långverkande grundbehandling. Metadon ska sättas in i samråd med läkare som är van vid preparatet. Halveringstiden är lång och kan variera påtagligt mellan olika individer.
Neuropatisk eller neurogen smärta
Neuropatisk smärta beror på en skada eller en sjukdom i det somatosensoriska systemet. Det beskrivs ofta som en brännande, stickande känsla och som allodyni (smärta i huden vid lätt beröring). Tillståndet är ofta heterogent och svårbedömt. Olika sjukdomstillstånd kan leda till neuropatisk smärta. Vid onkologisk sjukdom kan tumörens läge ge smärta, liksom behandlingen av den. Hos exempelvis neurologiskt sjuka barn kan sjukdomstillståndet i sig medföra neuropatisk smärta. Det går inte att kliniskt testa neuropatisk smärta hos barn på samma sätt som hos vuxna, ibland kan man behöva pröva en empirisk behandling (grundad på klinisk bedömning och erfarenhet) 211 .
Överväg empirisk behandling vid till exempel:
- Smärta utan att man ser en ”nociceptiv orsak” eller kan identifiera.
- Intermittent smärtbeteende som ökar med tiden.
- Symtom som är associerade med neuropatisk smärta.
- Symtom i samband med matning eller tarmrörelser, alltså visceral hyperalgesi.
- Plötslig och intensiv smärta eller återkommande smärtbeteende.
- Persisterande muskelspasmer eller spasticitet, eller ökade besvär.
- Dysautonomi (autonomisk dysfunktion).
- Symtom som börjar efter kirurgi.
- Sjukdom som är associerad med neuropatisk smärta, exempelvis Krabbes sjukdom.
Klonidin är en α2-adrenoreceptoragonist som hjälper vid nociceptiv, neuropatisk och visceral hyperalgesi eller smärta samt vid spasticitet, oro och autonom dysfunktion.
Gabapentin är ett förstahandsläkemedel för att behandla neuropatisk smärta hos barn 211 och det läkemedel som är godkänt på indikationen perifer neuropatisk smärta. Gabapentin har dock effekt mot både perifer och central neuropatisk smärta samt visceral hyperalgesi eller smärta, dysautonoma symtom och spasticitet 211 224 . Det kan ibland ge oerhört god symtomlindring. Gabapentin stabiliserar nervfunktionen, exempelvis via kalciumjonkanaler. Läkemedlet kan ges som kapsel (som går att öppna) och som mixtur (licens).
Gabapentin ges regelbundet 3–4 gånger per dag och behöver trappas upp under cirka 1–2 veckor, ibland mer och ibland mindre, beroende på behovet av lindring och de biverkningar som uppstår. Biverkningarna kan lindras genom en långsammare upptrappning, barn förefaller dock ha färre biverkningar än vuxna. En biverkan är bland annat trötthet, det kan därför vara lämpligt att börja behandling till natten samt att till en början även förlägga doshöjningar då.
Efter cirka en vecka når man en första behandlingsdos som behöver utvärderas, därefter kan dosen behöva höjas om effekten inte är tillräcklig eller om symtomen återkommer. Det kan dock ta flera dagar innan den smärtlindrande effekten uppträder. Dosen per kg för barn kan behöva vara betydligt högre än för vuxna, framför allt för barn under 5 års ålder 211 224. Vid utsättning ska gabapentin om möjligt trappas ut.
Pregabalin kan övervägas för äldre barn och ungdomar, framför allt om de även har en generell ångestproblematik, men har i övrigt sällan några kliniska fördelar jämfört med gabapentin. Det finns också en större klinisk erfarenhet av att använda gabapentin jämfört med pregabalin för barn 140.
Amitriptylin är ett tricykliskt antidepressivum (TCA) som i lågdosbehandling kan ge god effekt på neuropatisk smärta. Det är ett andrahandsmedel för barn som kan ges som singelbehandling eller tillsammans med gabapentin. Amitriptylin höjer nivåerna av serotonin och noradrenalin genom att hämma det presynaptiska återupptaget i centrala nervsystemet. Amitriptylin hjälper framför allt vid central neuropatisk smärta och visceral hyperalgesi eller smärta. Biverkan är muntorrhet och trötthet, varför det oftast är bäst med en dos till natten. Om nattdosen är svår att tolerera kan en dosering morgon och kväll underlätta. Det är då lämpligt att förlägga den högre dosen till natten, med fördelningen cirka 30/70 för morgon/kväll 224. Vid utsättning, ska TCA om möjligt trappas ut.
Karbamazepin är liksom gabapentin en antiepileptika och används framför allt vid exempelvis trigeminusneuroalgi, då en specifik nerv är påverkad och ger svår smärta i det området. Karbamazepin är mindre använt hos barn.
Metadon och esketamin kan övervägas vid behandling vid svår neuropatisk smärta.
Opioider har vanligtvis dålig effekt på neuropatisk smärta men kan ibland användas som tilläggsbehandling.
Visceral smärta och hyperalgesi
Visceral smärta är smärta som uppstår i bukhålans organ, lungsäcken eller hjärtsäcken. Visceral smärta kan vara av nociceptiv typ och orsakas av till exempel inflammation eller ischemi, såsom vid blindtarmsinflammation eller gallbesvär. Smärttillståndet kan även drabba barn med spridd cancer i bukhålan, det beror då på att tarmväggen, njurvägarna eller gallvägarna påverkas av tumörväxten. Initialt hjälper ofta paracetamol och vid behov även opioider. I ett senare skede, när tumören växer till, kan barnet få kolik eller spasmer. Den kliniska bilden kan vara svårbedömd, till exempel kan extra doser av opioider i stället leda till ökad smärta. Vid sådan smärta kan behandling med läkemedel mot kolik och spasm såsom NSAID med tillägg av butylskopolamin (Buscopan), ge mycket god lindring.
Visceral hyperalgesi är vanligt hos till exempel barn med neurologisk sjukdom och påminner då mer om neuropatisk smärta. Tarmrörelser och andra symtom från buken, som vanligtvis inte orsakar smärta, tolkas då som smärtsamt. Det är ofta relaterat till födointag, tarmrörelser, oro, ökad dystoni, kräkningar och svårighet att tolerera föda. Om man misstänker visceral hyperalgesi bör en empirisk behandling provas, i första hand med gabapentin och i andra hand med amitriptylin.
Procedursmärta
De flesta barn inom palliativ vård har gått igenom en period med intensiva och täta sjukhuskontakter som ofta har inneburit olika smärtsamma procedurer. Förhoppningsvis har smärtan kunnat lindras väl och proceduren har gjorts under trygga, lugna förhållanden. Tyvärr förekommer det fortfarande att barn har upplevelser av smärta, oro, otrygghet och bristande information med sig i bagaget. Dessa upplevelser kan leda till rädsla som förstärker smärtupplevelsen. Inom palliativ vård bör man försöka att minimera smärtsamma procedurer och noga följa kunskapsdokumentet om procedursmärta vid de ingrepp som planeras. Med god planering, noggrann information, förberedelse, rätt läkemedel och trygg omgivning bör man kunna leva upp till målet att inte utsätta barn i palliativ vård för smärta i samband med procedurer.
För mer information:
Riktlinjer för smärtbehandling hos barn – akut och postoperativ smärta
Smärta hos barn och ungdomar, Läkemedelsboken
Läs även mer här:
Fatigue och sömn
Fatigue
Fatigue är ett av det vanligaste rapporterade symtomen hos barn i palliativ vård. Det beskrivs som en överväldigande och försvagande känsla av utmattning som begränsar livet och som inte går att vila sig fri från 225 . Fatigue kan även yttra sig som depression, nedstämdhet, humörsvängningar, brist på motivation och känslan av att inte vara sig själv. Koncentrationsförmågan och minnet blir sämre 225 . Fatigue påverkar på så sätt barnets livskvalitet i flera dimensioner; fysiskt, psykiskt, socialt och kognitivt. Även vårdnadshavare rapporterar fatigue som ett besvärande symtom 226 227.
Orsakerna till fatigue kan vara sjukdomsrelaterade och behandlingsrelaterade samt är vanligt förekommande i alla faser av palliativ vård, särskilt i livets slutskede. En bidragande orsak kan vara; dåliga blodvärden, smärta, feber och nutritionssvårigheter. Även störd sömn på grund av oro, medicinering och nattliga kontroller kan bidra 226 227 .
Icke-farmakologisk behandling
Barnet och familjen behöver stöd i att strukturera dygnet så att barnet kan hushålla med sin kraft. Ett dygnschema bör innehålla rutiner för vila och sömnhygien. Måttlig fysisk aktivitet och lågintensiv träning kan minska fatigue. Se även avsnitt 14.15.2 Sömn.
Arbetsterapeuter är en god resurs när det behövs stöd i att se över aktivitetsmönster och ge stöd till aktivitetsprioritering. Arbetsterapeuten kan stötta med dygnsschema och aktivitetsbalans som en icke-farmakologisk behandling samt arbeta med meningsfulla aktiviteter, stimuli pauser och rutiner för sömnhygien 78.
Sömn
Sömn är nödvändigt för barn, oavsett om de är friska eller sjuka. Sömnen ger återhämtning och vila för både barnet och hela familjen, och är nödvändig för barns tillväxt, utveckling och psykiska hälsa. Även friska barn kan ha sömnproblem, men det är betydligt vanligare hos barn med livshotande sjukdom 228 229 . Brist på sömn eller en störd sömn, kan leda till försämrad livskvalitet på grund av trötthet på dagen, huvudvärk och retlighet. Det kan även förvärra smärta och öka risken för fatigue 225 .
Barn med gravt nedsatt syn kan sova sämre, eftersom de inte ser det dagsljus som påverkar den naturliga sömnregleringen 225 .
Sömnproblem hos barn kan yttra sig som:
- störd dygnsrytm
- uppvaknanden under natten
- svårighet att somna på kvällen
- svårighet att somna om på natten
- nattskräck eller ångest och oro under natten 230 231 .
Störd sömn kan ha psykologiska orsaker såsom oro över livssituationen, dödsångest, separationsångest och rädsla för mörker 225 . En viktig del av arbetet för bättre sömn, är att observera barnet när det somnar och sover. Sömnen kan analyseras utifrån skattningsskalor såsom VAS och BEARS sömnscreeningverktyg 232 som används för att ta en sömnanamnes. Sömndagbok kan också vara ett bra hjälpmedel 233 .
Störd nattsömn kan även förvärra andra symtom, till exempel smärta 225 . I livets slutskede kan barnet pendla mellan sömn och medvetslöshet, vilket innebär att det kan vara svårt att bedöma vakenhetsgraden. Det är dock mycket viktigt att alltid tala till barnet som om hen fortfarande kan höra 157 .
Störd sömn hos barn med livshotande sjukdom och vårdbehov kan upplevas som ett stort problem av vårdnadshavarna 231 234 , eftersom hela familjen påverkas. Vårdnadshavare som redan lever i en stressad situation och som blir väckta flera gånger per natt, kan drabbas av psykisk utmattning, vilket delvis kan bero på den störda sömnen 228 .
Beroende på sömnproblemets orsak samt barnets behov, finns en rad icke-farmakologiska och farmakologiska åtgärder att sätta in.
Icke-farmakologisk behandling
De vanligaste icke-farmakologiska åtgärderna handlar om att se över sovrutiner och pröva olika avslappningsbehandlingar.
Sovrutiner och sovmiljö är viktiga, och enkla förändringar kan ge stora resultat och stärka vårdnadshavarna
Individuellt utformade sovrutiner kan innehålla flera olika åtgärder:
- anpassad säng och speciell madrass
- omslutande bäddning
- vändschema (hjälp till lägesändring under natten)
- justering av barnets egen viloställning med eller utan positioneringskuddar
- ett varmt bad om möjligt eller användning av värmedyna
- minimering av yttre faktorer såsom ortoser, korsett eller annat som kan ge tryck
- minskad tystnad genom att sjunga eller spela svag musik
- rörelse genom att barnet vaggas i en vagn eller gunga eller får ligga i en vattensäng 173 .
Olika avslappningsbehandlingar såsom massage kan hjälpa barnet att slappna av och sova
Avslappningsbehandling kan ge bättre sömn:
- När andningstekniker kan tillämpas är det en mycket god hjälp för att minska spänning i kroppen och öka välbefinnandet. Här kan fysioterapeuten vägleda både barn och vårdnadshavare. Generellt gäller att nattsömnen blir bättre om man växlar mellan aktivitet och vila under dagen.
- Massage kan ges i olika former och variera från lätt beröring av exempelvis pannan till mjuka strykningar över rygg, mage eller annan vald kroppsdel. Ofta känner även den som ger beröringen ett ökat lugn. Det vetenskapliga stödet är otillräckligt när det gäller palliativ vård av barn, men klinisk erfarenhet talar för positiva effekter 157 173 .
Farmakologisk behandling
För att förbättra sömnen är det viktigt att identifiera orsaken och behandla med utgångspunkt från det. En del orsaker kan vara medicinska som exempelvis:
- epileptiska anfall
- dystoni (onormal muskeltonus)
- myokloni (muskelryckningar)
- reflux
- smärta
- spasticitet.
Behandling med melatonin
Melatonin är ett kroppseget hormon som kan inducera sömn vid sömnproblem, till följd av störning av den biologiska dygnsrytmen samt vid sömnsvårigheter och dygnsrytmstörningar hos barn med neuropsykiatriska funktionshinder och neurologisk sjukdom. Personer som är blinda eller har nedsatt synförmåga kan ha nedsatt styrning av melatoninutsöndring via dagsljuset.
Tänk på detta vid melatoninbehandling:
- Doseringen är individuell och lägsta effektiva dos bör eftersträvas.
- Melatonin rekommenderas inte till barn under 2 år men kan ges vid särskilda omständigheter.
- Dosen bör ges cirka 30–60 minuter före insomnade.
- Melatonin finns som mixtur (beredning från Apotek Produktion & Laboratorier) och i tabletter som kan krossas och slammas upp och ges via exempelvis gastrostomi (inte genom tunna sonder såsom jejnunalsond eller nasogastrisk sond) 235 .
