Palliativa vårdbehov ur olika sjukdomsperspektiv
Hos patienter med livshotande sjukdom/tillstånd ska palliativa vårdbehov övervägas, och palliativ vård erbjudas, ofta samtidigt med aktivt sjukdomsbegränsande behandling. Under sjukdomens förlopp ökar ofta det palliativa vårdbehovet och effekten av aktiva behandlingar minskar. Det gäller bland annat vid organsviktsjukdomar och generaliserade cancersjukdomar som är de vanligaste folksjukdomarna.
Kognitiva sjukdomar
Vad är kognitiv sjukdom?
Med kognitiv sjukdom menas en kognitiv funktionsnedsättning som orsakas av en fortskridande neurodegenerativ sjukdom, och som är så uttalad att patienten har svårt att klara sitt vardagliga liv 325 326. Den kognitiva nedsättningen ska ha varat i minst 6 månader och inte ha någon annan behandlingsbar orsak, för att det ska räknas som en kognitiv sjukdom. Demens är alltså inte en sjukdom utan en beskrivning av hur uttalad kognitiv funktionsnedsättning en person har 325. Flera olika sjukdomar kan leda till demens.
Svensk diagnostik baseras på ICD-10, och i både den och den kommande ICD11-versionen finns begreppet demens. I den nya DSM5 har kognitiv sjukdom däremot ersatts av termen kognitiv sjukdom 326.
Orsaker
Den vanligaste orsaken till kognitiv funktionsnedsättning är Alzheimers sjukdom som står för ungefär två tredjedelar av alla fall av demens 327 328 329. Ungefär 25 % orsakas av vaskulär sjukdom, cirka 15 % av Lewykroppsdemens och 3–5 % av pannlobssjukdom. En viktig differentialdiagnos till neurodegenerativ sjukdom är normaltryckshydrocefalus som kan debutera med enbart kognitiv svikt innan urininkontinens och gångrubbning tillkommer. I senare stadier av Parkinsons sjukdom och ALS samt vid långvarig alkoholöverkonsumtion tillkommer även kognitiv nedsättning som ofta är progressiv.
Det är också vanligt att personen har flera kognitiva sjukdomar, vilket kallas multietiologisk kognitiv sjukdom eller blandform. Vanligast är en kombination av Alzheimers sjukdom och vaskulär sjukdom. Denna blandform är troligen den vanligast förekommande i högre åldrar. Sammantaget finns det uppskattningsvis ett hundratal olika kognitiva sjukdomar och tillstånd som kan leda till grav kognitiv nedsättning. Den kliniska bilden kan variera mycket i början av förloppet men tenderar att bli alltmer ensartad i livets slutskede. Det är dock viktigt att ha kännedom om etiologisk diagnos eftersom bemötandet behöver anpassas även i senare skeden, framför allt utifrån patientens sjukdomsinsikt.
Förekomst
Ungefär 1 % av befolkningen som är 65 år och äldre har försämrad kognitiv funktion till följd av sjukdom. Vid 85 års ålder är 20 % av befolkningen diagnostiserade med en kognitiv sjukdom, och 50 % av dem som är 90 år eller äldre har en kognitiv sjukdom 327 330 331.
Den starkaste riskfaktorn för demens är hög ålder. Givet en åldrade befolkning ökar antalet personer med kognitiv sjukdom, både i Sverige och i världen. I Sverige finns för närvarande 130 000–150 000 personer med kognitiv sjukdom, och i världen finns cirka 47 miljoner sådana patienter. År 2050 kommer uppskattningsvis cirka 240 000 personer i Sverige och 130 miljoner personer i världen att lida av demens 330 331.
Symtombild
De olika kognitiva sjukdomarna leder till nedsättning i kognitiva (intellektuella), emotionella (känslomässiga) och centrala varseblivningsfunktioner och motoriska funktioner. Vanligen försämras minnet och förmågan att planera och genomföra vardagliga sysslor. Språk, tidsuppfattning och orienteringsförmåga är andra kognitiva förmågor som påverkas negativt. Detta innebär nedsatt förmåga att tänka abstrakt, försämrat omdöme och praktiska svårigheter att utföra olika handlingar. I slutskedet får personen svårt att gå, tala och svälja.
Symtomskattning
Många med kognitiv sjukdom får svårt att uttrycka sig verbalt. För att bedöma smärta kan man då använda det validerade instrumentet Abbey Pain Scale 332 333. Instrumentet bygger på röstuttryck (gnyr, jämrar sig, låter), ansiktsuttryck (spänd, rynkar näsan, jämrar sig), förändrat kroppsspråk, förändrat beteende och fysiologiska förändringar (förändrad kroppstemperatur, puls, blodtryck, svettningar, rodnad, blekhet i hyn) 332 333. Den så kallade SÖS-stickan kan också vara ett alternativ. Doloplus-2 är ett annat bedömningsinstrument som är framtaget för att mäta smärta bland äldre med nedsatt kommunikationsförmåga 334 335. MOBID kan användas för symtomskattning vid demens 336. Personalversionen av IPOS är en annan möjlighet när patienten inte kan berätta själv 337, även om erfarenheten vid just kognitiv sjukdom ännu så länge är begränsad.
Prognos och behandling
Det finns i dagsläget ingen botande behandling för någon av de kognitiva sjukdomarna 329 . Det innebär att sjukdomen förr eller senare kommer att leda till döden, och patienten kan ha palliativa vårdbehov redan från diagnostillfället. Utifrån klinisk erfarenhet är försämringstakten under det senaste året eller halvåret en relativt tillförlitlig prognostisk markör om inget akut inträffar.
Kognitiva sjukdomar är i dag Sveriges fjärde största folksjukdom. I Sverige insjuknar årligen cirka 25 000 personer och ungefär lika många avlider med demens 329. I dödsorsaksregistret (2018 års statistik) uppgavs demens som den primära dödsorsaken hos 12 500 personer. De vanligaste dödsorsakerna vid svår kognitiv nedsättning är lunginflammation och ischemisk hjärtsjukdom 338. Vården av personer med kognitiva sjukdomar kostade 2019 drygt 81 miljarder kronor, vilket är mer än kostnaden för till exempel cancersjukdomar och hjärt- och kärlsjukdomar tillsammans 322.
Dialog om prioriteringar från diagnos till livets slutskede
Vid kognitiv sjukdom är det särskilt viktigt att tidigt i sjukdomsförloppet tala med patienten om vad hen tycker är viktigt för sin resterande tid i livet. Här fyller samtal vid allvarlig sjukdom en viktig funktion och ett sådant bör planeras in tidigt efter att patienten har fått sin diagnos. Så länge patientens kognitiva funktioner medger det bör man även tala om hens önskemål och tankar inför livets slutskede. Särskilt komplext är det om patienten redan i tidigt skede efter diagnos saknar sjukdomsinsikt och möjlighet att reflektera över sin situation. I dessa fall får ofta närstående vara mycket delaktiga. Det är som alltid viktigt att dessa samtal dokumenteras i journalen och att informationen görs tillgänglig för all inblandad personal. Det kan exempelvis gälla synpunkter på framtida vårdåtgärder eller vem som ska företräda patienten när hen inte längre kan uttrycka sin vilja.
Tecken på övergång till livets slutskede
De sista åren i livet för en person med kognitiv sjukdom kännetecknas av en gradvis försämring av olika funktioner. Personen får uttalade fysiska och kognitiva funktionsnedsättningar till följd av den omfattande, fortskridande, neurodegenerativa sjukdomen. Patienten förlorar flera basala motoriska funktioner, såsom att gå eller hantera grundläggande ADL. Förmågan att kontrollera urin och avföring försämras också successivt. Samtidigt förlorar patienten även förmågan att äta själv, vilket innebär att hen behöver hjälp för att få i sig tillräckligt med näring. Eftersom personen kan ha svårt att tugga maten och svälja (oral apraxi), samt få uttalade sväljningssvårigheter, finns en risk för att maten samlas i munnen och att personen i värsta fall aspirerar. Måttliga eller svåra beteendemässiga och psykiska symtom vid kognitiv sjukdom (BPSD) är associerat med en ökad risk för att dö i förtid.
Kognitiva sjukdomar har ofta ett långsamt förlopp, och det kan vara svårt att bedöma rätt tidpunkt för brytpunktssamtal vid övergång till palliativ vård i livets slutskede. Det finns dock några tydliga kliniska tecken på att personen befinner sig i slutstadiet av sjukdomsförloppet 339 340 341 342 343 344 345 346 347 348:
- uttalade sväljningssvårigheter
- upprepade infektioner (vanligt med upprepad remittering till sjukhus på grund av detta)
- sängbundenhet eller mycket nedsatt gångförmåga
- uttalad nedsättning av eller förlust av språkförmåga.
Prognosen är nu dyster 343 344 345 346 347 348 och det är viktigt att våga samla de närstående (och patienten om möjligt) för det viktiga brytpunktsamtalet. Det är också viktigt att samtala om hur den sista tiden kan se ut och ”för vems skull” olika insatser ska göras. Brytpunktsamtalet är i många fall snarare en serie samtal där målsättningen med vården gradvis anpassas utifrån vad som är möjligt och rimligt.
Vid övergången till livets absoluta slutskede är det, utifrån klinisk erfarenhet, inte ovanligt att patienten minskar i vikt, trots försök att bibehålla optimal nutrition (med näringsdrycker, konsistensanpassning och matning). Detta indikerar övergång i en katabol eller kakektisk sjukdomsförlopp som inte går att vända med externt nutritionsstöd. När detta inträffar tyder klinisk erfarenhet på att personen som lider av svår demens har mycket begränsad tid kvar i livet (även om tidsförloppet är individuellt).
Dialog om prioriteringar i tid
Det är viktigt att i tid våga tala med patienten om vad hen tycker är viktigt i livets slutskede, medan hens kognitiva funktion medger det. Det är också viktigt att dessa samtal dokumenteras i journalen och att informationen görs tillgänglig för all inblandad personal. Det kan exempelvis gälla synpunkter på framtida vårdåtgärder eller vem som ska företräda patienten när hen inte längre kan uttrycka sin vilja.
Behandling och omvårdnad
Vården ska präglas av ett personcentrerat förhållningssätt och bygga på multiprofessionella team. Stöd till närstående är också en viktig faktor 349. Personer med kognitiv sjukdom dör ofta på kommunala vård- och omsorgsboenden för äldre 350 351. Det är särskilt viktigt att vårdpersonalen har kompetens för och erfarenhet av att vårda personer med grav kognitiv nedsättning samt känner patienten eftersom kommunikationen ofta bygger på att tolka ansiktsuttryck och kroppsliga tecken på olika symtom. Här utgör teamarbete i samband med registrering i BPSD-registret ett utmärkt stöd för personcentrerad vård och omsorg (www.bpsd.se), även om patienten inte har BSPD.
Smärta, andnöd, oro, illamående, förvirring och rosslig andning är vanliga symtom hos personer i livets slutskede. 201 348 352 353. Det är viktigt att identifiera, behandla och lindra dessa tillstånd. Behandlingen av olika symtom är densamma för patienter med grav kognitiv nedsättning som för andra personer i livets slutskede och bör så långt det är möjligt vara orsaksinriktad.
Vården bör inriktas på att ge största möjliga välbefinnande och utföras av den personal som känner personen bäst. För att kunna trygga situationen för patienten och de närstående krävs goda kunskaper både om kognitiva sjukdomar och om palliativ vård. Kommunikation med patienten och de närstående ställer stora krav på vårdpersonalen eftersom de flesta patienter som lider av demens och befinner sig i livets slutskede för länge sedan förlorade förmågan till verbal kommunikation 332 354. Strävan är att patienten ska vara symtomlindrad och att vidbehovsläkemedel ordineras i tid för att uppnå god symtomlindring när det blir aktuellt (mot smärta, illamående, oro, andnöd, rosslighet och ångest).
Icke-farmakologisk behandling används i vården av och omsorgen om personer med kognitiv sjukdom. Exempelvis kan bolltäcke, mjuk massage/beröring, TENS (transkutan elektrisk nervstimulering) och musik ha effekt även i livets slutskede.
Förhållningssätt under sjukdomsförloppet vid kognitiv sjukdom
European Association of Palliative Care (EAPC) har publicerat internationella riktlinjer för palliativ vård vid demens, baserat på vetenskaplig evidens 355. Sammantaget innehåller riktlinjerna 57 rekommendationer inom 11 domäner som nu också finns översatta till svenska356. Figuren nedan visar rekommenderat förhållningssätt under olika sjukdomsförlopp av förloppet vid demens, baserat på EAPC:s riktlinjer 355.
Figur 4. Förhållningssätt under sjukdomsförloppet vid demens
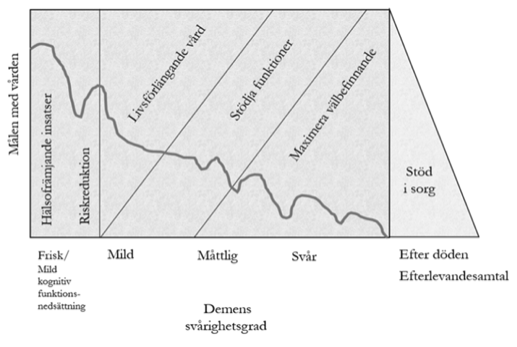
Källa: Palliativ vård vid demens, Gothia Fortbildning, 2018.
Läkemedelsbehandling vid kognitiv sjukdom
Forskningen går framåt och det finns flera lovande behandlingsstrategier, men i nuläget finns ingen botande behandling för någon kognitiv sjukdom. Oavsett bakomliggande kognitiv sjukdom är demens en obotligt fortskridande funktionsnedsättning som förr eller senare leder till döden.
I dag används tre läkemedel vid mild till måttlig Alzheimers sjukdom samt Lewykroppssjukdom: donepezil, rivastigmin (Exelon) och galantamin (Reminyl). Alla är kolinesterashämmare. Acetylkolin är ett viktigt signalämne i hjärnan som bryts ned av ämnet kolinesteras. Dessa tre läkemedel hämmar nedbrytningen så att mer acetylkolin kan användas i signaleringen och kontakten mellan nervceller, och då fungerar nervcellerna så bra som möjligt. Däremot påverkar de inte själva sjukdomsprocessen. Vid svårare kognitiv svikt kan memantin (Ebixa) användas. Det är också ett symtomlindrande läkemedel som med fördel kombineras med acetylkolinesterashämmare, i synnerhet vid Lewykroppssjukdom eftersom det visat mycket god effekt. Läkemedlet påverkar nervcellernas funktion genom ämnet glutamat vars funktion är att ”städa” i synapsen.
Studier på kolinesterashämmare och memantin har kunnat påvisa förbättringar i kognitiva funktioner, beteende och förmåga att klara dagliga aktiviteter. I en studie (SATS-studien) från 2014 påvisades att patienter som svarade bra på behandling med kolinesterashämmare levde längre. Patienter med 6 månaders positiv effekt av behandling uppvisade i genomsnitt en lika lång ökning av livslängden. Utifrån dagens kunskap verkar inte läkemedelsbehandling ha någon effekt på hur länge patienterna vårdas på särskilt boende. Den tidigare observerade förlängda livslängden verkar gälla patienter som svarat bra på behandling med kolinesterashämmare.
Vid vaskulär sjukdom eller frontotemporal sjukdom finns ingen evidens för behandling med kolinesterashämmare eller memantin. Vid vaskulär sjukdom behandlas kända riskfaktorer för hjärt- och kärlsjukdom enligt vårdprogram (exempelvis diabetes och stroke).
Symtomlindrande läkemedelsbehandling kan påbörjas oavsett ålder. Eftersom effekterna är begränsade bör de sättas in i ett lugnt skede för att underlätta utvärdering. Men även i ett sent stadium av sjukdomarna kan patienten ha nytta av behandling. Läkemedelsbehandling kan också prövas vid blandformer av Alzheimers sjukdom och vaskulär sjukdom eftersom den individuella effekten kan vara betydande.
Avsluta behandling
Generellt bör behandling med kolinesterashämmare och/eller memantin fortgå så länge patienten kan interagera med sina närstående och vårdare, och har viss ADL-funktion så att hen t.ex. kan äta själv, sköta sin personliga hygien eller förflytta sig själv. Den stora vinsten med läkemedelsbehandling är minskade kognitiva symtom och att man i bästa fall kan skjuta upp behovet av särskilt boende. Utifrån klinisk erfarenhet kan det dock ibland vara värt att pröva exempelvis memantin även för patienter på särskilt boende, vid uttalade beteendemässiga och psykiska symtom.
Vid tveksamhet om effekten av läkemedelsbehandlingen kan man göra ett utsättningsförsök och utvärdera effekten efter 2–4 veckor. Vid försämring bör man överväga att återinsätta behandlingen. Beredskap bör finnas för återgång till fulldos vid en snabb eller tydlig försämring som i vissa fall kan komma redan inom några dagar (i form av försämrade kognitiva funktioner, försämrad ADL-förmåga eller tilltagande BPSD).
Man bör undvika utsättning i nära anslutning till större förändringar i patientens tillvaro, till exempel en flytt till särskilt boende, eftersom flytten i sig innebär en konfusionsrisk och det då är svårt att värdera orsaken till försämringen. Dosminskning kan övervägas vid misstanke om biverkningar. Det gäller att i dialog med de närstående känna in rätt tidpunkt för utsättning av symtomatisk behandling.
Vid tydlig försämring eller icke tolererbara biverkningar bör behandlingen avslutas. Nedtrappning behövs inte. I november 2024 lanserades ett nytt kapitel om kognitiv sjukdom i Läkemedelsboken, och det kan användas som referens och kunskapskälla. Se lakemedelsboken.se/terapiomraden/geriatrik/ kognitiv-sjukdom/.
Ytterligare några länkar som kan vara användbara i vården av patienter med kognitiva sjukdomar:
Goda läkemedelsråd för sköra äldre 2025 (pdf), publicerad på sidan Skånelistan med Bakgrundsmaterial (vardgivare.skane.se).
Hjärtsjukdomar
Utmärkande för hjärtsjukdomar, särskilt hjärtsvikt, är det svängande förloppet och svårigheter i prognostisering. För att bättre möta patientens ofta komplexa behov är det viktigt att identifiera palliativa vårdbehov hos patienten redan då sjukdomen påverkar det dagliga livet. Att identifiera en brytpunkt är svårt och ofta fruktlöst. Viktigare är i stället att erbjuda patient och närstående ”samtal vid allvarlig sjukdom” tidigt och upprepat för att fånga symtom och efterhöra patientens önskemål. Den medicinska behandlingen av hjärtsvikt är en del också av symtomlindringen och bör försiktigt anpassas över tid 12357. Det kan behövas när patienten trots optimal behandling har svår hjärtsvikt NYHA IIIb eller IV, eller refraktär angina CCS IV 358 359 360, om patienten har upprepade behov av sjukhusvård, får dålig effekt av behandling eller upplever successivt försämrad livskvalitet.
Förutom de klassiska symtomen andnöd, trötthet och ödem, lider många patienter med hjärtsjukdom av smärta, ångest och illamående 361. Principerna för behandling av sådana besvär är desamma som i annan palliativ vård och berörs därför inte här.
Hjärtsvikt
Hjärtsvikt är ett vanligt sjukdomstillstånd, och allvarligare grader av hjärtsvikt, NYHA III–IV, innebär en kort förväntad överlevad. Därför är det viktigt att identifiera palliativa vårdbehov hos patienter med hjärtsvikt tidigare än vad som är vanligt i vården idag.
Ämnet hjärtsvikt behandlas i ett separat vårdförlopp, med en bilaga om palliativ vård vid hjärtsvikt. Här hittar du Bilaga F Palliativ vård vid hjärtsvikt. Den är ett komplement till vårdförloppen kronisk hjärtsvikt och palliativ vård, som innehåller en mer utförlig beskrivning av olika nyckelbegrepp och definitioner samt rekommendationer kring symtombehandling.
Dyspné vid hjärtsvikt
Dyspné är ett vanligt symtom som oftast behandlas med diuretika. Diuretika är dock ett läkemedel mot övervätskning och i vissa fall beror dyspnén på detta, men många hjärtsviktspatienter har också kroniskt obstruktiv lungsjukdom, KOL. Man bör därför försöka att bedöma graden av vätskeretention innan man behandlar dyspné med diuretika, för att undvika att patienten blir för hårt behandlad med försämrad njurfunktion som följd.
Opioder har den specifika effekten att lindra andnöd, troligen via opioidreceptorer i lungorna, och ofta räcker betydlig lägre doser än vad som krävs för smärtlindring. Dyspné är ett dynamiskt symtom som behöver små doser opiod att ta vid behov, eftersom hög dos långverkande opioid kan orsaka sedering och illamående. Opioider har visad effekt i det sena skedet av hjärt och lungsvikt med dyspné. Uppegående, något piggare patienter med en framför allt ansträngningsutlöst dyspné har en betydligt sämre hjälp av opioid. Vätskeretention förutsätter att man först måste få i sig vätska för att sedan retinera den. I livets absoluta slutskede slutar nästan alla patienter att dricka och behovet av diuretika kommer då också att minska.
Smärta vid hjärtsvikt
Smärta förekommer i hög grad hos hjärtsviktspatienter med palliativa vårdbehov men förbises ofta eftersom det sällan är det sviktande hjärtat som gör ont utan snarare konsekvenserna av det. Man bör därför se till helheten och fråga efter smärtor i svullna ben, gikt, trycksår på grund av långvarig immobilisering med mera. NSAID-preparat bör undvikas på grund av risk för försämrad njurfunktion, särskilt i närvaro av RAAS-blockad. Effekten av morfinpreparat är välkänd och väldokumenterad i livets slutskede, och sådana bör inte undanhållas hjärtsviktspatienter. Man bör dock i första hand välja oxikodon framför morfin eftersom den förra inte är lika beroende av njurfunktionen för sin elimination.
Depression vid hjärtsvikt
Cirka 20–30 % av patienterna med svår hjärtsvikt lider av depression enligt klinisk erfarenhet. Ju svårare hjärtsvikt, desto större risk för depression, samtidigt som svår depression innebär ökad risk för sjukhusinläggningar och vårdbehov. Grunden för att behandla depression i livets slutskede är god kontroll av övriga hjärtsviktssymtom och psykosocialt stöd till patient och närstående.
Pacemakerbehandling
ICD-behandling förebygger plötslig arytmidöd, till priset av risken för obehagliga elchocker. Risken kontra nyttan med fortsatt ICD-behandling bör därför kontinuerligt värderas och diskuteras med patienten när man börjar närma sig livets slutskede. I livets slutskede finns det risk för upprepade och meningslösa chocker och då bör patientens ICD stängas av. I dagsläget gör man inte alltid det. Rutiner och resurser för ICD-avstängning, även i hemmet, bör därför finnas på alla centrum som ansvarar för ICD-behandling. Bradykardipacemaker liksom resynkroniseringsbehandling (CRT) ger inga biverkningar, men det finns stor risk för svåra symtom om de stängs av och de bör därför kvarstå livet ut. Ur Bilaga F – Palliativ vård vid hjärtsvikt version 1.0.
Angina pectoris (kärlkramp)
Patienter med svår angina pectoris bör behandlas med nitroglycerin och morfin. Nitroglycerin som spray eller i långverkande beredning kan också ges vid svår andnöd och samtidig hjärtsvikt för att sänka fyllnadstrycket – om systemblodtrycket är acceptabelt (> 95–100 mm Hg). Patienter med svårbehandlad (refraktär) isolerad angina pectoris behöver symtomlindring, men prognosen är inte lika dålig som för patienter med svår hjärtsvikt i NYHA IIIB/IV. Dessa patienter bör erbjudas kontakt med en specialiserad palliativ enhet. Patienter med refraktär angina pectoris kan vara aktuella för TENS-behandling, EECP (extern pumpbehandling) eller SCS (Spinal Cord Stimulator) alternativt ESES (Epidural Spinal Electrical Stimulation – ryggmärgsstimulering) för att om möjligt lindra symtomen. Även dessa behandlingar gäller speciella patientgrupper som länge sköts i specialistvården. Patienter med angina pectoris kan ha stor nytta av bedömningar och råd från en fysioterapeut, till exempel om energibesparande förflyttningar och andningsinstruktioner.
Om man i samråd med patienten och de närstående beslutat att avstå från återupplivningsförsök i händelse av försämring behöver patienter med svår ischemisk hjärtsjukdom inte hjärtövervakning eller övervakning på en avdelning för hjärtintensivvård. Det symtomlindrande behovet bör då styra valet av vårdenhet.
Kroniskt obstruktiv lungsjukdom, KOL
Det vårdteam som ansvarar för vård av patienter med KOL bör ha nära samarbete med hemsjukvården, för att gemensamt och gradvis introducera palliativ vård med möjlighet till vård i hemmet när sjukdomen påtagligt begränsar patientens aktivitetsnivå och ger återkommande behov av akut vård.
Vårdteamen bör gemensamt förbereda medicinska åtgärder vid försämringshändelser genom färdiga läkemedelsordinationer. Dessa ska vara kända för patienten.
Symtomlindring vid KOL överensstämmer med grundprinciperna i all palliativ vård. Patientundervisning, träning och hjälpmedel kompletterar omvårdnad och läkemedelsbehandling.
Ett specialiserat palliativt team kan i sent sjukdomsskede kopplas in om symtombilden blir mer komplex, till exempel om patienten visar tecken på respiratorisk svikt och om symtomen är svåra att lindra.
KOL i framskridet stadium, med eller utan respiratorisk svikt, andnöd vid allt mindre ansträngning ger därmed allt större begränsningar i vardagen 362. Med andnöden kommer också ångest som kan leda till isolering, inaktivitet och relationsproblem under lång tid. Allt svårare exacerbationer (akut försämrad andning som kräver intensifierad behandling) ökar risken och rädslan för att dö 363.
På individnivå kan förloppet vara svårt att förutse, och därmed också prognosen. Några patienter har ett långsamt, jämnt försämringsförlopp medan andra pendlar och försämras ojämnt mellan exacerbationerna. Prognosen är därför svårförutsägbar, så samtal om vårdinnehållet och patienternas önskan,dvs.”samtal vid allvarlig sjukdom” bör föras tidigt och vid upprepade tillfällen. Vårdplanen behöver fortlöpande omprövas och uppdateras. För patienter med KOL i sent skede kan behoven av palliativa vårdinsatser likna de som förekommer vid till exempel lungcancer.
Slutskedet av KOL
Det finns ett antal faktorer som talar för att en patient med KOL är i sent skede av sin sjukdom och att förbättring inte längre är möjlig. Dessa faktorer är:
- en allt mer uttalad och irreversibel lungfunktionsnedsättning
- stigande koldioxidvärde (analys av blodgas tagen i vila)
- kakexi (ofrivillig viktnedgång)
- sekundär hjärtsvikt
- vilotakykardi
- tilltagande andfåddhet och trötthet redan vid mycket lätt ansträngning eller i vila.
- oförmåga att ta sig utanför bostaden
- depression
- tidig morgonångest.
Palliativ vård ger bättre symtomkontroll och livskvalitet och bör initieras när sjukdomen påverkar vardagen påtagligt, med allt tätare exacerbationer och vid andnöd och ångest 360.
Inhalationsbehandling och fysioterapeutiska insatser för att förbättra andning samt slemmobilisering ska fortgå livet ut i anpassade former som stabiliserande och symtomlindrande behandling. Fysioterapeuter kan också utvärdera och instruera patienter i inhalationsteknik. Tekniken kan behöva anpassas till förändrat sjukdomsstatus. Med förebyggande och tidiga interventioner vid exacerbationer går det att minska risken för plågsamma symtom och sjukhusvård 365. Antibiotikabehandling kan med fördel förberedas så att patienten får inhalationsbehandling samt antibiotika i tablettform så tidigt under exacerbationen som möjligt. Rekommenderad standardbehandling är amoxicillin (Amimox 750 mg x 3 i 5–7 dagar) eller doxycyklin (Doxyferm 100 mg 2 x 1 i 3 dagar) 366, men om det inte fungerar kan antibiotikabehandlingen i hemmet genomföras med läkemedel för intravenöst bruk, t.ex. ceftriaxon som ges som injektion en gång per dygn eller Cefotaxim iv i två eller tredos. Behandling med perorala steroider kan också förberedas i hemmet. Ofta gäller det prednisolon 10 mg 3–5 tabletter dagligen i nedtrappande schema, alternativt betemetason 0,5 mg 8–12 tabletter dagligen i nedtrappande schema över en period av 7–10 dagar.
Hypoxi och höga koldioxidvärden i tidigt palliativt skede kan indikera en dålig prognos. Hemventilator bör övervägas och funktion och behov av detta sedan utvärderas under sjukdomsförloppet 366. NIV behandling bör ske i samarbete med specialistklinik för att utvärdera indikation, effekt och anpassning av inställningar och apparatur. Vid uttalad hypoxi utan tecken till retention kan hemsyrgas övervägas som symtomlindring.
Stress är ett vanligt problem för patienter med KOL. Hjälpmedel och en god andningsteknik är viktiga för att lindra besvären, vilket motiverar nära samråd med arbetsterapeut och fysioterapeut. Informerande samtal har god effekt som stöd till KOL-patienternas psykologiska copingstrategier 367.
Symtomlindring
Symtomlindring ges enligt generella rekommendationer för KOL. En fysioterapeut bör medverka för att optimera patientens inhalationsteknik och lära ut energibesparande förflyttningar. Omvårdnaden bör planeras för att få ett lugnt tempo och fortlöpande dialog med patienten under alla vardagliga moment. Fokus bör vara på att patienten ska komma upp ur sängen eller stolen flera gånger varje dygn, med eller utan hjälp. Frisk luft och handfläkt lindrar andnöd 368. I palliativ vård har bronkdilaterande inhalationer ibland dålig effekt på grund av att patienten inte orkar genomföra behandlingen. Hjälp med inhalationsteknik kan vara av värde vid försämring och försvagad andning. Förmår patienten inte inhalera korrekt och effektivt längre kan terbutalin provas i form av subkutan injektion. Detta kan bli aktuellt i sent skede av sjukdomen. Opioider såsom morfin i tablett- eller injektionsform blir i allmänhet aktuell som symtomlindring vid svår dyspné. Se även avsnitt 15.2 Andningsbesvär. Anpassad nutrition med fokus på energität föda förbättrar ofta patientens ork och livskvalitet. Överväg till exempel näringsdrycker eller annan energiförstärkning. Koldioxidretention ger sänkt medvetande som sedan övergår i medvetslöshet utan mekaniska kvävningssymtom.
Neurologiska sjukdomar
Behovet av palliativ vård för patienter med neurologiska sjukdomar har inte uppmärksammats i samma utsträckning som för patienter med andra sjukdomar, främst cancer. I dag har de flesta neurologiska patienter inte tillgång till palliativ vård som är skräddarsydd för deras specifika behov 369, men denna patientgrupp uppmärksammas nu mer. För att lyfta fram det som särskiljer de neurologiska sjukdomarna är de neurologiska tillstånden i detta avsnitt indelade i två olika huvudtyper beroende på sjukdomsförlopp, nämligen progredierande neurologiska sjukdomar och stroke.
Patienter med primära hjärntumörer, högmaligna gliom i synnerhet och patienter med cerebrala metastaser har oftast snabb sjukdomsprogress, kort förväntad livslängd och massiv symtombild i livets slutskede, och de behöver därmed ofta hela det palliativa teamets kompetens – ibland nästan direkt efter diagnostillfället. Patienten kan få fokalneurologiska bortfall och kognitiv påverkan, sekundärt till tumörens lokalisation, och i slutskedet är det vanligt med generell hjärnpåverkan med dysfagi (sväljningssvårigheter), dåsighet, huvudvärk, kramper, agitation,konfusion delirium och rosslingar 370. Se vidare nationellt vårdprogram för CNS-tumörer.
Progredierande neurologiska sjukdomar
Många patienter får tidigt kommunikationssvårigheter och kognitiv påverkan. Det är viktigt att tidigt i förloppet ha en dialog om prognos, planering och efterfråga patientens önskemål.
Andning och nutrition påverkas ofta, och andningshjälpmedel och nutritionshjälpmedel (PEG) bör också diskuteras tidigt i förloppet med patienten.
Depression är ett vanligt symtom som ska uppmärksammas.
Specifika aspekter på välbefinnande
Patienter med kroniska neurologiska sjukdomar förlorar förmågan att t.ex. gå, använda händer och armar, kommunicera och svälja. Ibland drabbas även kognitionen. Detta leder till successiva inskränkningar av livsföringen, och många får upprepade kriser. Patienterna behöver professionellt stöd under hela förloppet, och vårdkedjan bör skräddarsys från diagnostillfället och fram tills döden inträffar. Turner-Stokes et al. 371 föreslår samarbete mellan neurologi, rehabiliteringsmedicin och palliativ vård. Det är viktigt att utreda patientens förmåga att kommunicera och klara ADL för att tidigt kunna sätta in stödjande insatser. Med rätt anpassning, hjälpmedel och personligt stöd kan patienten ofta kommunicera och utföra vissa vardagliga aktiviteter trots omfattande funktionsnedsättningar.
Den tilltagande förlusten av autonomi och det ökade behovet av hjälp med ADL kan göra att patienten känner sig som en belastning för de närstående, utan eget värde. Hopplöshetskänslor är vanliga, och både suicidtankar och suicid är överrepresenterade bland patienter med kroniska neurologiska sjukdomar såsom ALS, MS och Parkinsons sjukdom. Lewis et al. 372 har identifierat tre nyckelfaktorer för suicidrisk: känsla av hopplöshet, depression och social isolering. Depression är också vanligt förekommande hos patienter med neurologisk sjukdom.
En del patienter drabbas av förvirring som kan vara mycket svårbehandlad. Många får kommunikationssvårigheter, med eller utan kognitiv påverkan, så eventuella framtida vårdbegränsningar ska helst diskuteras med patienten relativt tidigt i förloppet, när hen fortfarande är kapabel att ta till sig information och förmedla sina tankar och önskemål. Samtidigt kan patienten vara i akut kris på grund av diagnosbeskedet. Det är en avvägning hur man bäst balanserar delaktighet med respekt för patientens känslor och förmåga att delta.
I sjukdomens senare skede kan det vara mycket svårt att bedöma patientens symtom, till exempel smärta eller ångest, och därmed svårt att utvärdera effekten av den palliativa behandlingen 373. Detta ställer större krav på vårdgivarens och de närståendes förmåga att tolka signaler.
Vissa patienter med till exempel Huntingtons sjukdom eller ALS med frontallobsdemens får beteendestörningar som innebär apati, social isolering och nedsatt exekutiv funktionsförmåga. Dessa beteendeförändringar kan vara utomordentligt svåra att hantera för både närstående och vårdgivare.
En del patienter med sväljningssvårigheter kan drabbas av upprepade kvävningstillbud, vanligen efter att ha svalt fel. Utöver upprepade bedömningar och behandlingsråd från en logoped kan slemlösande och salivminskande behandlingar ibland ge viss lindring. Återkommande aspirationer är vanliga och lunginflammation är en frekvent dödsorsak. I möjligaste mån bör man fortsätta att ge patienterna smakportioner för både lustens och munslemhinnans skull. Noggrann munvård är minst lika viktig för de patienter som inte längre försörjer sig via munnen som för övriga patienter 54.
En del patienter drabbas av svår och plågsam förstoppning som ibland kan leda till att man anlägger en stomi.
Många patienter drabbas av svårbehandlad smärta av multifaktoriell orsak. Spasticitet kan också vara smärtsam och försvåra den vardagliga skötseln. Spasticitet kan behandlas med läkemedel, gärna i kombination med rörelsebehandling och råd från en fysioterapeut.
Andningssvikt med koldioxidretention i livets slutskede är den vanligaste dödsorsaken för patienter med neuromuskulär påverkan.
Indikation för PEG vid neurologiska sjukdomar
Indikationen för perkutan endoskopisk gastrostomi (PEG) är att oralt näringsintag inte fungerar på grund av sväljningssvårigheter av olika grad. Sväljningsvårigheter är vanligt förekommande hos patienter med kroniska neurologiska sjukdomar. Tidiga diskussioner är viktiga för att patienten tillsammans med läkaren ska kunna ta ställning till framtida behandlingsmöjligheter, inklusive nutritionsstöd och PEG. Vårdbegränsningar bör också diskuteras i detta skede liksom patientens preferenser. Om patienten önskar nutritionsstöd bör adekvat nutrition säkras innan patienten når slutskedet av sjukdomen om det är möjligt. För vissa räcker det med konsistensanpassad kost och näringsdrycker, medan andra behöver PEG eller motsvarande.
Patienten behöver vara i så gott och stabilt skick att hen klarar att medverka vid och förstå innebörden av inläggning av PEG om åtgärden ska kunna genomföras. I vissa fall anläggs PEG med metod som kräver sövning. I andra fall kan PEG anläggas radiologiskt utan mer omfattande sedering. För vissa patienter med neurologisk sjukdom innebär PEG-inläggning en oacceptabelt stor risk för aspirationskomplikationer pga. komplicerande faktorer. Faktorer att också väga in är trötthet, generell svaghet och kognitiv påverkan. Det är ytterst den medicinska bedömningen där möjlig nytta och troliga risker avvägs som avgör om åtgärden kan genomföras och innebära en symtomlindring. Med tidig insättning kan den livskvalitetshöjande och fysiologiska nyttan maximeras, samtidigt som riskerna med ingreppet minskar. I samband med PEG-insättning bör man också diskutera hur och när en nutritionsbehandling ska avslutas i sent palliativt skede.
Motorneuronsjukdomar
Vid motorneuronsjukdomar drabbas framför allt motorneuronen, vilket ger tilltagande muskelsvaghet. Den vanligaste är amyotrofisk lateral skleros (ALS). Medelöverlevnaden vid ALS är tre år efter debut av symtom. Det finns också motorneuronsjukdomar med långsammare progress. Gemensamt för dem är att patienten utvecklar andningssvikt på grund av allt svagare andningsmuskulatur. Många patienter får möjlighet att pröva icke-invasiv ventilator (NIV) när andningssvikten blir symptomgivande. I Sverige är det relativt ovanligt med invasiv ventilator (respiratorbehandling) vid motorneuronsjukdom.
Många patienter får också sväljningssvårigheter och kan ha nytta av PEG 374. Samtal och beslut om PEG är ofta komplexa.
Patienter med motorneuronsjukdom bör skötas i nära samverkan mellan neurolog och någon med palliativ specialistkompetens, och gärna i kontakt med ett multidisciplinärt palliativt team som har erfarenhet av dessa sjukdomar. Kontakten bör etableras tidigt i sjukdomsförloppet, eftersom många patienter senare får svårt att redogöra för sina önskemål. Hur tidigt i förloppet detta är lämpligt måste bedömas från person till person Många vill vårdas i hemmet tills de dör, och därför behövs tidigt en plan för att avveckla nutritionsstöd och andningsstöd i sent palliativt skede. Det är lika viktigt som att erbjuda och sätta in stöd för nutrition och andning.
Många patienter med motorneuronsjukdomar är förlamade i både armar och ben och har uttalade muskelatrofier. En del har problem med muskelkramper och spasticitet, vilket kan bli mycket smärtsamt och kräver behandling. Många har vidare tal- och sväljningssvårigheter, delvis beroende på svag mun- och svalgmuskulatur, men även som en del av andningsproblemet. Det kan finnas risk för aspiration av maginnehåll och därmed utveckling av lunginflammation. Patienterna kan då få en uttalad andningspåverkan. Annars brukar andningsbesvären öka långsamt och inte bli akuta, förutom i samband med en slempropp. Patienter med spinal start (i extremiteter) använder också gärna NIV, men för patienter med huvudsakligen tidiga bulbära symtom (svaghet runt mun och svalg) kan NIV vara svårt att använda eftersom masken läcker mycket runt den försvagade munnen. Det är heller inte ovanligt att patienten inte vill använda sin NIV även om den underlättar andningen.
Patienten kan ha problem med slemproduktion, oro och ångest, och då behövs lindring med opioider, sedativa och antikolinergika 375 376. Slemproblemet kan lindras effektivt med en så kallad hostmaskin, vilket i sin tur minskar ångesten av kvävningskänslan som uppstår pga. slemsamling i luftrören. Det kan vara gynnsamt att använda maskinen flera gånger om dagen, även i förebyggande syfte. Om patienten har smärta och andnöd, men inte slemproblem, ges morfin. Vid mer uttalad oro och ångest kan man pröva bensodiazepiner eller neuroleptika. Ofta är patienten tydligt påverkad och trött av koldioxidretentionen, och glider in i ett komatöst tillstånd. De flesta patienter dör lugnt och stilla 375. En andel av patienter med ALS utvecklar en påverkad kognition. Tidigt i förloppet bör en företrädare för patienten utses.
Se vidare Vårdförloppet för ALS.
Muskelsjukdomar
Vid muskelsjukdomar är det funktionen i själva muskeln som avtar. Det finns många ärftliga muskelsjukdomar som gör att patienterna dör i barnaåren, men i och med ett bättre omhändertagande kan nu vissa grupper leva upp till vuxen ålder. En sådan sjukdom är Duchennes muskeldystrofi som är könsbundet recessiv. Många av dessa sjukdomar påverkar också andra organsystem inklusive hjärtmuskulatur och hjärnan (kognition). Icke ärftliga muskelsjukdomar är delvis behandlingsbara och en liten andel patienter utvecklar svår andningssvikt.
Vissa patienter utvecklar en kardiomyopati som ger hjärtsvikt. Andningen är också nedsatt på grund av påverkan på andningsmuskulaturen eller en ren restriktiv lungfunktionsnedsättning som orsakas av torakal skolios, och patienterna har generellt mycket uttalad muskelatrofi med uttalad svaghet. Omhändertagandet blir detsamma som vid motorneuronsjukdomar. Det finns inga kontrollerade studier av behandling i sjukdomens sena sjukdomsförlopp.
Parkinsons sjukdom och atypisk parkinsonism
Parkinsons sjukdom (PD) är den näst vanligaste neurodegenerativa sjukdomen, efter Alzheimers sjukdom. Patienter med PD har ökad förekomst av självmordstankar medan suicidförekomsten inte är ökad, möjligen på grund av att patienterna inte förmår begå självmord på grund av nedsatt psykomotorisk funktion och/eller apati 377.
En stor andel av patienterna med PD utvecklar kognitiva nedsättningar inklusive demens 378. Eventuella vårdbegränsningar måste diskuteras när patienten fortfarande är kapabel att ta till sig information och förmedla sina tankar och önskemål. Avancerade behandlingar såsom duodopa och Deep Brain Stimulation (DBS) kan sättas in vid behandlingssvikt, men bör undvikas om patienten är i slutet av sjukdomsförloppet. Många patienter får svårt att svälja i livets slutskede, vilket påverkar både nutrition och medicinering. Den vanligaste dödsorsaken bland PD-patienter är aspirationspneumoni 379 380.
Den tydligt palliativa fasen av PD kan pågå i flera år och kännetecknas främst av minskat svar på den dopaminerga behandlingen och av kognitiv försämring. Patienterna drabbas ofta av visuella hallucinationer, återkommande fall, demens och tilltagande beroende av hjälp med ADL. Patienterna fluktuerar i sin motorik, svarar sämre på behandlingen och är samtidigt känsligare för biverkningar 380. Det är viktigt att försiktigt trappa ner den dopaminerga behandlingen, eftersom ett tvärt avslut kan medföra svåra utsättningssymtom. Om patienten inte kan svälja kan man överväga dopaminerga plåster eller i undantagsfall sond. Terminala plågsamma och svårbehandlade symtom är svår tremor, svår bradykinesi och agiterad förvirring med eller utan hallucinationer.
Multipel systematrofi, progressiv supranukleär pares och kortikobasalt syndrom är sällsynta parkinsonliknande sjukdomar (atypisk parkinsonism, ”Parkinson plus”). De degenerativa symtomen är då mer omfattande, och behandling med L-dopa inte är lika framgångsrik som vid PD. Dessa sjukdomar har en allvarlig prognos och en svårlindrad symtombild. Vårdbehovet i sen sjukdoms fas är lika komplext som i den palliativa vården av patienter med motorneuronsjukdom.
Multipel skleros (MS)
MS i framskridet stadium medför svåra fysiska och psykiska symtom 381. Den kognitiva förmågan försämras i någon grad hos cirka hälften av alla personer med MS, men en mindre andel kan behöva en företrädare. Detta behov bör tillgodoses innan patienten förlorar förmågan att själv fatta och kommunicera beslut 382.
Personer med MS har i sent sjukdomsskede ofta symtom såsom fatigue, smärta, svår spasticitet och depression. Dysfagi och dysartri är också vanligt förekommande.
Spasticitet kan få svåra följder såsom nersatt rörlighet, smärta, kontrakturer, blås- och tarmdysfunktion och trycksår 382. Flexionskramper kan vara extremt smärtsamma. Det behövs aktiv behandling med både fysikaliska åtgärder och läkemedel för att förhindra fibrotiska muskler, kontrakta leder, svår smärta och dekubitussår 382.
Många patienter upplever en förändrad ytlig känsel snarare än en förlorad känsel. Andra beskriver dysestesi (obehag vid beröring) eller restless legs 382. I olika sammanställningar anges också att 30–80 % lider av smärta. Svår smärta vid MS anses vara en av de svåraste utmaningarna att komma till rätta med. Den är oftast lokaliserad till fötter och ben, och kräver noggrann analys och en behandlingsplan. Utredningen måste utesluta andra orsaker till smärtan såsom förändringar i skelettet, besvär från buken, urinvägsinfektion, blåsstenar och baklofenpumpsdysfunktion. Fysioterapi minskar risken för kontrakturer. Baklofen peroralt och intratekalt reducerar spasticiteten. Injektion av botulinumtoxin i adduktorerna kan minska ömheten i deras muskelfästen, medan injektion i iliopsoas-musklerna kan eliminera eller lindra de smärtsamma flexionskramperna. Analgetika -NSAID eller opioider - har nästan aldrig någon effekt på neurogen smärta. Gabapentin eller amitryptilin i första hand och pregabalin i andra hand ger ibland viss lindring.
Diazepam till natten minskar spasticiteten samtidigt som det ger viss ro till patienten och underlättar insomnandet.
En del patienter med progressiv MS och hjärnstamsdysfunktion har svårt att svälja. Vid mer uttalade svårigheter bör PEG övervägas och diskuteras med patient och närstående om patienten medger. Nasogastrisk sond kan vara en kortsiktig lösning i väntan på PEG 382.Behandling med nasogastrisk sond är aldrig en långsiktig behandlingsform.
Många av dessa patienter vårdas på olika vårdboenden där primärvårdens läkare är ansvariga. Därmed behöver dessa läkare också neurologisk kompetens i dessa frågor.
Stroke, förekomst och prognos
Stroke kan leda till döden, direkt eller i ett senare skede.
Vid stroke är det ofta svårt att tidigt bedöma prognosen.
Målen för vården efter stroke behöver ofta omprövas kontinuerligt.
Intensiva vårdinsatser i akutskedet är ofta motiverade tills en säker prognostisk bedömning kan göras.
Stroke är den tredje vanligaste dödsorsaken i Sverige och är samlingsnamn på hjärninfarkt och hjärnblödning. Hjärninfarkt står för 85 % av fallen och hjärnblödningar för 15 %, varav subaraknoidala blödningar utgör 5 %. Sedan ett drygt decennium minskar antalet personer som insjuknar i stroke, trots att befolkningen ökar. Under den första veckan efter insjuknandet dör cirka 8 %, medan cirka 17 % dör inom 3 månader och cirka 23 % dör under första året. Andelen avlidna är högre efter en hjärnblödning, cirka 34 %, jämfört med cirka 14 % efter en hjärninfarkt 383.
Död till följd av stroke kan inträffa antingen som en konsekvens av det akuta insjuknandet, inom någon timme eller vecka, eller i ett senare skede. Dessa situationer beskrivs var för sig nedan.
Döende i akut sjukdomsskede efter stroke
Insjuknade i stroke sker väldigt plötsligt, vilket gör att patienten vanligen inte är förberedd och de närstående ofta blir väldigt chockade av det som inträffat. Vården av patienter med akut och omfattande stroke kännetecknas av komplexa och ibland omfattande insatser. Det är svårt att tidigt uppskatta prognosen för överlevnad och förväntade kvarstående funktionsnedsättningar på både kort och lång sikt. Ofta är det oklart om patienten är i livets slutskede eller inte 384. Behandlingsbeslut behöver därför omprövas kontinuerligt, ibland flera gånger varje dygn.
I det akuta skedet efter stroke är det ofta aktuellt med beslut om:
- kurativ behandling
- behandlingsbegränsningar
- behandling för att minska hjärnskadan
- vård med palliativ inriktning.
Vid akut insjuknande i stroke tar man först ställning till akutbehandling såsom reperfusion eller neurokirurgi i syfte att öka överlevnadschansen och förbättra prognosen. Initialt kan prognosen vara svår att bedöma och beslut om behandling fattas baserat på ett osäkert beslutsunderlag 385. Man bör också tidigt ta ställning till behandlingsbegränsningar, till exempel när det gäller HLR eller intensivvård, och ompröva beslutet kontinuerligt. Om en åtgärd inte bedöms gagna patienten ska man besluta om behandlingsbegränsning. Det första omhändertagandet riktas också mot att minimera hjärnskadan och därigenom skapa goda förutsättningar om patienten skulle överleva. I det ingår att optimera blodtryck, puls, syrgasmättnad, temperatur och blodsocker 308. Beslut om behandling för att minska hjärnskadan kan fattas oberoende av beslut om behandlingsbegränsningar såsom ingen HLR eller ingen intensivvård. Ett för tidigt beslut om att begränsa behandling kan leda till sämre prognos och ökad dödlighet, men faktorer såsom ålder och samsjuklighet väger också in. En del patienter bedöms ha irreversibel hjärnskada med betydande risk för allvarliga men, och sakna rimlig möjlighet till rehabilitering. De befinner sig därmed i livets slutskede och ska få symtomlindring och god omvårdnad.
Hjärnskadan utvecklas vanligen snabbt men kan förvärras under de första dygnen till följd av hjärnsvullnad. Efter denna tid är hjärnskadan fullt utvecklad och underlaget för prognos därmed säkrare. Komplikationer såsom urinvägsinfektion och pneumoni till följd av aspiration och sängläge samt feber är vanligt. Många har svårt att nutriera sig via munnen i det akuta skedet på grund av både sänkt vakenhet och dysfagi, dvs. svårighet att äta och svälja. Dysfagi kan vara övergående. Beslut om fullvärdigt nutritionsstöd kan behöva vänta tills prognosen är mer säker för att undvika en onödig påfrestning på kroppens organsystem för den livshotande sjuka patienten.
Många patienter som insjuknar med livshotande stroke har medvetandesänkning, kognitiv påverkan och begränsad förmåga att kommunicera. Detta innebär att de sällan kan uttrycka sin egen vilja och önskningar om vården eller delta aktivt i beslutsfattande 386.
De flesta har en viss förbättringspotential under lång tid, och utfallet kan bli bättre än vad som ursprungligen prognostiserats. En del kan också så småningom kan vara delaktiga i beslut om vårdnivå och vårdbegränsningar.
Närstående får ofta en viktig roll som förmedlare av information om personen och hens tidigare uttalade vilja och önskningar vid svår sjukdom 386. Målen för vården måste fortlöpande förankras hos de närstående, och en god dialog runt beslut för vården är nödvändigt 387. Närstående bör ges möjlighet att ta in situationen och prognosen innan några definitiva beslut fattas. Under denna tid bör förutsättningarna för en god överlevnad optimeras. Växlingen mellan liv och död kan vara plötslig och omvälvande. Till exempel kan en patient plötsligt vakna till efter några dagar utan vätsketillförsel, efter ett beslut om att avvakta med nutritionsstöd. Det omvända förekommer också, alltså att patienter med initialt god prognos snabbt försämras och dör hastigt 388.
Symtom och tecken vid döende i akut skede efter stroke
Patienter med svår eller livshotande stroke kan ha uttalat rosslig andning. God munvård och antikolinerga läkemedel kan underlätta. Sugning i nedre luftvägar bör undvikas eftersom det retar och kan ge upphov till ökad slembildning.
Hos medvetandesänkta patienter kan puls- och blodtrycksstegring, hög andningsfrekvens och motorisk oro vara tecken på smärta. I dessa fall bör man pröva analgetika i form av opioider subkutant eller intravenöst.
Intrakraniell tryckstegring kan ibland ge kraftig huvudvärk med oregelbunden andning, sänkt syresättning och sänkt medvetandegrad, med eller utan oro – så kallad inklämning som i förlängningen leder till hjärtarytmier och andningsstillestånd. Inklämning kan inte behandlas men huvudvärken ska lindras, förslagsvis med opioider.
Epileptiska krampanfall till följd av hjärnskadan kan också förekomma, följt av en lång postiktal fas (trötthet med förvirring). Patienten bör då få läkemedel för att bryta alternativt förebygga nya epileptiska anfall (midazolam alternativt levetiracetam). Anfall som går över av sig själv inom några minuter kräver ingen akut behandling.
I livets slutskede behövs ofta en kombination av analgetika (opioider) och sederande läkemedel i form av bensodiazepiner eller deras derivat (midazolam), varav de sistnämnda även ger ett krampskydd. Kontinuerlig infusion av läkemedel bör övervägas för jämnare effekt utan genombrott av symtom.
Döende till följd av stroke i senare skede
Patienter som överlever det akuta insjuknandet i svår eller livshotande stroke har ofta kvarstående nedsatt kognitiv förmåga. Förmågan att förstå och göra sig förstådd kan variera. Många kan ha svårt att nutriera sig beroende på sänkt vakenhet, svårighet att svälja (dysfagi), minskad aptit och kognitiva och motoriska funktionsnedsättningar samtidigt som livslusten kan avta 389. Dysfagi är det vanligaste symtomet vid livets slutskede efter stroke 389. Beslut om enteral nutrition via nasogastrisk sond eller PEG kompliceras av att patienten har svårt att uttrycka sin vilja och det är svårt att ge en säker prognos på längre sikt. Även här är det viktigt att ge tid för upprepade bedömningar av patienten, samt för närstående att förstå situationen. Nasogastrisk sond är ett gott alternativ för att initialt tillgodose nutrition utan att utsätta patienten för ett PEG-ingrepp. Om behovet av enteral nutrition bedöms vara mer långvarigt (> 4 veckor) rekommenderas PEG 390. Här bör dock patientens sammantagna hälsostatus vägas in, och för sköra patienter kan man avstå från att sätta PEG. För personer som har enteralt nutritionsstöd bör man också ha en dialog med patient och närstående om att minska eller avsluta nutrition i livets slutskede för att undvika onödig belastning på den döende kroppen.
Patienter med en allvarlig stroke i postakut och kroniskt skede har motsvarande vårdbehov som personer som dör till följd av andra kroniska sjukdomar eller ålderdom. Det är viktigt att tidigt ge vården en palliativ inriktning, innan livets slutskede inträtt. Man bör även ta ställning till och dokumentera eventuella vårdbegränsningar när det gäller livsuppehållande åtgärder. Detta gäller inte bara HLR utan även vård på intensivvårdsavdelning, vätska och nutrition, samt förebyggande åtgärder såsom trombosprofylax och behandling av livshotande komplikationer innefattande till exempel lunginflammation. För personer med svår stroke, som bor på särskilda boenden, bör man överväga ett förhandsbeslut om att patienten inte ska skickas till sjukhus vid en ny stroke eller annan allvarlig händelse.
Solida tumörsjukdomar
Cancersjukdomar är en heterogen grupp av sjukdomar med stor spridning vad gäller prognos och behandling.
Onkologiska vårdgivare bör ha god kompetens i palliativ medicin.
Patienter med cancer bör följas med regelbunden symtomskattning. Det bör finnas rutiner för att identifiera cancerpatienter som bedöms ha nytta av tidig kontakt med eller bedömning av en enhet med kompetens i specialiserad palliativ vård.
Det behövs mer samarbete mellan onkologiska behandlingsenheter och enheter med kompetens i palliativ medicin.
Vårdpersonal med palliativmedicinsk kompetens bör delta vid multidisciplinära onkologiska konferenser, särskild när diskussionen gäller patienter med komplexa palliativa vårdbehov och dålig prognos.
Aktuell utveckling inom onkologi som påverkar palliativ vård
Forskningen och utvecklingen inom onkologi har gjort stora framsteg och det finns flera nya behandlingsmöjligheter vid olika cancersjukdomar. Standardiserade vårdförlopp har också etablerats brett, med beskrivningar av processer och rutiner för primärutredning vid misstänkt cancersjukdom. Numera är det vanligt att behandlingsrekommendationer i både kurativt och palliativt syfte tas fram på multidisciplinära konferenser (MDK), oavsett om det gäller nydiagnostiserade fall eller återfall i cancersjukdom. Vid dessa konferenser efterfrågas regelbunden medverkan av specialister med kompetens inom palliativ medicin 391 men för de flesta cancerdiagnoser är detta inte rutin ännu.
Vårdförlopp
Samtidigt ökar insikten om att standardiserade vårdförlopp bör kombineras med individuella bedömningar som utgår från patientens egna önskemål, och att en standardiserad diagnostik och aktiv behandling bör undvikas för patienter som sannolikt inte får någon effekt av behandlingen. I kampanjen Kloka kliniska val, som Svensk Onkologisk förening tagit fram i samverkan med Svenska Läkaresällskapet, rekommenderas också att undvika cytostatikabehandling eller annan toxisk systemisk tumörbehandling för patienter som har avancerad tumörsjukdom och låg sannolikhet för meningsfullt livsförlängande eller livskvalitethöjande effekt (t.ex. WHO funktionsstatus 3–4). I stället är rådet att fokusera på symtomlindring och palliativt omhändertagande.
Antalet patienter som diagnostiseras med en ny cancer (incidens) ökar stadigt, liksom antalet som lever med en cancersjukdom (prevalens) 392. Cancersjukdomar är fortfarande bland de vanligaste dödsorsakerna i Sverige 393.
Utvecklingen inom en rad områden såsom kirurgi och antitumoral behandling med läkemedel och strålbehandling har lett till förlängd överlevnad även för patienter med metastaserad sjukdom och delvis mycket avancerad tumörbörda, som tidigare förväntades ha kort överlevnad 394. Oftast erbjuds patienten en kombination av olika behandlingar i en långsiktig multidisciplinär approach.
Cancersjukdomar är i dag en heterogen grupp av sjukdomar med stor variation när det gäller prognos och behandlingsalternativ. Metastaserad cancersjukdom är heller ingen enhetlig diagnos. Onkologer behöver i större utsträckning kommunicera det förväntade vårdförloppet och möjligheterna att fortsätta med en aktiv antitumoral behandling, men även eventuella begränsningar i livsuppehållande behandling utifrån patientens förutsättningar. Sjukvården har ett stort ansvar för att informera och ge stöd så att patienten och de närstående ska kunna vara delaktiga i bedömningen av fördelar och eventuella nackdelar med de föreslagna behandlingarna. Med detta stöd minskar risken för att överbehandla patienter, samtidigt som patienterna får realistiska förväntningar på vården och kan göra aktiva val i behandlingsbesluten. För de flesta cancersjukdomar finns situationer som inbjuder till dialog om den fortsatta behandlingens mål och inriktning (i engelskspråkiga länder förtydligas samtalets intention oftast med ”goals of care”): när sjukdomen bedöms vara obotlig, när progress eller toxicitet leder till att man omprövar valet av onkologisk behandling, när patienten inte längre bedöms ha nytta av aktiv antitumoral behandling och när patienten bedöms närma sig livets slutskede. Evidensbaserade riktlinjer har utvecklats för klinisk prognostisering 395och för att tillsammans med patienten väga potentiell nytta av behandling mot eventuell negativ påverkan på livskvaliteten 395.
Behandlingsstrategier
Detta vårdprogram fokuserar på allmänna principer för palliativ behandling av tumörsjukdomar. De olika cancervårdsprogrammen beskriver sjukdomsspecifika symtom som förekommer i palliativ sjukdomsförlopp, med förslag på lämpliga åtgärder. Ett nationellt vårdprogram om akut onkologi beskriver orsaker till komplikationer som kan drabba patienter under onkologisk behandling, och potentiella behandlingar av dem. Även det nationella vårdprogrammet för cancerrehabilitering ger värdefull information.
Funktionsstatus, nu ofta uttryckt i WHO PS/ECOG-skala, behandlingsrespons och begränsande biverkningar av antitumoral behandling är viktiga prognostiska faktorer i valet av fortsatt behandlingsstrategi. Initialt är det därför oftast oklart om patienten kan erbjudas potentiellt kurativa behandlingsstrategier eller inte 396. Även samsjuklighet, till exempel hjärt- och lungsjukdom, begränsar ofta möjligheterna till fortsatt intensiv onkologisk behandling. Se tabellen i avsnitt 12.1.3 Bedömningsinstrument vid identifiering av palliativa vårdbehov.
Integration av onkologisk och palliativ vård
För patienter under onkologisk behandling innebär regelbunden standardiserad symtomskattning bland annat högre livskvalitet och längre överlevnad 397 398. En stor andel patienterna avlider på sjukhus.
Data från Svenska palliativregistret visar överlag sämre utfall vad gäller vårdkvalitet för patienter som avlidit på sjukhus jämfört med de som avlidit inom kommunal och/eller specialiserad hemsjukvård, med reservation för lägre täckningsgrad för slutenvårdsenheter 59.
Cancerfondens rapport om palliativ vård 2024 399 och den uppdaterade versionen av cancerstrategin 400 belyser brister i den palliativa vården för cancerpatienter och ger förslag på konkreta åtgärder. Man betonar särskilt att palliativ vård inte enbart handlar om vård i livets slutskede utan bör implementeras tidig i patientens vårdförlopp. Det framgår också att cancerpatienter bör ha mer jämlik tillgång till både allmän och specialiserad palliativ vård. Dessutom lyfter man fram behovet av kompetens hos onkologiska vårdgivare men även väl etablerade rutiner för samverkan med vårdgivare inom den allmänna och specialiserad palliativa vården, för att tidigt kunna identifiera patienter med palliativa vårdbehov.
Uppföljning i allmän eller specialiserad palliativ vård övervägs oftast inte förrän man bedömer att aktiv antitumoral behandling inte längre är möjlig. Internationella riktlinjer har dock uppdaterats med rekommendationer om tidig integrerad palliativ vård utifrån evidens som visar fördelar med det 401. Ett antal studier belyser nämligen vinsten av att integrera onkologiska och palliativa vårdinsatser tidigare i vårdförloppet 402 403 404 405. För patienterna innebär det ökad livskvalitet, minskad symtombörda och ökad möjlighet att förstå sin prognos och uttrycka sina önskemål om vård i livets slutskede. Det är dock fortfarande osäkert huruvida tidig palliativ vård ökar den totala överlevnaden, och om alla symtom kan påverkas i ett tidigt skede. Studierna var inte helt konklusiva och studieuppläggen heterogena 406.
Enstaka studier har även visat att tidig anslutning till palliativ vård ökar vårdpersonalens 407 och de närståendes välmående 408 samt minskar kostnader för hälso- och sjukvården 409.
Enheter med kompetens i palliativ medicin och onkologiska behandlingsenheter behöver samarbeta på nya sätt, och följande förslag kan gynna detta samarbete:
- Bygg infrastruktur för palliativ vård (till exempel öppenvårdsmottagning och konsultteam till slutenvård och hemsjukvård).
- Låt kontaktsjuksköterskan vara en betydelsefull länk i samarbetet för patienter i tidigt sjukdomssjukdomsförlopp.
- Integrera den cancerspecifika vårdplanen (Min vårdplan) med vårdplaner för palliativa behov.
- Ge möjlighet att tidigt erbjuda patienter kontakt med specialiserat palliativt team när det behövs, även medan aktiv livsförlängande onkologisk behandling fortfarande pågår.
- Skapa system för kommunikation, samarbete och koordination mellan palliativ vård och onkologi.
- Ha regelbundna multidisciplinära diskussioner om gemensamma patienter.
- Gör regelbunden symtomscreening i onkologisk verksamhet. Det bör finnas rutiner för att identifiera cancerpatienter som bedöms ha nytta av tidig kontakt med eller bedömning av en enhet med kompetens i palliativ medicin. Se även Kapitel 11 Team inom palliativ vård.
Detta är exempelvis lämpligt för patienter med:
- otillräcklig symtomkontroll trots insatta åtgärder (Visuell analog skala, VAS > 3)
- komplexa symtom eller snabb sjukdomsprogress med förväntade komplexa symtom
- andra särskilda omständigheter såsom komplexa psykosociala behov
Ryggmärgskompressioner
Ryggmärgskompression (medullakompression) är en allvarlig komplikation hos patienter med cancer och drabbar främst dem med myelom eller skelettmetastaser av bröstcancer, prostatacancer, lungcancer eller njurcancer. Ungefär 5–10 % av alla cancerpatienter kommer att drabbas av ryggmärgskompression. Tidig diagnos och behandling kan höja patientens livskvalitet, minska smärta och öka fysiska funktion och oberoende 410 .
Symtom
Nytillkommen eller förvärrad smärta i nacken eller ryggen är det vanligaste symtomet vid ryggmärgskompression, och smärtan kan förvärras av hosta, ansträngning eller av sängliggande. Ofta förekommer också motorisk svaghet. Därtill upplever patienterna andra neurologiska symtom såsom känselbortfall, urinblåsepares och/eller sfinkterpares 410 (Nationellt vårdprogram Akut onkologi, Nationellt vårdprogram Prostatacancer).
Akut utredning och behandling
Vid misstanke om ryggmärgskompression ska patienten handläggas akut och ansvarig läkare, t.ex. onkolog eller hematolog, bör kontaktas omedelbart.
Högdos kortison ska ges vid neurologiska symtom med målet att minska motorisk och sensorisk påverkan. Initialt ges en dos betametason 16 mg x 2, sedan 16 mg x 1 dagligen i väntan på åtgärd. Kvarliggande kateter via urinröret (KAD) läggs vid behov eftersom ryggmärgskompression kan innebära blåstamponad pga. risk för urinblåsepares. Kortison kan kompletteras med omeprazol 20–40 mg x 1. Vid behov kontrolleras även blodsockernivå eftersom högdos kortison kan påverka diabetes eller utlösa en sekundär diabetes 410 (Nationellt vårdprogram Akut onkologi).
MRT helrygg (inte endast delar av ryggraden) ska göras akut eller senast inom 24 timmar, särskilt om patienten har sensoriska eller motoriska bortfallssymtom, eftersom chansen till framgångsrik behandling minskar vid fördröjning 410 (Nationellt vårdprogram Akut onkologi).
Fortsatt behandling
Hos patienter med en förväntad längre överlevnad är det viktigt att omedelbart kontakta behandlande läkare redan vid misstanke om ryggmärgskompression, för att diskutera behandlingsnivå och avgöra om det är aktuellt med kirurgi och/eller strålbehandling.
När personen närmar sig livets slutskede är det sällan indicerat med utredning, men kortison kan vara aktuellt som symtomlindrande behandling i kombination med övrig smärtlindring.
Länkar:
Nationellt vårdprogram Akut onkologi
Nationellt vårdprogram prostatacancer: se kapitel 14 Palliativ vård och insatser, avsnitt 14.4 Ryggmärgskompression.
Palliativ strålbehandling
Strålbehandling är ett bra alternativ vid symtomgivande cancerrelaterade tillstånd.
Det här avsnittet gäller främst patienter med avancerad cancersjukdom. För patientgrupper med gynnsam prognos och ytterligare behandlingsmöjligheter hänvisas till vårdprogrammen för respektive diagnos.
Praktiska synpunkter
Patienten måste kunna ta till sig information om hur behandlingen förbereds, planeras och genomförs. Hen måste kunna medverka och följa personalens instruktioner även när hen är ensam i behandlingsrummet. Vid förberedande strålbehandlingsdatortomografi och själva strålbehandlingen måste patienten kunna ligga stilla i 20–30 minuter, ibland längre, på en relativt hård brits. Det kan upplevas som obehagligt och smärtsamt. Rutinmässigt sövs eller sederas ej patienten för palliativ strålbehandling. Patienten behöver vara tillräckligt smärtlindrad före transport till en strålbehandlingsenhet.
Strålbehandlingen ska gagna patienten och det är viktigt med noggrann avvägning mellan nytta och biverkningar. Vid fel behandlingsindikation finns det risk för sämre livskvalitet och tidskrävande inneliggande vård 411.
Stålbehandlingseffekten kan dröja 2–4 veckor. Patientens förväntade livslängd är därför en viktig faktor och bör uppskattas till minst 2 månader för att palliativ strålbehandling ska kunna gagna patienten
För att bedöma vilka patienter som kan ha nytta av behandlingen har det gjorts försök med olika skattningsverktyg, till exempel WHO/ ECOG performance status, Comprehensive geriatric assessment (G8/CGA) 412, Recursive partitioning analysis (RPA) 413 och Clinical frailty score (CFS) 414. Resultaten har dock varit blandade.
För patienter med en dålig prognos och eller funktionsstatus större än 2 ska det finnas en stark behandlingsindikation, till exempel svårbehandlad smärta.
Kontakt och dialog med strålbehandlingsinriktad onkolog är värdefull inför ställningstagande till strålbehandling i palliativt skede.
Remissen till strålbehandlingsenheten bör innehålla information om diagnos, prognos, allmäntillstånd och skattad förväntad livslängd, patientens förmåga att medverka och symtomens debut, lokalisation och svårighetsgrad. Om patienten har en pågående onkologisk behandling kan den behöva pausas. Andra behandlingsalternativ kan bli aktuella, såsom avlastande kirurgi eller invasiva endoskopiska ingrepp.
Behandling
Antalet fraktioner och slutdosen avgörs individuellt, utifrån symtomens orsak och svårighetsgrad samt patientens allmäntillstånd och förväntade överlevnad.
Rekommendationen är att behandlingen ges utan fördröjning och på enklaste och minst tidskrävande sättet. Behandlingen kan ta 1 dag men också pågå i upp till 3 veckor.
Indikationer
I de flesta vårdprogram finns ett kapitel om palliativ strålbehandling. Sådan behandling kan exempelvis bli aktuell för patienter med
- smärta, exempelvis smärtsamma skelettmetastaser
- luftvägsobstruktion
- medullakompression
- blödningar
- tumörsår
- Kompression i vena cava superior
- passagehinder i esofagus
- hjärnmetastaser.
Onkogenetisk utredning
Vid spridd cancersjukdom kan både patienten och de anhöriga undra om tumörsjukdomen kan ha en ärftligt bakomliggande orsak. I första hand rekommenderas att patienter eller närstående, i samråd med ansvarigt tumörteam, vänder sig till den cancergenetiska mottagningen för mer information. Om patienten har kort förväntad tid kvar i livet kan man spara ett blodprov i blodbank (”banka”), för att underlätta en framtida cancergenetisk utredning. Detta görs enklast med ett blodprov på 5–10 ml i ett EDTA-rör med lila kork. Det behöver inte centrifugeras eller frysas. Remissen ställs till klinisk genetik för bankning av DNA.
Kontaktuppgifter till onkogenetiska mottagningar finns på cancercentrum.se.
Hematologiska maligniteter
Patienter med hematologisk malignitet får i lägre utsträckning än andra cancerpatienter tillgång till specialiserad palliativ vård, och dör oftare inom akutsjukvården 415 . Detta gäller även i Sverige enligt data från svenska palliativregistret 416, och även bland de allra äldsta.
Hematologiska maligniteter skiljer sig på flera sätt från solida tumörer, och innebär särskilda utmaningar och behov i fråga om palliativ vård. Tyvärr saknas särskilda riktlinjer för hematologiska patienter i de internationella palliativa riktlinjer som publicerats av EAPC, MASCC, ESMO och ASCO, även om specifika riktlinjer ibland tar upp patientgruppen. Ett exempel är ESMO:s riktlinjer för anemi och järnbrist hos cancerpatienter 391. Stora delar av riktlinjerna för palliativ vård vid cancer är givetvis också relevanta för hematologiska patienter, och behöver inte upprepas här. Detta avsnitt fokuserar på den särskilda hänsyn som kan behöva tas för patienter med hematologisk malignitet.
Olika typer av hematologisk malignitet
Hematologiska maligniteter är en heterogen grupp av sjukdomar med olika förlopp och behov. Shaulov et al. 417 ger en översikt över olika typer av hematologiska vårdförlopp och beskriver tre huvudtyper:
- ”The rollercoaster” är typiskt för akut leukemi och högmaligna lymfom. Sjukdomsförloppet kännetecknas av snabba svängningar i symtomintensitet. Det finns chans till bot men stor risk för toxicitet av behandlingar.
- ”The war of attrition” är typiskt för myelom och lågmaligna lymfom. Sjukdomarna är obotliga men innebär ofta långa symtomfria perioder. Det finns chans till påtaglig effekt av behandling även sent i sjukdomsförloppet.
- ”The transfusion tether” är typiskt för myelodysplastiska syndrom (MDS) och myelofibros. Sjukdomsbilden domineras av benmärgssvikt snarare än typiska cancersymtom, och lång tid med transfusionsberoende obotlig sjukdom.
Prognostisering
Prognosverktyg som utvecklats för solida tumörer är inte validerade för hematologiska maligniteter 418 och fungerar ofta dåligt för att identifiera patienter som närmar sig livets slutskede. Särskilt vid sjukdomstyper såsom akut leukemi och högmaligna lymfom kan patienterna ha en relativt god funktionsnivå kort tid innan döden inträder. För att patienterna ska få den önskade vården i livets slutskede, t.ex. få dö i hemmet, kan de behöva anslutas till specialiserad palliativ vård trots att det saknas typiska kriterier för anslutning såsom komplexa symtom 419. Det förutsätter dock en tydlig kommunikation mellan hematologisk klinik, palliativ vård och patienten och de närstående om vårdens mål och önskad vårdnivå vid försämring.
Benmärgssvikt och transfusionsbehov
Flera hematologiska maligniteter, särskilt MDS och akuta leukemier, präglas av benmärgssvikt. Beroende på sjukdomens aggressivitet kan patienterna leva med uttalat transfusionsbehov i flera års tid, ofta utan samtidiga tecken på avancerad sjukdom såsom kakexi eller sarkopeni. Det gör anemin till en potentiellt begränsande faktor för livskvalitet och aktivitetsnivå 420. Det är därför viktigt att transfusionsstrategi och Hb-mål anpassas till individen och regelbundet utvärderas för att möta patientens behov. I livets slutskede minskar i regel transfusionernas positiva effekt, vilket gör att de då i dialog med patienten bör fasas ut.
Trombocytopeni, sekundärt till behandling eller sjukdomsrelaterad benmärgssvikt, kan ge blödningar framför allt i slemhinnor och vara stressande och obehagligt för patienter och närstående. Akuta blödningar är en inte ovanlig dödsorsak vid refraktär akut leukemi 421. Transfusioner av trombocyter har en kortvarig effekt på grund av trombocyternas korta livslängd 422 men kan vara värdefullt i utvalda fall. Cyklokapron förebygger inte blödning vid trombocytopeni 423 men har en plats som akut behandling både lokalt och systemiskt.
Tidig integration av palliativ vård
Integration av palliativ vård i aktiv cancerbehandling är betydligt mer utbrett för patienter med solida tumörer än vid hematologisk malignitet. Ett par randomiserade studier av har dock visat att parallellt stöd av palliativa konsultteam ger påtaglig effekt på symtom, depression och ångest vid kurativt syftande vård för akut leukemi 424 och vid allogen stamcellstransplantation 425. I ASCO:s uppdaterade riktlinjer från 2024 rekommenderas därför att palliativ vård integreras tidigt i förloppet vid hematologisk malignitet 426.
Nyckeln till att erbjuda patienter med hematologiska maligniteter ett bra palliativt förhållningssätt redan tidigare i sjukdomsförloppet är ett gott samarbete mellan hematologen och enheter med palliativ kompetens.
Skörhet – tilltagande vårdbehov vid många sjukdomstillstånd
Patienter med ökad skörhet och svåra symtom ska identifieras inom alla vårdformer för att de ska få optimerad palliativ vård.
Skörhet betyder en minskad anpassningsförmåga vid fysiska, psykiska och sociala påfrestningar hos äldre 427. WHO-definitionen från 2016 lyder: ”en progredierande åldersrelaterad försämring av olika kroppsfunktioner som resulterar i minskade reserver och som leder till stor sårbarhet vid olika påfrestningar och därmed ökar risken för olika typer av negativa hälsoutfall”. Skörhet är förknippat med risk för fall (muskelsvaghet), ökat beroende av andra, vård på sjukhus eller på vårdboende och risk för snar död 428. Många patienter har depression, smärta, nedsatt kognition och låg livskvalitet 428 429.
Sköra äldre är en patientkategori som kan ha svåra symtom och som är en särskild utmaning för palliativ vård eftersom gruppen är svårare att identifiera än till exempel patienter med cancersjukdomar, och inte lika väl undersökt. Svensk forskning har visat att symtombördan bland patienter som räknas som sköra eller finns i riskzonen för skörhet är jämförbar med den bland sjukhusvårdade cancerpatienter 430 och att dessa patienter sällan får tillgång till specialiserad palliativ vård 431. Läs gärna mer i SKR:s stödmaterial Proaktiv vård av sköra äldre.
Risken för skörhet ökar med åldern, från 4 % i gruppen 65–69 år till 26 % i åldern 85+.
Identifiera sköra äldre
För att fler sköra äldre med hög symtombörda ska få tillgång till både allmän och specialiserad palliativ vård är det viktigt att tillståndet identifieras. Skattning för skörhet är en hjälp i den individuella bedömningen av vilken vårdnivå som är lämplig – men kan inte stå ensam.
Det finns många olika instrument för att identifiera skörhet, men ingen golden standard. Ett internationellt utbrett instrument, särskilt inom akutvård, är Clinical Frailty Scale (CFS) som graderar skörhet och funktionsnedsättning på skalan 1–9 432. CFS är enkel att använda, och det är en differentierad skala, vilket gör den lämplig för syftet riskstratifiering. Redan vid nivå 4 bör palliativa vårdbehov övervägas, och vid nivå 7 och däröver ska vården främst handla om att förbättra livskvalitet, det vill säga palliativ vård.
Det är inte den kronologiska åldern, antalet funktionsnedsättande diagnoser eller antalet vårdtillfällen som avgör när vårdens inriktning bör övergå till palliativ vård.
Tecken på att ett palliativt förhållningssätt bör styra vårdens inriktning
Patienten har:
- svårt att klara allmän daglig livsföring, och vilar allt mer
- upprepade oplanerade vårdtillfällen på sjukhus på grund av försämring och
- progredierande nedsatt kognitiv förmåga.
-Läkaren svarar nej på ”förvåningsfrågan”:
Skulle du bli förvånad om patienten inte lever om ett år?
Tecken på att patienten har en kort tid kvar att leva
Patienten:
- är väsentligen sängbunden
- vilar stora delar av dygnet
- kan inte svälja mediciner och kan endast dricka små klunkar.
Brytpunkt
Samtal vid allvarlig sjukdom och brytpunktsbedömningar av den sköra patienten är en fortlöpande process och kräver upprepade helhetsbedömningar. Det är viktigt att överväganden och bedömningar journalförs så att alla vårdaktörer kan ta del av information kring gjorda bedömningar, oberoende av vårdplats.
Patienter med skörhet och palliativa vårdbehov ska ha en läkare som fast vårdkontakt. Kontinuitet i kontakten mellan patient och vård är av stor vikt för att följa förloppet och ge adekvat vård och stöd
För sköra äldre patienter förändras behandlingsmålen fortlöpande; det är alltså en process och sällan något som avgörs vid ett enskilt samtal. Patienten och de närstående behöver tid för att ta in information och bearbeta insikten att livets slutskede närmar sig. De flesta av dessa patienter lider av flera sjukdomar, vilka är mer eller mindre medicinskt påverkbara. Dessutom får biverkningar av läkemedel större betydelse i takt med att livskvaliteten blir viktigare än livsförlängning. Patientens egna önskemål väger också tungt, ibland förmedlade i samråd med närstående. Se även avsnitt 8.2.3 Brytpunktssamtal.
Det är viktigt att den patientansvariga läkaren, som kan ha följt patienten i flera år, ställer sig frågan om patienten utifrån en helhetsbedömning kommer leva om ett halvår eller ett år.
Ofta är det personal i kommunens äldrevård som ser en fortskridande försämring och kan uppmärksamma läkaren på att man bör överväga ett palliativt förhållningssätt. Brytpunktssamtal hålls i förhållande till grundsjukdomen eller sjukdomarna. En akut komplikation bör bedömas separat, och behandlas på adekvat vårdnivå.
För sköra äldre är det viktigt med en uppdaterad vårdplan. Se Kapitel 11 som omfattar medicinska bedömningar och omvårdnadsbedömningar. Palliativa vårdbehov, eventuella genomförda samtal, patientens preferenser och optimal vårdnivå är viktig information för hela vårdkedjan och måste följa patienten genom vården samt uppdateras. En särskild utmaning är att många multisjuka har kognitiv svikt eller demens: 50–70 % av patienterna på äldreboenden har nedsatt kognitiv förmåga. I det läget har de svårt att ta ställning till beslut om vårdinsatser och handläggning vid livets slutskede i ett brytpunktssamtal, även om närstående medverkar. Ibland finns skriftliga önskemål som patienten nedtecknade innan hen blev sämre eller fick kognitiva problem. Sådana är viktiga att beakta, särskilt om de närståendes synpunkter är klart annorlunda än patientens ursprungliga önskemål. Om man inte känner till patientens inställning eller önskemål, via varken närstående eller tidigare anteckningar, måste läkare och övrig personal agera utifrån vad som kan antas vara patientens bästa.
Vidare bör man tidigt i det palliativa förloppet ta ställning till mer avancerad livsuppehållande behandling såsom dialys, HLR och respiratorvård. I regel är dessa vårdformer till mindre nytta för patienten, men avvikelser i vårdrutiner måste dokumenteras och förankras hos patient och närstående.
Läkemedelsbehandling
Ompröva läkemedelsordinationer fortlöpande.
Prioritera symtomlindrande läkemedel.
Säkerställ att patienten får ordinerade läkemedel.
Var observant vid övergång till dosexpedierade läkemedel, eftersom patienter som eventuellt tidigare inte tagit sina mediciner enligt ordination, nu får alla sina mediciner med denna hjälp.
Var beredd på förändrade behandlingsmål och minskad provtagning.
Ompröva avancerad och specifik behandling som är insatt på specialistmottagningar, till exempel cytostatika.
När det gäller multisjuka patienter i eller nära palliativ sjukdomsförlopp måste läkemedelsbehandlingen omprövas. Symtomlindrande läkemedel prioriteras medan riskreducerande kan avslutas 433. Till exempel bör man överväga att sätta ut blodtrycksläkemedel, eller minska dosen, och omvärdera nyttan med fortsatt antikoagulationsläkemedel 434 435.
I tidig palliativ vård ska målsättningen med behandlingen sättas i relation till patientens skörhet och prognos. Högre blodsockervärden kan till exempel accepteras eftersom diabeteskomplikationer inte har någon relevans. Då är det viktigare att undvika risk för lågt blodsocker eftersom det kan ge besvärande symtom och sänka livskvaliteten. Riktigt låga nivåer kan till och med vara livsförkortande.
Många patienter har svårt att hantera sina läkemedel, vilket innebär risk för förväxlingar och oplanerade medicinavslut. Dosexpedierade läkemedel kan då vara ett bra alternativ, och ofta är det ett villkor för att kommunens hemsjukvård ska ta över läkemedelsansvaret. Med dosexpediering blir följsamheten mycket hög, och man bör vara uppmärksam på oväntade biverkningar ifall läkemedel kanske inte tagits enligt ordination tidigare.
De flesta sköra äldre i palliativt sjukdomsförlopp får allt sämre njurfunktion, så läkemedelsbehandlingen är det viktigt att finna en balans mellan symtomlindring och risk för svåra biverkningar på grund av försämrad förmåga att eliminera renalt utsöndrande läkemedel. Kontakt med en nefrolog kan vara värdefull.
Patienter med uttalad skörhet har ofta svårigheter att upprätthålla kontakter med tandvården. Det kan på sikt leda till omfattande behandlingsbehov med ökad risk för infektioner, smärta och malnutrition. Det är viktigt att vården, tandvården och kommuner ombesörjer att patienter med nedsatt autonomi får hjälp till rätt tandvårdsstöd. Många av dessa patienter har rätt till tandvårdsstöd. Perorala läkemedel som lidokainbehandling vid smärta, behandlingar mor svamp och smaklös tandkräm vid illamående bör erbjudas.
När patienten behöver sjukhusvård
En skör patient som behöver sjukhusvård bör direkt läggas in på en avdelning.
Efter utskrivning bör ansvarig läkare snabbt följa upp patientens tillstånd.
När vårdbehovet hos sköra äldre inte kan tillgodoses i hemmet eller på ett särskilt boende ska det finnas möjlighet för vård på sjukhus. Studier av sköra äldre patienter som direktinlagts på avdelning med ett teambaserat arbetssätt, så kallad CGA (Comprehensive Geriatric Assessment), visar mindre risk för försämring av HRQoL (hälsorelaterad livskvalitet) 436 437.
Efter utskrivning är det viktigt att snabbt följa upp patientens tillstånd. Uppföljningen bör göras i samverkan mellan slutenvård, primärvård och kommun, och ska leda till en tydlig behandlingsstrategi som alla vårdaktörer får ta del av. Vid behov av återinläggning ska patienten om möjligt direkt tillbaka till samma avdelning.
Försämringar är vanliga hos sköra äldre. En god planering mellan patientansvarig läkare, patient och vårdpersonal ökar möjligheten att rätt åtgärd vidtas när det händer.
Psykisk sjukdom
Ungefär 1 % av befolkningen har bipolär sjukdom, 1 % har schizofreni och 5 % har någon beroendesjukdom, vilket betyder att dessa patienter inte är ovanliga i den palliativa vården. Samverkan med den psykiatriska vården är därför viktig när det gäller vilken läkemedelsbehandling patienten ska få och hur patienten ska bemötas för att optimera omvårdnaden. Psykiatrin behöver informeras om patientens diagnos, prognos och läkemedelsbehandling, särskilt cytostatika och kortison, samt om psykiskt särskilt påfrestande behandlingar kommer att ges, till exempel strålbehandling.
Pågående behandling, interaktioner
Långtidssjuka med psykiatrisk diagnos och uppföljning står oftast på psykofarmaka som kan interagera med annan behandling, och doseringen kan därför behöva justeras uppåt eller nedåt. Interaktioner mellan psykofarmaka och exempelvis cancerläkemedel är ofullständigt kartlagda. Utsättning av psykofarmaka kan leda till symtom, särskilt om behandlingen avslutas tvärt. Den psykiatriska behandlingen bör i allmänhet fortsätta, men i många fall behöver den modifieras när patienten hamnar i palliativt skede. Samverkan med den psykiatriska vårdgivaren är då viktig, men allmänpsykiater har sällan uppdaterad och fullständig kännedom om interaktioner eller inverkan av somatiska sjukdomar.
De flesta psykofarmaka metaboliseras i levern, och många interagerar med annan behandling via cytokrom P450. Stämningsstabiliseraren litium utsöndras via njurarna och har ett snävt behandlingsintervall eftersom för låga nivåer ger risk för bristande effekt (dvs. risk för återfall i affektiv sjukdom) medan för höga nivåer ger stor risk för njurskada på grund av litiums njurtoxiska egenskaper. Många patienter som vårdas inom palliativ vård får med tiden nedsatt njurfunktion och det finns därför stor risk för att litiumnivåerna blir alltför höga. Täta kontroller av litiumnivåerna i blodet rekommenderas därför, speciellt när njurfunktionen försämras. Även för antiepileptika som ges i stämningsstabiliserande syfte kan man behöva mäta läkemedelskoncentrationerna för att säkerställa att patienten har tillräcklig dos efter dosjusteringar och/eller insättning av interagerande läkemedel. Läkemedelsinteraktionsverktyg kan ge mer information om möjliga interaktioner, t.ex. detta: janusmed.se/interaktioner. De flesta antidepressiva, särskilt SSRI och serotonin-noradrenalinsåterupptagshämmare (SNRI), kan ge utsättningssymtom såsom ångest, vilket kan minskas med nedtrappning över flera veckor, eventuellt under övergång till långverkande SSRI (fluoxetin).
Om patienten är beroende av alkohol eller droger kan samarbetet kring vården bli besvärligt. Patienten kan upplevas som manipulerande eller aggressiv, och inte minst riskerar behandlingen av smärta att bli lidande. Hos opioidberoende individer upplevs inte opioider längre som euforiserande, utan normaliserande, vilket kan vara bra att veta.
Substitutionsbehandling med metadon eller buprenorfin förhindrar opioidabstinens och ger opioidtolerans, men ger bara kortvarig analgesi. Därför kan dessa patienter behöva högre doser opioid vid smärta. Den kliniska erfarenheten är att andningsdepression är mycket sällsynt hos dessa patienter, bl.a. för att smärta är andningsprotektivt. Behandlingen vid dessa tillfällen är kortverkande opioid i tillägg till metadon eller buprenorfin 438.
Patienter med långvarigt bruk av bensodiazepiner eller korstoleranta substanser får vid utsättning eller minskad dos s.k. reboundsymtom, och i svårare fall får de abstinenssymtom. I palliativa situationer är beroendefrågan mindre laddad, men toleransökningen kan vid längre sjukdomstider bli problematisk. Då kan det vara bäst att inleda underhållande ångestbehandling med till exempel SSRI eller buspiron. Övergång till lorazepam (stark beroendepotential) kan övervägas om patienten har kvarstående ångest.
Kronisk njursvikt
Kronisk njursvikt är vanligt i befolkningen och beror inte sällan på annan underliggande sjukdom, exempelvis diabetes eller hjärt- och kärlsjukdom. Allt sämre njurfunktion är också en del av det normala åldrandet. Kronisk njursvikt i stadium IV (GFR <30 ml/min), och framför allt stadium V (GFR <15 ml/min) medför ofta symtom som leder till låg hälsorelaterad livskvalitet och sänkt funktionsnivå i dagliga aktiviteter. Parallellt ses ofta ett ökat behov av sjukhusvård på grund av komplikationer som är relaterade till njursvikt, till exempel ökad infektionskänslighet, hjärt- och kärlsjukdom och tilltagande skörhet.
Patienter med njursjukdom i slutstadiet, och med så kallade uremiska symtom, kan behandlas med dialys eller bli transplanterade, vilket innebär två olika former av njurersättande behandling. För många av dessa patienter är transplantation av olika skäl inte möjlig. Vissa vill heller inte börja med dialys, och det är inte säkert att dialysbehandling bedöms vara till gagn för patienten. Det gäller exempelvis vid kort förväntad överlevnad, hög samsjuklighet och nedsatt funktionsnivå där dialys inte förväntas bidra nämnvärt till vare sig livslängden eller livskvaliteten.
Dialys
Det finns två dialysformer: peritonealdialys och hemodialys. Peritonealdialys kan skötas av patienten eller vårdare i hemmet, antingen genom dagliga upprepade manuella påsbyten eller med maskin, så kallad APD (automatiserad peritonealdialys). Hemodialys ges intermittent och oftast på sjukhus, men vissa patienter kan sköta behandlingen själva i hemmet. Det senare ställer höga krav på patienten och lämpar sig inte för alla. Hemodialys på sjukhus ges vanligen under 4–5 timmar tre gånger i veckan.
Patienter med kronisk njursvikt stadium V som inte vill ha njurersättande behandling, eller som inte bedöms vara aktuella för sådan, ska få medicinskt stödjande behandling. Den består i ett multiprofessionellt omhändertagande för att tillgodose adekvat symtomlindring samt om möjligt korrigera olika rubbningar i kroppen.
För svårt sjuka patienter med dialysbehandling bör frågan om fortsatt dialysbehandling lyftas när nya svårbehandlade symtom eller sjukdomar tillkommer. En viktig aspekt är den tid som dialysbehandlingar tar, i kombination med transporter och i många fall ökad sjukhusvård, eftersom den kan upplevas som betungande för patienten. Om dialysbehandlingen inte bedöms bidra till förlängd överlevnad eller ökad livskvalitet, kan den i samråd med patienten trappas ner och endast ges för symtomlindring, eller sättas ut helt. Medianöverlevnaden efter avslutad dialys är 4–6 dagar.
Palliativ vård i livets slutskede
Vid övergång till palliativ vård i livets slutskede behöver patientens läkemedelslista ses över. Läkemedel som inte längre är nödvändiga sätts ut (fosfatbindare, kaliumsänkande läkemedel, D-vitamin, statiner, natriumbikarbonat etcetera), provtagningar minimeras och palliativa vidbehovsläkemedel sätts in eller optimeras till patientens tillstånd och behov.
Patienter i livets slutskede med njursjukdom lider ofta av smärta, ångest, andningssvårigheter, konfusion, fatigue, illamående, restless legs och klåda. Det finns anpassade skattningsinstrument för patienter med njursvikt (IPOS-Renal och ESAS-r: Renal).
Sedvanliga palliativa vidbehovsläkemedel kan användas, med undantag för morfin och kodein som bör undvikas. Vid läkemedelsbehandling bör man ta hänsyn till graden av njursvikt. Man kan behöva anpassa både läkemedelsdoser och administreringsintervall för att undvika biverkningar till följd av ansamling av läkemedlet eller av aktiva metaboliter (Janusmed 2024). En god tumregel är att starta med låga doser och sedan försiktigt titrera upp dem. Symtomlindringen bör balanseras mot risken för överdosering. Patienten kan behöva opioider mot smärta och andnöd (fentanyl, buprenorfin, metadon, hydromorfon, oxikodon) och benzodiazepiner mot ångest och muskelkramper, men även medel mot illamående (ondansetron, metoklopramid, haloperidol) och klåda (mjukgörande kräm, gabapentin, klemastin, haloperidol, midazolam). Vid neurogen smärta ges gabapentin eller pregabalin i reducerad dos. Om loopdiuretika ordineras behöver man ge en högre dos än vid normal njurfunktion. Utan någon urinproduktion alls ger diuretika endast tveksam effekt på symtomen vid övervätskning. Vid stickningar i fingrarna kan kalciumpreparat behöva ges intravenöst. Restless legs kan behandlas med levodopa, pramipexol eller gabapentin 439 440 441 442 443 444 445 446 447.
