Diagnostik
Bilddiagnostik
Vid adnextumör med misstanke om icke-epitelial äggstockscancer går bilddiagnostisk utredning och remittering till på samma sätt som vid epitelial äggstockscancer, se Nationellt vårdprogram äggstockscancer, epitelial.
De stora internationella organisationerna ger olika rekommendationer om bilddiagnostik vid icke-epitelial äggstockscancer [34-36]. Många av rekommendationerna avseende bilddiagnostiken i det här vårdprogrammet bygger därför även på beprövad erfarenhet och konsensus.
Adnexexpansiviteter
Ultraljud
Transvaginalt ultraljud (TVU) av läkare med god erfarenhet av gynekologiskt ultraljud är av värde vid diagnostik av adnexexpansiviteter, för att skilja benigna tumörer från maligna. Vid spridd cancer kan man utreda vidare med mellannålsbiopsi om primariteten är oklar eller om patienten inte bedöms vara primärt operabel. På alla patienter med misstänkt äggstocksmalignitet utförs även en systematisk transabdominal undersökning för att få en fullständig bild, eftersom många resistenser är stora och sträcker sig ovanför bäckenet.
Många icke-epiteliala adnextumörer har ett karakteristiskt utseende med ultraljud (se bilaga 1 Ultraljudsdiagnostik icke-epiteliala äggstockscancer), vilket tillsammans med analys av icke-epiteliala tumörmarkörer gör att den specifika diagnosen ofta kan misstänkas redan pre-operativt. I bilaga 1 sist i rapporten finns en detaljerad beskrivning av ultraljudsfynd vid olika icke-epiteliala tumörer.
Magnetkamera
Magnetresonanstomografi (MRT) har hög diagnostisk säkerhet när det gäller att skilja mellan maligna och benigna adnexexpansiviteter enligt ORADS MRI-system [37]. I en nyligen publicerad europeisk multicenterstudie inkluderande 1 340 kvinnor med sonografiskt oklara adnexexpansiviteter hade MRT en sensitivitet på 93 % och en specificitet på 91 % [38]. Med MRT kan man oftast avgöra om en adnexexpansivitet utgörs av en benign förändring samt dess karaktär, exempelvis om den är teratom eller fibrom/tekom, vilket gör att specificiteten oftast redovisas högre jämfört med liknande ultraljudsstudier.
MRT inriktas, i detta sammanhang, på lilla bäckenet, men det är tekniskt möjligt att göra diagnostiska MRT-undersökningar av hela buken och även i viss mån av thorax (mediastinum) [39]. För att inte undersökningstiden ska bli för lång får man då välja MRT-protokoll som inte är särskilt inriktade på lilla bäckenet.
MRT-undersökningen ska vara multiparametrisk, dvs. omfatta grundsekvenser men även diffusionsviktade och kontrastmedelsförstärkta sekvenser. Detaljerade rekommendationer för MRT-protokoll för undersökning av gynekologiska expansiviteter i lilla bäckenet finns på Svensk förening för medicinsk radiologis (SFMR:s) webbplats, se Metodböcker från Svensk ureogentitalradiologisk förening (SURF).
Bild- och funktionsmedicinsk och annan preoperativ utredning vid misstänkt icke-epitelial äggstockscancer
Generella rekommendationer
- Gynekologiskt ultraljud är förstahandsmetod för undersökning av adnextumör. Ultraljudsfynd som kan tala för icke-epitelial äggstockscancer beskrivs i bilaga 1 Ultraljudsdiagnostik icke- epiteliala äggstockscancer.
- Cytologi bör utföras vid ascites eller pleuravätska.
- Preoperativ biopsi bör enbart utföras vid tecken på spridd sjukdom.
- Vid klinisk misstanke om malign äggstockscancer hos kvinnor < 40 år bör man ta prov för alfafetoprotein (AFP), humant koriongonadotropin (hCG) i serum och laktat-dehydrogenas (LD), förutom CA 125. Därutöver kan placentalt alkaliskt fosfatas (PLAP) ibland vara förhöjt vid dysgerminom. Inhibin B och Anti-Müllerskt hormon (AMH) kan vara förhöjt vid granulosacellstumörer, och båda bör analyseras vid misstänkt granulosacellstumör. Ett alternativ är att frysa ner preoperativt serumprov för senare analys efter histologiskt svar. Vid förhöjda tumörmarkörer bör dessa följas tills de normaliserats. S-kalcium är viktigt vid misstanke om småcellig cancer av hyperkalcemisk typ.
- DT thorax-buk bör utföras preoperativt för att kartlägga tumörutbredning. Vid överraskningsdiagnos utförs DT torax-buk postoperativt inför ytterligare behandling.
- MRT kan utföras om ultraljud inte är konklusivt, eller om mer information önskas om lokal tumörutbredning inför avancerad kirurgi.
- Definitiv diagnos kan endast ställas genom histopatologisk undersökning av adnexexpansivitet.
Övrig utredning
- Vid misstanke om gonadoblastom bör karyotypbestämning utföras eftersom dessa kan ha kromosomavvikelser och tumören kan utvecklas från outvecklade gonadanlag [40].
- Vid misstanke om granulosacellstumör och tekom bör endometriebiopsi tas för att utesluta samtidig endometriecancer.
- Vissa småcelliga karcinom kan ge hyperkalcemi, hyponatremi och inadekvat ADH-sekretion (SIADH) som kan ge trötthet, illamående, huvudvärk och kräkningar samt kramper [41].
- Vissa germinalcellstumörer (gulesäckstumörer, embryonala karcinom och koriokarcinom) är högmaligna tumörer och kräver ett snabbt omhändertagande (inom 2 veckor).
DT thorax-buk med intravenös kontrastmedelstillförsel ger information om tumörspridning som är viktig för den preoperativa bedömningen med behandlingsbeslut under den multidisciplinära konferensen (MDK).
Om det i enskilda fall är intressant att visualisera urinvägarna i detalj, och få information om utsöndring, bör detta anges på remissen, så att undersökningen inkluderar bilder enligt DT-urografiprogram. Vid gravt nedsatt njurfunktion kan MRT besvara denna frågeställning.
Tumörgenomväxt till tarm kan i viss mån påvisas med DT, men vid oklarhet bör i första hand MRT utföras.
Vårdprogramgruppen anser att det i dag inte finns evidens för att rekommendera positronemissionstomografi (PET-DT) vid all utredning före behandling. PET-DT kan dock övervägas om utbredd metastasering inte har påvisats med tidigare metoder och stor kirurgi planeras, eller vid andra särskilda situationer som diskuterats på MDK.
Remissinformation
Av remissen för radiologisk undersökning bör det framgå om patienten tidigare är opererad i buk eller bäcken eller har genomgått strålbehandling, om och var det finns tidigare bilddiagnostiska undersökningar samt om det finns kontraindikationer för de olika undersökningarna, t.ex. kontrastmedelsallergi, njursvikt eller vissa typer av pacemaker eller andra implantat. Kortfattad beskrivning av fynd vid den gynekologiska undersökningen med ultraljud samt uppgifter om eventuell ärftlighet och tumörmarkörer/hormonellt status är värdefull tilläggsinformation i remisstexten.
Tumörmarkörer vid icke-epitelial äggstockscancer
Germinalcellstumörer (tumörmarkörer)
Rekommendationer
- Tumörmarkörer har en viktig roll i diagnostik, behandling och uppföljning av germinalcellstumörer.
- Preoperativt serumprov för bestämning av AFP, hCG, LD och CA 125 rekommenderas vid misstanke om malign adnextumör hos kvinnor < 40 år.
- Vid gulesäckstumör är AFP-nivåerna ofta mycket höga och används för att styra behandlingen. Samma gäller hCG vid koriokarcinom. Vid embryonalt karcinom och blandtumörer kan måttligt förhöjda värden av den ena eller båda markörerna förekomma.
- Vid rent dysgerminom är AFP normalt och hCG normalt eller endast lätt förhöjt.
- Falskt förhöjda värden i serum av AFP och hCG är sällsynta, men kan förekomma om heterofila antikroppar mot djurprotein finns hos patienten. Försiktighet rekommenderas i fall där laboratorieresultat inte stämmer med kliniska fynd.
- Olika testmetoder ger ofta olika resultat vid analys av markörer, särskilt för hCG.
- Serumvärden av tumörmarkörer från olika sjukhuslaboratorier kan skilja sig åt avsevärt.
Alfafetoprotein (AFP)
Alfafetoprotein (AFP) är ett onkofetalt antigen och transportprotein med molvikt 70 kD, och är fostrets motsvarighet till albumin. AFP produceras hos fostret i gulesäcksvävnad, gastrointestinal vävnad och lever och förekommer i riklig mängd i gulesäck och amnionvätska. AFP är förhöjt hos 60–70 % av alla patienter med testikelcancer av icke-seminomtyp.
AFP är en känslig markör för vissa varianter av maligna germinalcellstumörer i ovariet (tabell 2). Vid gulesäckstumör (malign endodermal sinustumör) är AFP- nivåerna ofta mycket höga och används för att styra behandlingen. AFP är också lätt till måttligt förhöjt i flera fall av embryonala karcinom och maligna teratom av blandtyp, och kan då användas kliniskt tillsammans med hCG som markör. Vidare kan förhöjt AFP bero på gastrointestinal malignitet, leversjukdom, graviditet eller ärftlig persisterande AFP [42].
Humant koriongonadotropin (hCG)
Hormonet hCG produceras under graviditet av moderkakans cytotrofoblastceller. Det är ett glykoprotein med molvikt 36 kD och består av en alfa- och en betaenhet samt åtta olika sido-sockerkedjor. Kombinationen av dessa resulterar i stor variabilitet i strukturen av hCG. I serum och urin förekommer ordinärt hCG men också minst fem ytterligare former. När hCG används som tumörmarkör vid mola, malign trofoblastsjukdom och germinalcellstumörer är det viktigt att använda en metod som korrekt mäter alla varianter av hCG och beta-hCG. Vissa metoder kan ge falskt låga värden vid persisterande sjukdom efter behandling. Man kan heller inte jämföra analysresultat från olika laboratorier utan vidare, vilket har betydelse när patienter remitteras mellan olika sjukhus [43, 44].
Vid malign germinalcellstumör av blandtyp förekommer ibland stegring av hCG-nivå (tabell 2). I dessa fall kan markören användas i kombination med AFP. Vid embryonala karcinom är hCG förhöjt i cirka hälften av fallen, och vid koriokarcinom är hCG kraftigt förhöjt och används för att monitorera behandlingseffekten. Vid rena dysgerminom kan hCG-nivån vara lätt förhöjd. Om denna markör är mera påtagligt förhöjd i serum är det inte fråga om ett rent dysgerminom, och en patolog bör konsulteras för kompletterande diagnostik.
Tabell 2. Tumörmarkörer vid maligna germinalcellstumörer i ovariet
|
|
AFP |
hCG |
LD |
CA-125 |
|
Dysgerminom |
_ |
+ |
+ |
+ |
|
Gulesäckstumör |
+ + + |
_ |
+ |
+ |
|
Omoget teratom (rent) |
_ |
_ |
+ |
+ |
|
Embryonalt karcinom |
+ |
+ |
+ |
+ |
|
Koriokarcinom |
_ |
+++ |
+ |
-/+ |
|
Blandad germinalcellstumör |
+ |
+ |
+ |
+ |
+ + +: Hög nivå i serum.
+: Förhöjd eller normalnivå i serum.
AFP: Alfafetoprotein
hCG: Koriongonadotropin
LD: Laktatdehydrogenas
Användning av AFP och hCG i serum för att monitorera behandlingseffekt
Om AFP- och/eller hCG-nivån i serum är förhöjd preoperativt eller postoperativt vid germinalcellstumör i ovariet, kan den ena eller båda av dessa markörer användas för att monitorera behandlingseffekten efter kirurgi och under cytostatikabehandling. Halveringstiderna är < 7 dygn för AFP, och 3 dygn för hCG efter radikal kirurgi eller under effektiv cytostatikabehandling. Om inte markörvärdena följer denna halveringsakt kan det innebära att det finns en resttumör eller att cytostatikabehandlingen har otillräcklig effekt. Vid testikelcancer av icke-seminom-typ har förlängd halveringstid av någon av de två markörerna i serum visat sig vara prognostiskt ogynnsamt. Den svensk- norska SWENOTECA-gruppen rekommenderar därför noggrann monitorering av AFP och eller hCG i serum under pågående cytostatikabehandling [45], se även fördjupningslitteratur på SWENOTECA.
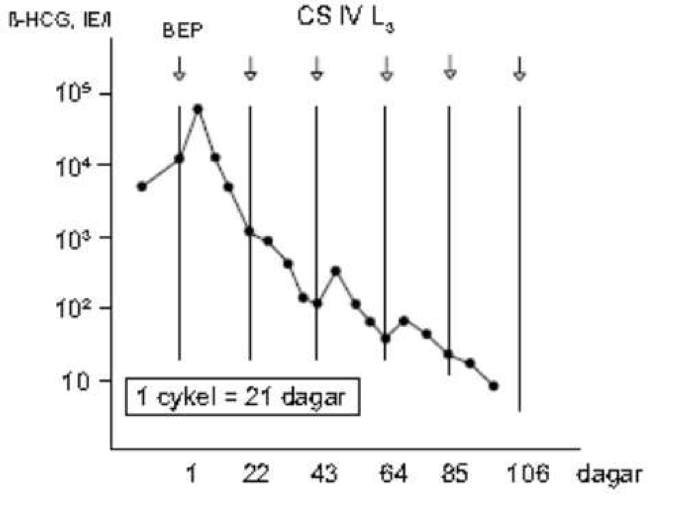
Prov för AFP och eller hCG tas dag 1, dag 5 och dag 15 i varje behandlingscykel och halveringstiden mäts utifrån detta peak-värde enligt figur 5. I praktiken plottas markörvärdena i semilogaritmiska nomogram, se figur 6. Vid cytostatikabehandling mot manifest sjukdom eller vid resttumör efter operation, kan dock en ut svämning av AFP eller hCG ske i serum direkt efter cytostatikakuren med ett temporärt peak-värde. Detta ska inte ska tolkas som behandlingssvikt. Vidare kan man vid mycket hög tumörmarkörnivå före cytostatikabehandling (ß-hCG >100 000 IE/L och AFP > 50 000 ug/L) notera att minskningstakten följer halveringskurvan de första 2–3 cytostatikacyklerna för att avta efter den 3:e eller 4:e kuren och förbli något förhöjd (hCG- eller AFP-värden runt 30–50 ug/L ), och därefter bara långsamt minska. Detta fenomen ska inte betraktas som behandlingssvikt. Vid tecken på bristande respons eller om tolkningen är osäker rekommenderas rådgivning med kollegor i vårdprogramsgruppen och med onkologer som är experter på testikelcancer.
Figur 5. Exempel på förhöjt peak-värde av hCG i serum på dag 5 efter 1:a cytostatika cykeln vid avancerad testikelcancer (SWENOTECA III och IV, 1999)
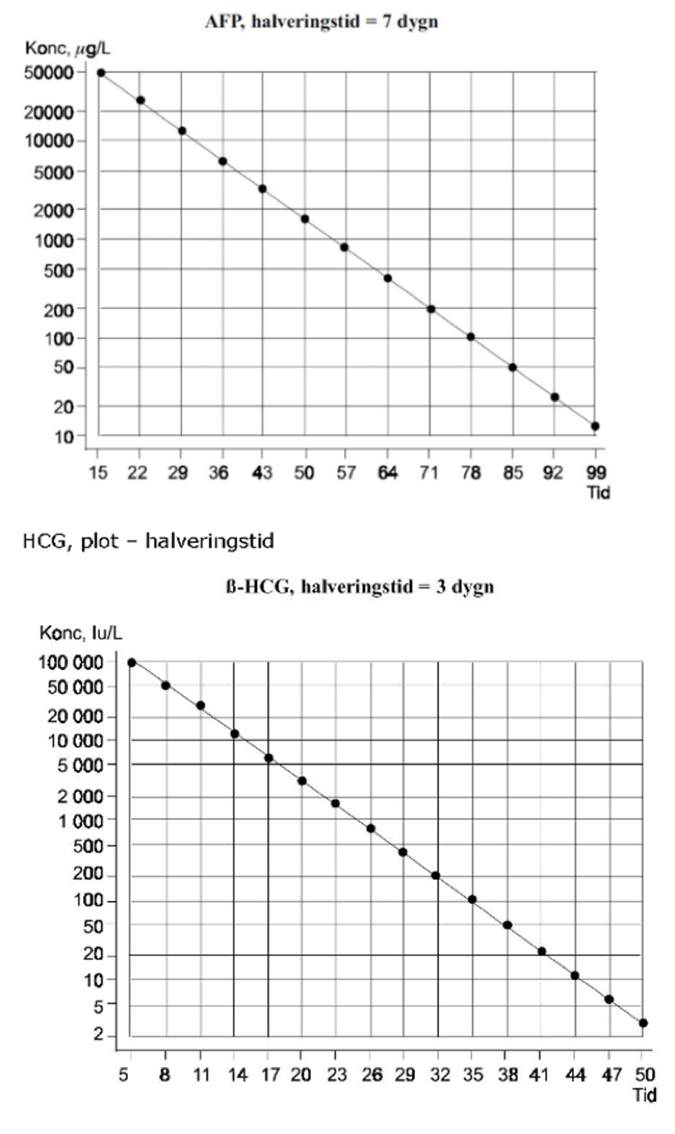
 Figur 6. Logaritmiska nomogram för plottning av AFP och hCG i serum under cytostatikabehandling (SWENOTECA VIII, 2012)
Figur 6. Logaritmiska nomogram för plottning av AFP och hCG i serum under cytostatikabehandling (SWENOTECA VIII, 2012)
Könssträngs- och stromacellstumörer (tumörmarkörer)
Rekommendationer
- Vid könssträngs- och stromacellstumörer är nivåerna av inhibin, särskilt inhibin B, och Anti-Müllerskt hormon (AMH) förhöjda i serum i majoriteten av fallen, särskilt vid granulosacellstumör. För att öka sensitiviteten rekommenderas att båda dessa hormoner analyseras.
- Preoperativt serumprov för bestämning av inhibin B, AMH och CA 125 rekommenderas. Alternativt kan fryst serum förvaras i väntan på histologisk bedömning av operationspreparaten och senare analys.
- Inhibin B och AMH kan även användas i uppföljningen under och efter behandling.
FSH och östradiol
Follikelstimulerande hormon (FSH) är ett hypofyshormon som utsöndras i kraftigt förhöjda nivåer efter menopaus på grund av upphävd feedback från ovariet via östradiol och inhibin. Granulosacellstumörer är i många fall östrogenproducerande. Patienter med dessa tumörer kan därför få symtom på östrogenproduktion, till exempel blödningar efter menopaus. I serum konstateras då inte sällan förhöjd östradiolnivå och sänkt FSH-nivå.
Den kliniska nyttan av rutinmässiga hormonbestämningar är tveksam och rutinmässig hormonbestämning rekommenderas inte. Däremot kan dessa analyser vara av visst värde vid klinisk misstanke om granulosacellstumör. I dag finns dock känsligare och mer specifika serummarkörer (inhibin och AMH) för granulosacellstumörer.
Inhibin
Inhibin är ett peptidhormon med en alfa-kedja och en beta-kedja, och det produceras i testikelns Sertoliceller och i ovariets granulosa- och tekaceller i folliklarna. Inhibin är involverat i de hormonella feedbackmekanismerna som styr ovarierna. Normalt hämmar inhibin FSH-sekretionen i hypofysen. Inhibin B bildas fysiologiskt i primärfolliklar och små folliklar under utveckling, medan inhibin A bildas i den fullt utvecklade, dominanta follikeln samt i corpus luteum efter ovulationen. Fysiologiska serumnivåer av inhibin A (< 150 ng/L) och B (< 200 ng/L) fluktuerar under menstruationscykeln.
Hos friska kvinnor som genomgått menopaus är inhibin A < 5 ng/L och inhibin B < 15 ng/L.
Vid granulosacellstumör är halten av inhibin patologiskt förhöjt i majoriteten av fall. Inhibin B i serum, mätt med modern metodik, är mer förhöjt över fysiologiska nivåer (cirka 60 gånger) än inhibin A (cirka 6 gånger) vid klinisk progressiv tumörsjukdom [46-48], Inhibin B lämpar sig därför bäst att mäta vid granulosacellstumör och andra könssträngs- och stromacellstumörer. I en studie påvisades inhibin B-nivåer i intervallet 327–22 520 ng/L vid granulosacellstumörer. I andra studier [46, 49] har sensitiviteten för inhibin B i serum, när det gäller att påvisa granulosacellstumör, varit 89–100 %. Falskt negativ serumnivå av inhibin B kan dock förekomma. Specificiteten för inhibin B var å andra sidan 100 % i de studierna. Inhibin sjunker till låga eller ej påvisbara nivåer efter kirurgi [49, 50].
Anti-Müllerskt hormon (AMH eller MIS)
Anti-Müllerskt hormon (AMH, även kallat ”müllerian inhibitory substance”, MIS) tillhör (liksom inhibin) tillväxtfaktorfamiljen TGF-beta. AMH är ett glykoprotein som fysiologiskt modulerar ovariets follikeltillväxt genom att selektera en dominant follikel och reducera övriga folliklars känslighet för stimulerande FSH. I motsats till inhibin är AMH-nivån i serum konstant under menstruationscykeln. Efter menopaus sjunker AMH till låg eller ej påvisbar nivå. AMH i serum sjunker även före menopaus i takt med att det finns allt färre aktiva folliklar i ovariet.
En förhöjd serumnivå av AMH är mycket specifik för granulosacellstumör [51, 52] men förekommer även vid Sertolicellstumör. Förhöjd AMH-nivå har inte påvisats vid någon annan benign eller malign äggstockscancer eller vid annan typ av cancer.
I en studie fann man förhöjda nivåer av AMH hos 8 av 9 patienter (89 %) med progressiv granulosacellstumör [52]. I andra studier var sensitiviteten för AMH ,för att påvisa sjukdomsprogress, vid granulosacellstumör 76–91 % [47, 48, 51], så falskt negativ AMH-nivå kan förekomma vid granulosacellstumör [49]. I ytterligare en studie föreslogs därför att både inhibin B och AMH skulle mätas för att öka sensitiviteten [53]. AMH i serum har inte korrelerat med tumörstadium och tycktes inte heller korrelera med inhibin-nivån [47, 51].
Efter framgångsrik kirurgi eller annan behandling sjunker AMH-nivån i serum till mycket låg eller ej påvisbar nivå på några få dagar. AMH kan därmed användas för att bedöma kirurgisk radikalitet och för att förutsäga sjukdomsåterfall.
Diagnosbesked
Rekommendation
- Patienter bör få saklig individuellt anpassad information om sjukdomen, dess behandling och förväntat resultat, så att de kan göra ett grundat ställningstagande till den behandling som erbjuds. Vid diagnosbeskedet som läkare ger, bör kontaktsjuksköterska närvara.
- Patienter bör få ett eller flera uppföljande samtal som upprepar och kompletterar informationen från diagnosbeskedet.
Oftast är inte diagnosen helt säkerställd vid undersökningen hos gynekolog eller vid första besöket på en kvinnoklinik eller ett tumörkirurgiskt centrum. Patienten bör få så noggrann information som möjligt och hur utredningen och planeringen kommer att fortgå, från beskedet om att man misstänker äggstockscancer tills en definitiv diagnos finns. Informationen bör vara både muntlig och skriftlig.
Framgångsrik patientinformation kan mätas i kortare vårdtid och sjukfrånvaro, postoperativt mer fysisk aktivitet och rörlighet, mindre smärtupplevelse och analgetikakonsumtion samt mindre oro [54, 55].
Hållpunkter för diagnosbeskedet och uppföljande samtal:
- Uppmana patienten att ha en närstående med sig. Den närstående har då möjlighet att efter besöket komplettera med information som patienten inte har uppfattat eller kunnat ta till sig.
- Ge information om sjukdomen och behandlingen: förväntat sjukdomsförlopp, behandlingsmöjligheter, komplikationer och tidsperspektiv.
- Ta upp påverkan på arbetsförmågan. Berätta om de sjukskrivningsregler som gäller enligt rekommendationer från Socialstyrelsen samt om olika högkostnadsskydd.
Alla inblandade vårdaktörer ska få del av den information som är viktig för patientens sjukdom och behandling.
