Behandling av återfall
Rekommendation
- Vid recidiv efter kemoimmunterapi: ibrutinib eller akalabrutinib.
- Vid recidiv efter avslutad underhållsbehandling med kovalent BTK-hämmare: återstart av ibrutinib eller akalabrutinib.
- Vid recidiv efter kovalent BTK-hämmare som recidivbehandling, eller progression under pågående behandling med kovalent BTK-hämmare, rekommenderas CAR-T (brexu-cel eller liso-cel) för patienter som bedöms lämpliga.
Andra alternativ:
- Pirtobrutinib
- R-bendamustin
- R-BAC
- R-GEMOX
- R-lenalidomid
- VR-CAP
Recidiv efter kemoimmunterapi – BTK-hämmare
Den preparatgrupp som är mest väletablerad i form av respons och långtiseffekt vid recidiverande MCL är kovalenta BTK-hämmare (BTKi) (+++). Det finns ett flertal preparat på marknaden, men i Europa är ibrutinib och akalabrutinib registrerade på denna indikation. Dessa preparat rekommenderas därför för de flesta patienter som andra linjens behandling efter kemoimmunterapi, och ges som kontinuerlig behandling fram till sjukdomsprogress. I denna situation ges BTK-hämmare som monoterapi, dvs. inte i kombination med rituximab.
Kommentar:
För hantering av biverkningar av BTK-hämmare, såsom blödningsbenägenhet, arytmier, infektioner och hypertoni, hänvisas till Nationellt vårdprogram för kronisk lymfatisk leukemi.
Tillägg av venetoklax till ibrutinib har visats förbättra behandlingsutfall men då venetoklax ännu inte är godkänt på denna indikation kan det inte rekommenderas 57.
Ett flertal kliniska prövningar pågår med nya läkemedel för recidiverande MCL, och man bör därför alltid ställa sig frågan om en patient i denna situation kan ingå i en klinisk prövning.
Recidiv efter avslutad underhållsbehandling med kovalent BTK-hämmare
Då underhållsbehandling med kovalent BTKi numera rekommenderas som led i standardbehandlingen (enligt TRIANGLE), kan situationen uppstå att patienten bibehåller sin remission under underhållsbehandling men recidiverar i ett senare skede.
Rekommendationen är då att återinsätta behandling med ibrutinib eller akalabrutinib om minst 6 månader förflutit sedan senaste dosen av BTKi. Också i denna situation ges BTK-hämmare som monoterapi, dvs inte i kombination med rituximab.
Recidiv efter kovalent BTK-hämmare
CAR-T-cellsbehandling
För patienter som tidigare behandlats med kovalent BTK-hämmare som recidivbehandling, eller progredierar under sådan behandling, är för närvarande den mest effektiva behandlingen CAR-T i form av brexukabtagen-autoleucel (brexu-cel) eller lisokabtagen-maraleucel (liso-cel).
Dessa två preparat är godkända i Sverige för behandling av vuxna patienter med recidiverande eller refraktärt mantelcellslymfom (MCL) som tidigare erhållit systemisk behandling med bland annat en BTK-hämmare. Detta innebär att även patienter som erhållit BTK-hämmare i primärbehandlingen, exempelvis patienter behandlade enligt TRIANGLE, är aktuella för CAR-T vid sitt första recidiv.
Baserat på inklusionskriterier och internationella erfarenheter 58 har nedanstående riktlinjer för behandling med CAR-T-cellsbehandling utarbetats av den svenska RCC-CAR-gruppen.
CAR-T-cellsbehandling ska endast administreras av kvalificerade centrum och föregås av nationell MDK. Man bör ta i beaktande att risken för allvarlig neurotoxicitet och hematologisk toxicitet tycks vara högre vid MCL jämfört med DLBCL.
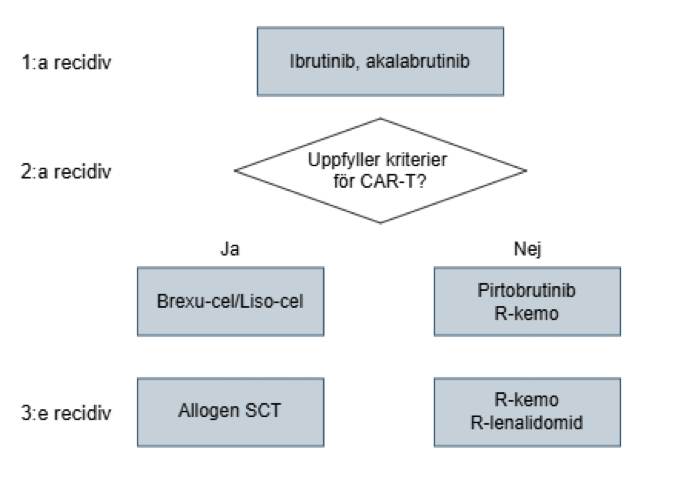
Figur 1.Behandlingsalgoritm för recidiv av MCL
Remitteringsgång
- Patient bedöms uppfylla kriterier för CAR-T-cellsbehandling.
- Sätts upp på nationell MDK.
- Fallet diskuteras, och om CAR-T-celler rekommenderas föreslås behandlingsort i första hand på bas av geografisk närhet/regiontillhörighet.
- Ansvarig läkare meddelas och skriver remiss till CAR-T-behandlingssjukhus.
- Patienten kallas för leukaferes.
- Handläggning i väntan på CAR-T-celltillverkning diskuteras.
- Lymfodepletion och CAR-T-celler ges på CAR-T-cellssjukhuset.
- Patienten övervakas med avseende på akuta biverkningar.
- Patienten registreras i EBMT-registret, Register för cancerläkemedel och nationella lymfomregistret av CAR-T-cellssjukhuset.
- Utvärdering av respons med PET-CT och benmärgsundersökning efter 30 och 90 dagar.
- Uppföljning för behandlingseffekt och biverkningar var 3:e månad i 2 år sedan för eventuella senbiverkningar i 15 år.
Bridging-/holdingbehandling
Mycket talar för att det är fördelaktigt att minska tumörbördan så mycket som möjligt före CAR-T-cellsbehandling. För att åstadkomma detta får patienten så kallad bridging terapi under tillverkningen av CAR-T-celler. Behandlingen väljs utifrån vad patienten tidigare behandlats med och responderat på. Strålbehandling mot lokaliserad sjukdom kan vara ett gott alternativ vid MCL 58. Pirtobrutinib kan också utgöra ett alternativ i denna situation.
I vissa fall krävs också behandling innan leukaferes, så kallad holdingbehandling, med anledning av mycket snabbt progredierande sjukdom. Val av behandling får också här individualiseras.
Specifika biverkningar av CAR-T-celler
De allvarligaste biverkningarna av CAR-T-celler är cytokinfrisättningssyndrom (CRS) och neurotoxicitet (immune effector cell associated neurotoxicity syndrome, ICANS) 59.
CRS kommer ofta de första dagarna efter CAR-T-celler och orsakas av en kraftig immunaktivering. Kardinalsymptomen är feber, hypotension och hypoxi men alla organsystem kan drabbas. CRS kan ofta behandlas framgångsrikt med anti IL6-R antikroppen tocilizumab (Roactemra) och steroider. En infektion kan driva ett CRS och empirisk infektionsbehandling är ofta nödvändig. Notera att om tocilizumab givits stiger inte CRP som förväntat vid efterföljande infektion.
Neurotoxicitet orsakas sannolikt av cytokiner och inträffar någon dag senare än CRS och kan vara alla typer av neurologiska symtom. Behandlingen är steroider och neurologisk övervakning. Dödsfall finns beskrivna både för CRS och ICANS. Risken för svår ICANS tycks vara högre vid MCL.
Sena biverkningar har hittills varit långdragen pancytopeni som behandlas med transfusioner och eventuellt G-CSF, samt B-cellsaplasi då alla normala B-celler uttrycker CD19. Risken för långdragen cytopeni och svåra infektioner (aplastisk fenotyp) tycks vara högre för patienter med mantelcellslymfom. Frikostighet med antibiotikaförskrivning bör gälla i denna situation. Om Ig-brist i kombination med upprepade bakteriella infektioner ges substitution. Internationella riktlinjer finns tillgängliga för hantering av ovanstående biverkningar.
Allogen stamcellstransplantation
Allogen stamcellstransplantation (SCT) ger möjlighet till långtidsremission hos patienter med återfall av mantelcellslymfom (+++). Yngre patienter som tidigare genomgått högdosbehandling med autologt stamcellsstöd och i förekommande fall CAR-T bör därför värderas för allogen SCT, med hänsyn till biologisk ålder och samsjuklighet 60. Behandlingen är dock förknippad med en betydande sjuklighet och dödlighet.
För att uppnå tillräckligt stabil remission inför allogen SCT bör patienten få induktionsbehandling, vilken är beroende av vilken primärbehandling som givits.
Övriga patienter
Behandlingsvalet avgörs här av vilken primärbehandling som givits. Vid icke-symtomgivande sjukdom kan exspektans övervägas också vid återfall. Ett nytt alternativ som visat aktivitet även hos patienter med recidiv efter behandling med kovalent BTKi är pirtobrutinib, en icke-kovalent BTK-hämmare 61.
Om > 6 månader förflutit sedan senaste dosen rituximab, bör rituximab övervägas som tillägg till kemoterapi.
Föreslagna behandlingsalternativ:
- Pirtobrutinib (++)
- Lenalidomid +/- rituximab (++)
- R-bendamustin (++)
- R-BAC (++)
- VR-CAP (++)
- R-GEMOX (++).
R-BAC ges vid återfall i följande dosering: bendamustin 70 mg/m2 dag 1–2 och cytarabin 500 mg/m2 dag 1–3. Rituximab ges dag 1.
Lenalidomid ges i dosen 25 mg/dag i 3 veckor, följt av 1 veckas paus. Kan också kombineras med rituximab, 375 mg/m2, givet med fyra veckors intervall (++).
Andra lovande läkemedel under utveckling för patienter med återfall av MCL är BCL2-hämmarna venetoklax och sonrotoclax 62, glofitamab, en bispecifik CD20/CD3 antikropp 63, liksom BTK-degraderare 6465. Dessa läkemedel är dock ännu ej godkända för användning vid MCL.
CNS-återfall
Här rekommenderas i första hand behandling med kovalent BTKi 66 (+++). Patienter med respons på behandling bör också anmälas till nationell CAR-T MDK för diskussion om behandling med CAR-T cellsbehandling, då respons verkar likvärdig med den som ses hos patienter utan CNS-återfall i registerstudier (+).
I andra hand kan behandling ges som vid primärt CNS-lymfom. Förslagsvis kan DeAngelis-protokollet användas 67: MVP x 5, konsolidering med högdos cytarabin x 2 (+). Strålbehandling kan också övervägas.
Vid CNS-återfall efter genomgången CAR-T-cellsbehandling är alternativen färre, men strålbehandling eller icke-kovalenta BTK-inhibitorer kan prövas.
Strålbehandling
Mantelcellslymfom är en mycket strålkänslig tumör, varför låga doser av strålbehandling (4 Gy x 2) är en utmärkt effektiv och vältolererad behandling i symtomlindrande syfte (++) 68. Detta kan också ges mot stora områden, exempelvis buken.
