Symtom
Detta kapitel om symtom som kan uppstå vid palliativ vård är uppbyggt utifrån ett teambaserat arbetssätt. För varje symtom beskrivs initialt definition, förekomst och orsaker, sedan bedömning, anamnes och undersökningar. Behandlingen för varje enskilt symtom delas in i orsaksinriktade, icke-farmakologiska och farmakologiska åtgärder. Varje avsnitt avslutas med information om patientmedverkan och kommunikation med patienten och de närstående.
Akut konfusion/delirium
Akut konfusion eller delirium är vanligt förekommande, framför allt i sent palliativt sjukdomsskede. Det förorsakar stort lidande för både patienten och de närstående, och gör det svårt för patienten att förmedla sig. Tillståndet skapar ofta även utmaningar för vårdpersonalen.
Definition, förekomst och orsaker
Akut konfusion definieras som snabb utveckling av störningar i uppmärksamhet och kognitiv förmåga. Medvetandegraden kan vara fluktuerande. Riskfaktorer för att utveckla akut konfusion är demens, tidigare förvirring, hög ålder, nedsatt syn eller hörsel, sömnbrist och miljöombyte.
Tabell 4. Konfusion kan utifrån patientens agerande indelas i hyperaktiv eller hypoaktiv
|
Hyperaktivt delirium |
Hypoaktivt delirium |
|
Motorisk oro. Kan misstolkas som oro eller ångest och öka risken för felbehandling. |
Trötthet, slöhet, psykiskt dämpad och mer sängliggande. |
|
Stönande och ljud som saknar mening |
Svårt att bibehålla uppmärksamhet i kontakt med andra |
|
Hallucinationer eller vanföreställningar |
Kan misstolkas som fatigue eller depression vilket ökar risken för felbehandling |
Det är vanligt att patienten är hypoaktiv dagtid men hyperaktiv nattetid, dvs. har ett fluktuerande delirium.
Differentialdiagnoser och potentiellt bidragande orsaker till delirium
Delirium kan bland annat bero på:
- läkemedelsbiverkningar, särskilt vid behandling med opioider, bensodiazepiner, tricykliska antidepressiva och antikolinergika
- otillräcklig symtomlindring vid till exempel smärta
- ökat ödem hos patienter med känd CNS-metastasering
- symtomgivande hyperkalcemi, hyponatremi
- hypo- eller hyperglykemi
- leversvikt
- hypoxi
- urinretention.
Bedömning, anamnes och undersökningar
Tillstånd med akut förvirring och delirium förbises ofta, och det finns en risk för att de missbedöms och uppfattas som depression, oro eller ångest eller ses som att patienten enbart har ett avvikande beteende 448 449 450 . Tidig upptäckt av tecken på konfusion, med störd dygnsrytm och sömn, är avgörande för prognosen eftersom en tidig diagnos möjliggör bättre effekt av icke-farmakologiska interventioner och lågdos medicinering med mindre biverkningar. Av samma skäl är icke-farmakologiska interventioner första steget i en behandling av konfusion.
Vid bedömning av en patient med exempelvis förändrat mentalt tillstånd kan man utgå från följande tre perspektiv:
- medvetandegrad: exempelvis medvetslös, sovande men väckbar, helt klar och alert, rastlös, upprörd eller våldsam
- kognition: exempelvis uppmärksamhet, minne, inlärning, medvetande, språk och beslutsfattande, problemlösning, orienterad till tid, rum och person samt förekomst av hallucinationer
- typ av förlopp: hastig försämring eller fluktuerande tillstånd.
Anamnes, kroppslig undersökning och andra undersökningsresultat ger en hållpunkt för att bedöma eventuell intoxikation, abstinensproblematik, läkemedelsbiverkan eller annan organisk orsak än neurodegenerativ grundsjukdom (DSM-5).
Konfusion kan bedömas med hjälp av Confusion Assesment Method (CAM) 451.
Behandling vid akut konfusion/delirium
Orsaksinriktad behandling
I första hand bör man behandla bakomliggande orsaker såsom urinretention, hypoglykemi eller hyperglykemi.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Icke-farmakologisk behandling går ut på att på olika sätt minska överbelastande stimuli till hjärnan. Den kan innebära att skapa en lugn och tyst miljö genom att till exempel ta bort yviga krukväxter och fladdrande gardiner, stänga av ljud från radio och ljud och bild från tv samt ha nattljus för att minska skrämmande och hallucinogena skuggor. Rummet bör även ha en tydligt synlig klocka och kalender. Vårdpersonalen behöver också göra patienten delaktig i vad som sker genom att tala om vad som händer i vårdsituationen och vem som är närvarande i rummet.
Om vårdpersonalen saknar kunskap och erfarenhet av att tidigt upptäcka tecken på kognitiv svikt och konfusion finns risk för att patienten inte får tidiga icke-farmakologiska interventioner och farmaka i lågdos, vilket i sin tur ökar risken för behandlingsresistent delirium och senare behov av sedering som behandling. Fenomenet beskrivs i litteraturen som en ”destruktiv triangel” mellan 1. hyperaktivt delirium (konfusion) som leder till 2. ökad oro och utmattning hos patient och närstående, och sedan 3. utmattad och stressad vårdpersonal som känner sig manade att sedera patienten, vilket i sin tur ökar patientens konfusion osv. 452.
Figur 5. Destruktiva triangeln
Illustration: Åsa Johansson, RCC Norr.
Farmakologisk behandling
Vid utebliven effekt av omvårdnadsåtgärder, och om patienten tycks ha besvärande agitation, paranoida vanföreställningar eller svår oro, är neuroleptika förstahandsvalet i farmakologisk behandling. Pröva per oral klometiazol 300 (–600 mg) 1–3 gånger dagligen. Som alternativ kan haloperidol i låg dos, 0,5–1 mg peroralt eller subkutant med doseskalation upp till 3 mg eller risperidon eller olanzapin prövas.
Vid uttalade sömnstörningar där starkare sederande effekt önskas föreslås Levomepromazin som alternativ. Beakta att den parenterala beredningen är licenspreparat.
Bensodiazepiner bör undvikas i behandling av delirium eftersom de kan förvärra patientens symtom.
För sköra äldre avråds behandling med antipsykotiska eller antikolinerga läkemedel och långverkande bensodiazepiner. Överväg Klometiazol 300 mg till natten under begränsad tid och i undantagsfall.
I ett sent palliativt skede är målet att lindra plågsamma symtom av konfusion.
Patientmedverkan och information till patient och närstående
Det finns pedagogiska fördelar med att förklara för patient, närstående och vårdpersonal att konfusion är ett tecken på ”hjärnsvikt” – hjärnan har svårt att sortera och processa alla intryck och därför ”sviktar” med konfusion som resultat. Det förklarar även varför både icke-farmakologiska och farmakologiska behandlingsinterventioner kan ha effekt: Man ”hjälper” hjärnan att hantera alla intryck genom att begränsa dem.
Förvirringen kan göra det svårt för patienten att kommunicera och upprätthålla relationer. Tillståndet påverkar även förmågan att förmedla hur man mår, hur man upplever besvärande symtom och hur man vill ha det 453 454. Andelen patienter som utvecklar akut delirium minskar om tecknen på konfusion tidigt upptäcks och behandlas 450 455 456.
Det är även viktigt att kunna erbjuda avlastning för närstående i form av ett kompetent och tryggt nattvak, både i hemmiljö och i slutenvård. Risken är annars att de närstående blir utmattade av sömnbrist, och då kan situationen ytterligare förvärras 452.
Andningsbesvär
Andningsbesvär är vanligt förekommande bland patienter med palliativa vårdbehov, främst andnöd och rossel. Vid andnöd ska i första hand orsaken behandlas. Om det inte är möjligt ska symtomlindrande behandling övervägas, och den kan vara både farmakologisk och icke-farmakologisk. Vid rossel är omvårdnad ofta förstahandsåtgärd.
Definition, förekomst och orsaker
Andnöd definieras som en subjektiv upplevelse av obehag i samband med andning 457. Upplevelsen beror på ett samspel mellan flera fysiologiska, psykologiska, sociala och omgivningsmässiga faktorer. Andnöd kan uppkomma som en följd av fysiska aktiviteter, men också som en reaktion på känslomässiga upplevelser. Andnöd i vila kan försämra livskvaliteten.
Andnöd är vanligt bland exempelvis patienter med hjärt- och kärlsjukdomar redan i tidigt palliativt skede. En systematisk översikt visade att andnöd förekom hos 10–70 % av patienterna med cancer, 60–88 % av patienterna med hjärtsjukdom och 90–95 % av patienterna med KOL 458 i tidigt palliativ sjukdomsförlopp. Oavsett grundsjukdom är andnöd vanligt förkommande i livets slutskede.
I livets slutskede är det också vanligt att andningsmönstret förändras. Andningen kan vara ytlig i perioder och sedan djup, följt av andningsuppehåll (Cheyne-Stokes andning). Den kan också bli mer ansträngd när döden närmar sig. Mot slutet av livet klarar patienten inte alltid av att svälja, hosta upp slem eller vända sig, och kan då få en rosslande andning. Det rosslande ljudet beror på att slem och partiklar rör sig upp och ner i luftvägarna utan att personen kan hosta upp det. Ofta är patienten inte vid medvetande när rosslingarna uppkommer och det är osäkert om hen själv upplever det som obehagligt 381.
Bedömning, anamnes och undersökningar
Det är bara patienten själv som vet hur andningsbesvären känns, och känslan av andnöd behöver inte stämma med graden av avvikelse i mätbara parametrar (till exempel syremättnad, andningsfrekvens eller avvikelse på röntgenbilder). Andnöd är alltså en subjektiv upplevelse och bör bedömas av patienten själv, t.ex. genom strukturerad symtomskattning med IPOS, ESAS-r, VAS eller NRS. Läs mer i kapitel 14. Andnöd kan beskrivas utifrån hur intensivt den upplevs, hur ofta den uppkommer, om den endast uppstår vid ansträngning eller även i vila och hur obehagligt det känns. Kroppslig undersökning inkluderande auskultation och anamnes ger oftast viktig vägledning i bedömning av orsaken till patientens andnöd. I tidigt sjukdomsförlopp kan kompletterande provtagning såsom Hb, proBNP och kroppstemperatur ge vidare vägledning i diagnostiken.
Behandling vid andningsbesvär
I första hand eftersträvas en orsaksinriktad behandling, men om det inte är möjligt ska symtomlindrande behandling ges.
I livets absoluta slutskede är det viktigast att lindra symtomet, till exempel med omvårdnadsåtgärder och/eller extradoser opioid 459, eftersom det då sällan är meningsfullt att utreda eventuell bakomliggande orsak.
Orsaksinriktad behandling
I tidigt sjukdomsskede finns olika orsaksinriktade behandlingar, se tabell 5 nedan.
Tabell 5. Orsaksinriktade behandlingar
|
Orsak |
Överväg |
|
Pleuravätska, ascites |
Dränage, pleurodes vid återkommande pleuravätska |
|
Central bronkobstruktion |
Laser, stent, strålbehandling, ev. med initial högdos steroidbehandling |
|
Anemi |
Transfusion |
|
Lungembolier |
Antikoagulantia |
|
Infektion |
Antibiotika, antimykotika |
|
Generell obstruktivitet |
Bronkolytika (ev. med spacer eller via mask), kortison |
|
Hjärtsvikt |
Diuretika, nitrat, utsättning av intravenös vätske- och/eller näringsbehandling |
|
Smärta i bröstkorgen |
Optimerad analgetika |
|
Sekretstagnation |
Lägesändring, sekretionshämmande läkemedel, men inte sug i luftvägarna i sent palliativt skede |
|
Ångest |
Trygg och lugn vårdmiljö, psykosocialt stöd, farmakologisk behandling |
Icke-farmakologisk behandling
Omvårdnadsåtgärder
I mötet med patienter som lider av andnöd är det extra viktigt att förmedla lugn och trygghet. Andnöd skapar ofta oro och ångest, och en patient med andnöd bör därför inte lämnas ensam.
En viktig omvårdnadsåtgärd är att hjälpa patienten till en bekväm kroppsställning, till exempel genom att erbjuda elektriskt ryggstöd till sängen, lätta på åtsittande kläder eller öppna ett fönster. Beprövad erfarenhet visar att patienter med andnöd ska få sitta eller ligga enligt eget önskemål, och att kuddar under armar och i svanken kan underlätta andningsarbetet.
Många patienter med andnöd blir hjälpta av att en svag luftström från en hand- eller bordsfläkt blåser mot ansiktet 460 461. Fläkten bör hållas 15–20 cm från ansiktet och riktas mot näsa och mun. Hos patienter som får syrgas är det extra viktigt med god munvård, eftersom behandling med syrgas torkar ut slemhinnorna. Varm dryck kan kännas lindrande, men var vaksam på övervätskning. Undvik luftvägsirriterande ämnen såsom parfym och cigarettrök.
Patienter med andnöd kan behöva vila och spara energi till aktiviteter som de uppskattar och prioriterar.
Det rosslande ljudet kan upphöra genom försiktig lägesändring 462 och god munvård där munhålan torkas ren från slem. Om patienten får antikolinerga läkemedel är det viktigt att fukta munhålan med en munvårdspinne eller fuktgivande spray eftersom de läkemedlen leder till muntorrhet.
Rehabiliteringsåtgärder
Sekretstagnation och obstruktivitet kan behandlas med inhalation och motståndsandning som följs upp med ”huffing” (hosta med öppet struplock), forcerad utandning eller understödd hoststöt, anpassat till patientens ork och förmåga. Man kan också pröva att andas tillsammans med patienten för att hitta en optimal frekvens och teknik. Vidare kan man stödja andningen med sina händer runt patientens bröstkorg och följa med i bröstkorgens rörelser.
Beakta även möjlighet för positionering och viloställningar för att avlasta ansträngd muskulatur samt rollator för energibesparing.
Farmakologisk behandling
Vid rosslande andning finns ingen tydlig evidens för att farmakologisk behandling lindrar 463, men tidigt insatt behandling kan ha effekt i vissa fall.
Morfin eller annan stark opioid
Opioider i peroral eller parenteral administrering har viss dokumenterad symtomlindrande effekt mot andnöd, men för närvarande finns ingen evidens för att inhalation av nebuliserad opioid lindrar 464 465. Data från 2022 visar dock att långverkande opioid i låg dos till uppegående patienter med KOL inte har någon tydlig symtomlindrande effekt utan tvärtom kan bidra till trötthet 466.
Opioider anses inte innebära någon risk för andningssvikt med försiktig titrering för att uppnå en effektiv dos. Om patienten är opioidnaiv (inte får kontinuerlig behandling med morfin eller liknande) titrerar man fram en lindrande dos, förslagsvis i små steg från 5 mg peroralt eller 2,5 mg subkutant (morfin eller oxikodon). Vid pågående opioidbehandling, t.ex. pga. smärta, rekommenderas samma vidbehovsdos som ordinerats mot smärta.
Bensodiazepiner
Studier har visat att bensodiazepiner lindrar känslan av andnöd om patienten samtidigt har ett ångestpåslag, men de har ingen effekt på andnöden i sig 467. Lämpligt val är oxazepam som har medellång effekt, har kort tid till insättande effekt och inte innehåller aktiva metaboliter. Hos svårt sjuka patienter bör midazolam övervägas.
Syrgasbehandling
Det finns svag och delvis motsägande vetenskaplig och erfarenhetsmässig grund för att ge palliativ syrgasbehandling mot andnöd 461 468 . Syrgas bör förbehållas patienter som har påvisad syrebrist i vävnaderna (hypoxemi) och saturation < 90 % i vila, och som får en dokumenterad lindring av syrgas 469.
Loopdiuretika
Det finns en översiktsstudie av den lindrande effekten av loopdiuretika såsom furosemid vid andnöd. En del studiedeltagare upplevde god effekt av furosemid, vid både maligna och icke-maligna sjukdomar 470 .
Antikolinergika
Enligt sammanställningar av befintliga studier saknas tydlig evidens för användningen av antikolinerga läkemedel på indikation rossel i livets slutskede. Däremot kan man pröva det för vissa sjukdomstillstånd, t.ex. neurologiska sjukdomar som ger nedsatt förmåga att mobilisera sekretion i luftvägarna. Vissa patienter kan ändå vara hjälpta av läkemedel som komplement till omvårdnadsåtgärder 463 471 472. I första hand kan man pröva den antikolinerga substansen glykoperronium (Robinul), 1–2 ml subkutant vid behov max 3 gånger dagligen, i symtomlindrande syfte 473. Behandlingen bör inledas tidigt och effekten utvärderas inom några dagar. Ett alternativ till glykoperronium kan vara hyoscinbutylbromid (Buscopan) 474.
Patientmedverkan och kommunikation med patient och närstående
En kvalitativ studie visade att andnöd är ett särskilt utmanande symtom för närstående som vårdar personer med långt framskriden sjukdom i hemmet. Studien visade även att de närstående var dåligt förberedda inför akuta försämringsperioder och i många fall saknade strategier för att lindra andnöd. Professionen kan förmedla kunskaper för problemlösning utifrån den närståendes förmågor och resurser 381.
Rosslingarna brukar komma under de sista dygnen eller timmarna i livet, och är ett av många tecken på att livet närmar sig sitt slut. Var uppmärksam på att rosslande andning kan vara plågsamt för de närstående, och att de kan behöva hjälp och stöd i dessa situationer. Oftast underlättar det om de närstående får veta att patienten själv inte nödvändigtvis upplever rosslingarna som obehagliga och att farmakologisk behandling kan förvärra muntorrhet utan att göra någon direkt nytta. Vårdpersonal kan också lindra närståendes oro genom att förklara varför den rossliga andningen uppstår.
Depression
Depression är ett relativt vanligt förekommande symtom hos patienter med palliativa vårdbehov. Regelbunden screening för depressiva besvär bör ingå i rutinmässig symtomskattning. Behandlingen kan bestå av läkemedelsbehandling samtidigt som patienten stödjs med icke-farmakologiska insatser.
Definition, förekomst och orsaker
Depression är ett tillstånd med sänkt stämningsläge (nedstämdhet) samt nedsatt kognition (tankeförmåga) och funktionsförmåga, och det en av de mest vanlig förekommande psykiska hälsoproblemen.
Patienter med livshotande sjukdomar upplever oftast någon form av psykologisk stressreaktion. Studier där patienter beskriver sin symtombörda visar att en 475 476 betydande andel uppskattar sig ha en hög symtombörda för depressiva besvär. Depressiva besvär leder ofta till sämre livskvalitet och svårigheter att emotionellt hantera sociala kontakter i slutet av livet. Depression kan också förstärka andra symtom såsom smärta samt är förknippad med fler inläggningar till slutenvård och ökad risk för suicidtankar. Den kan även leda till minskad mat- och dryckesintag med undernäring som följd
Bedömning, anamnes och undersökningar
Patientens känslor av hopplöshet, hjälplöshet och skuld samt nedsatta livskvalitet bör sättas i relation till sjukdomssituationen.
Regelbunden screening för depressiva besvär bör ingå rutinmässigt i symtomskattning. Valet av skattningsskalor bör anpassas till patientens förmåga att kommunicera psykiska besvär. Frågor såsom ”har du känt dig deprimerad under stora delar av de senaste veckorna?” kan användas. Man kan även be patienten att skatta sina besvär av depression, nedstämdhet eller minskat intresse i genomförbara aktiviteter på en VAS-skala. Detta öppnar för vidare dialog om patientens psykiska mående och behov av intervention. Ett annat skattningsinstrument är MADRS-S som ger stöd i att identifiera depressiva symtom.
Andra symtom av depression såsom minskad energi, nedsatt funktionsförmåga, nedsatt aptit och kognitiv störning kan vara svåra att skilja från grundsjukdomens symtom, men man bör ta upp det med patienten om de inte korrelerar med det förväntade somatiska sjukdomsförloppet.
Kvinnligt kön, ung ålder och otillfredsställande symtomlindring (särskild smärta) anses vara riskfaktorer för depression, liksom ouppmärksammade existentiella behov och tidigare episoder av depression.
Psykiskt status
I patientens psykiska status är det viktigt att beakta
- allmänt – patientens yttre, kontakt och kognition
- motorik – mimik, psykomotorik
- emotioner – grundstämning, affekter, ångestnivå
- psykotiska symtom – exempelvis hallucinationer och vanföreställningar
- sjukdomsinsikt
- suicidalitet, se tabellen nedan.
Tabell 6. Suicidstegen
|
Tanke – handling |
Frågor |
|
Nedstämdhet |
Hur mår du? Är allt hopplöst? |
|
Dödstankar |
Känns allt meningslöst? |
|
Dödsönskan |
Har du önskat att du vore död? |
|
Suicidtankar |
Har du tänkt på att ta ditt liv? |
|
Suicidimpulser |
Har du varit nära att skada dig själv? |
|
Suicidavsikter eller planering |
När? Var? Hur? |
|
Direkt suicidhandling |
Har du försökt någon gång? När? Var? Hur? Fanns utlösande faktorer? |
I tidig palliativ sjukdomsförlopp bör man överväga att utreda eventuellt bidragande hypotyreos eller anemi. Även ytterligare sjukdomar kan öka risken för depression, såsom neuropsykiatriska funktionsdiagnoser, andra psykiatriska diagnoser och (tidigare eller pågående) skadligt bruk eller beroende av alkohol och/eller narkotika.
Behandling vid depression
Orsaksinriktad behandling
Förlust av autonomi är för många patienter en bidragande faktor till depression och upplevelse av minskad livskvalitet. Vården bör utformas på ett sätt som stöttar autonomin, tillsammans med patienten och utifrån hens önskemål om vårdåtgärder.
Depression kan också ha andra orsaker:
- Uteslut otillfredsställande symtomlindring som bidragande orsak till depression, särskilt förekomst av smärta.
- Gör en läkemedelsgenomgång. Exempelvis betablockerare, kalciumantagonister, bensodiazepiner och kortison kan bidra till ökad depression, och indikationen bör vägas mot eventuella psykiska biverkningar.
Icke-farmakologisk behandling
Om patienten uttrycker suicidala tankar bör man kontakta en enhet med kompetens i psykiatri
Omvårdnadsåtgärder, rehabiliteringsåtgärder
Vid depression kan det vara bra att tillsammans med patienten se över levnadsvanor när det till exempel gäller sömn, aktivitet och mat. Att röra på sig, ha en regelbunden sömnrytm och undvika alkohol kan ha en positiv inverkan på patientens mående 477.
För patienter med palliativa vårdbehov kan t.ex. samtalsstöd, musikterapi och akupunktur ha goda effekter på depression. Internationellt lyfts värdighetsterapi (dignity therapy) som en verksam insats. Behandlingen går ut på att uppmärksamma viktiga komponenter för upplevd värdighet i den döende människans liv, och att identifiera källor till psykosocialt och existentiellt stöd 478.
Farmakologisk behandling
- Vid förväntad överlevnad på flera veckor eller längre: Överväg insättning av antidepressiva såsom SSRI.
- Vid samtidigt förekomst av sömnstörningar kan atypiska antidepressiva såsom mirtazapin vara en fördel då mirtazapin är milt sederande.
- Vid samtidig förekomst av neuropatisk smärta kan man överväga antidepressiva såsom duloxetin.
- I sent palliativt skede kan bensodiazepiner erbjudas.
Patientmedverkan och kommunikation med patient och närstående
Trygg vårdrelation, kontinuitet och öppenhet för dialog i frågor som rör psykisk hälsa är viktigt för patienter med depression och deras närstående. Det är värt att reflektera över andra orsaker till depressionen än enbart den livshotande sjukdomen, och vid problem med den sociala situationen kan par- eller familjeterapi vara till hjälp 479 .
Diarré
Diarré kan förekomma i både tidigt och sent palliativt skede, beroende på diagnos. Det är ett symtom som är plågsamt och besvärligt för patienten, och påverkar både socialt umgänge och fysiska aktiviteter. Behandlingen styrs i första hand av misstänkt genes och patientens upplevda besvär.
Definition, förekomst och orsaker
Diarré är oftast definierat som mer än 3 lösa eller vattniga avföringar per dag. Symtomet är mer sällan förkommande än förstoppning vid palliativ vård, men förekommer särskilt i samband med vissa sjukdomar och tillstånd.
Möjliga orsaker till diarré är:
- infektion, exempelvis med Clostridioides difficile
- korttarmssyndrom (short bowel syndrome), till exempel efter omfattande tarmresektion eller vid anläggning av hög stomi
- leversvikt och exokrin pankreassvikt, som ofta kännetecknas av voluminösa, illaluktande eller fettglänsande och eventuellt ljusfärgade avföringar som är svåra att spola ner i toaletten
- fistelbildningar i tarmkanalen
- samsjuklighet, till exempel med inflammatoriska tarmsjukdomar eller celiaki
- strålbehandling med påverkan på tarmar
- neuroendokrina cancersjukdomar
- läkemedelsbiverkan.
Bedömning, anamnes och undersökningar
Patientens tidigare avföringsvanor och förekomst av subjektiva besvär bör ingå i bedömningen av behandlingsbehov. I anamnesen ingår att bedöma patogenes till diarré som led i behandlingsvalet. Rektal undersökning utförs för att utesluta fekalom eller analsfinkterinkontinens (dålig tonus i analsfinkter och/eller försämrad knipförmåga).
Bristolskalan kan användas för att bedöma avföringens konsistens och form 480.
Behandling vid diarré
Orsaksinriktad behandling
- Uteslut förstoppningsdiarré och minska laxantia med målet att åstadkomma regelbunden och för patienten tolerabel avföringsfrekvens och -konsistens.
- Ta reda på om patienten även har t.ex. inflammatoriska tarmsjukdomar, celiaki eller pankreassvikt. Om samsjukligheten anses vara bidragande orsak bör handläggningen följa behandlingsprinciperna för det aktuella tillståndet.
- Överväg antibiotikabehandling vid infektionsutlöst diarré som orsakas av exempelvis klostridieinfektion.
- Kontakta den behandlande enheten om läkemedelsbiverkan misstänks vara orsaken (t.ex. antitumoral behandling).
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Diarré kan förekomma i både tidigt och sent palliativt skede beroende på diagnos, även om det är mindre vanligt än förstoppning. 273 275. Det är ett symtom som är både plågsamt och besvärligt för patienten. En viktig åtgärd är att vätskeförlusten ersätts så att personen inte blir dehydrerad. Vid diarré kan det vara svårt att hålla avföringen, med inkontinens som följd. Det kan försvåra både socialt umgänge och fysiska aktiviteter, och patienten kan behöva hjälp med att prova ut inkontinenshjälpmedel. 276. För mobila patienter i tidig palliativ sjukdomssjukdomsförlopp kan man kontakta t.ex. en stomiterapeut för utprovning av analpropp. Se även avsnitt 13.4.7 Elimination.
Rehabiliteringsåtgärder
Bedömning och rådgivning från dietist vid intolerans eller överkänslighet för födoämnen eller malabsorptionsproblematik.
Farmakologisk behandling
I det tidiga sjukdomssjukdomsförloppet inriktas behandlingen huvudsakligen på den förmodade orsaken till diarré. Exempelvis:
- Substitution med pankreaspulver (kapsel Creon) vid tecken till pankreassvikt, 25 000–40 000 lipasenheter i samband med matintag.
- Metronidazol alternativt vankomycin för klostridieutlöst kolit (samt utsättning av förorsakande antibiotika).
- Kolestyramin vid gallmalabsorption, t.ex. 1 x 2–4 i tidigt sjukdomsskede.
- Kortison vid inflammatorisk tarmsjukdom.
- Fibergranulat i form av sterkuliagummi x 1–3 dagligen som kan påtagligt minska diarréfrekvensen och förbättra avföringens konsistens.
- Överväg tillfällig stöttning med parenteral vätska vid reversibel orsak till diarré i det tidiga sjukdomssjukdomsförloppet.
- Undvik motilitetshöjande läkemedelsbehandling om patienten samtidigt har illamående, t.ex. metoklopramid.
- Överväg loperamid 2 mg x 2 vid behov.
- Överväg opioider i låg dos (för i övrigt opioidnaiva patienter), t.ex. opiumtinktur eller låg dos morfin.
- Överväg ondansetron peroralt eller intravenöst pga. dess förstoppande bieffekt. (OBS denna behandling är kontraindicerad vid neuroendokrina tumörer.)
- I svåra fall kan man överväga tillägg av oktreotid 100–200 mikrogram x 3 subkutant.
Patientmedverkan och kommunikation med patient och närstående
Det är viktigt att tillsammans med patienten finna strategier för att hen ska kunna upprätthålla meningsfulla aktiviteter och sociala kontakter. Patienten behöver också rådgivning och tillgång till inkontinenshjälpmedel, t.ex. via distriktssköterska.
Fatigue
Fatigue är ett av de vanligaste symtomen vid avancerad sjukdom. Det beskrivs ofta som en subjektiv fysisk eller mentalt dränerande, oövervinnerlig känsla av utmattning och/eller trötthet som påverkar livet och förmågan att utföra dagliga aktiviteter.
Definition, förekomst och orsaker
Det är en trötthetsupplevelse som inte går att vila bort 294. Många patienter berättar inte för hälso- och sjukvårdspersonal om denna känsla. Det kan bero på vilken information patienten får, och om vårdpersonalen inte pratar om fatigue kan patienten uppfatta att det inte är viktigt. Patienten kan också bli orolig för att den utbredda tröttheten beror på progress av sjukdomen.
Upplevelsen och påverkan av fatigue kan variera beroende på var i sjukdomsprocessen patienten befinner sig. I ett tidigt palliativt sjukdomsförlopp kan tillståndet ha en större negativ inverkan på det dagliga livet och livskvaliteten än i ett sent skede. Känslan kan också variera från dag till dag, eller till och med under samma dag. Tilltagande fatigue är vanligt förekommande när en person närmar sig livets slutskede 481.
Bedömning, anamnes och undersökningar
Fatigue är en subjektiv upplevelse och bör alltså bedömas av patienten själv. På svenska används ofta ordet trötthet, men det är viktigt att notera hur patienten själv pratar om sin situation. Samtala om och bedöm fatigue på ett systematiskt sätt. Ställ frågor såsom: ”Upplever du någon trötthet? Om ja, hur svår har den varit i genomsnitt under den senaste veckan? Hur påverkar tröttheten din förmåga att fungera?”.
Fatigue eller trötthet ingår i skattningsskalor såsom ESAS-r och IPOS. Det går också att göra ytterligare utredning med ett fatiguespecifikt instrument såsom Functional Assessment of Chronic Illness Therapy – Fatigue Scale (FACIT-F). Det finns ingen klarlagd behandlingsstrategi utan behandlingen är ofta symtomatisk [294, 314, 482].
Behandling vid fatigue
Orsaksinriktad behandling
Oftast behövs en individanpassad behandling eftersom orsaken till fatigue i regel är komplex och det varierar vilka faktorer som bidrar. Både icke-farmakologiska och farmakologiska behandlingar kan prövas och kombineras.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Icke-farmakologisk intervention kan vara att sjuksköterskan ger information om symtomet, inklusive orsak och hanteringsstrategier. Patienten kan också föra dagbok för att undersöka om det finns mönster i tröttheten. Vidare behövs nutritionsråd om hen har svårt att äta och befinner sig i tidig palliativ sjukdomsförlopp. Psykosocialt stöd kan ge minskad fatigue men det saknas tydlig evidens.
Rehabiliteringsåtgärder
Fysisk aktivitet och träning har visat god effekt vid avancerad cancer. Vid palliativ vård behöver omfattningen och intensiteten anpassas till patientens förmåga och vanor. Regelbunden aktivitet ger tydligast effekt 483, och korta vilopauser under dagen kan ge mer ork och skapa en balans mellan aktivitet och vila. Akupunktur har även visats ha god effekt 484.
Farmakologisk behandling
Farmakologiska interventioner har testats men den samlade evidensen är relativt svag. Vid cancerrelaterad fatigue föreslås i första hand kortison i korta behandlingsperioder 222 294 485. I vissa situationer, till exempel inför en viktig familjehögtid, kan man överväga en boosterdos kortison under överinseende och ordination av läkare. Undersök även om patienten har anemi, hypotyreos, elektrolytrubbning, infektion eller depression eftersom dessa behandlingsbara tillstånd bidrar till fatigue. Behandling av vitamin D-brist har visats kunna minska fatigue hos patienter med spridd cancersjukdom 191. Låga nivåer av vitamin D i blodet; 25-hydroxivitamin D i nivåer <50 nmol/L har också visat sig vara associerat med fatigue 486 487.
Patientmedverkan och kommunikation med patient och närstående
Patienten och de närstående bör få information om vad fatigue beror på och ifall åtgärder som rör motion och kost kan bidra till minskade symtom.
Feber och svettningar
Feber och svettningar förekommer i både tidigt och sent palliativt skede, och är ofta orsakat av patientens sjukdom eller en infektion. Feber i sent palliativt skede kan bero på dysfunktion i det centrala nervsystemet. Vid feber och svettningar behandlas den bakomliggande orsaken när det är möjligt, i kombination med symtomlindrande icke-farmakologisk och farmakologisk behandling.
Definition, förekomst och orsaker
Svettningar är en normal kroppsreaktion med syftet att upprätthålla optimal kroppstemperatur. Onormalt starka svettningar, framför allt nattetid, som inte uppfyller detta syfte är vanligt förekommande vid avancerad cancersjukdom, särskilt vid lymfom.
Besvärande svettningar förekommer även vid infektion, hypertyreos och menopaus, vid endokrina sjukdomar såsom diabetes mellitus, vid neurologisk skada såsom komplext regionalt smärtsyndrom eller efter stroke (fokala svettningar i nervskadat område). Andra orsaker är alkoholkonsumtion och läkemedelsbiverkning, exempelvis SSRI-preparat och hormonbehandling vid till exempel bröst- och prostatacancer.
Feber kan ha flera orsaker hos patienter vid palliativ vård. Feber till följd av pågående infektion kan och ska i vissa fall utredas och behandlas, vilket är ett medicinskt beslut. Feber utan infektiös genes, så kallad hypertermi, är vanlig i sent palliativt skede och kan ha paramaligna orsaker eller bero på dysfunktion i centrala nervsystemet, läkemedelspåverkan eller inflammatoriska processer 488 489.
Bedömning, anamnes och undersökningar
En utredning av bakomliggande orsaker, samt eventuell påverkan på patientens välmående, bör ligga till grund för utredning och behandling. Vid nattliga svettningar blir nattsömnen störd och patienten behöver byte av säng- och nattkläder, vilket bör uppmärksammas i bedömningen av vilken behandling som ska erbjudas.
Behandling vid feber och svettningar
Orsaksinriktad behandling
I tidig palliativ sjukdomssjukdomsförlopp, när symtomen inte indikerar progress i hematologisk eller annan malign sjukdom, kan man utreda och behandla den underliggande orsaken, till exempel infektion eller hypertyreos.
Sätt ut eller byt eventuella läkemedel som misstänkts ge upphov till svettning om det bedöms vara lämpligt.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Omvårdnadsåtgärder vid feber och svettningar kan vara att svalka av patienten med fuktig handduk, hålla rummet svalt och luftigt, varsamt tvätta kroppen, bädda i sängen med svalare sängkläder och erbjuda vätska och frekvent munvård. Rikliga nattliga svettningar kan kräva frekvent byte av kläder och sänglakan nattetid. Var uppmärksam på störd nattsömn med trötthet som följd.
En patient i sent palliativt skede kan ha svårt att förmedla sina behov, och det är därför viktigt att uppmärksamma tecken på att patienten fryser eller känner sig varm, och att vidta åtgärder därefter.
Rehabiliteringsåtgärder
Vid svettningar och vallningar orsakade av endokrinbehandling vid bröst- eller prostatacancer eller menopaus till följd av operation vid gyncancer har akupunktur visat god effekt 484.
Farmakologisk behandling
Feber och svettningar kan behandlas med:
- paracetamol eller NSAID (som dock också kan ge upphov till svettningar)
- prednisolon initialt 0,5–1 mg/kg kroppsvikt eller motsvarande betametason, med utvärdering av försökets effekt inom några få dagar
- amitriptylin, gabapentin och olanzapin, även om det saknas vetenskapligt underlag för effekt och dosförslag. (Amitriptylin kan också ge upphov till svettningar).
Ifrågasätt eventuell plåsterbehandling vid kraftig svettning och/eller feber eftersom det finns risk för förändrat läkemedelsupptag genom huden.
Patientmedverkan och kommunikation med patient och närstående
Informera patienten och de närstående ifall svettningar bedöms bero på grundsjukdomen snarare än en infektion, och varför infektionsbehandling i så fall ska sättas ut eller inte sättas in. I sent palliativt skede kan dysfunktion i centrala nervsystemet orsaka feber. Då är det viktigt att informera närstående om att det är en normal process, som inte beror på infektion eller annan behandlingsbar orsak, och att febernedsättande läkemedel sällan är effektiva i detta skede 490 .
Hicka
Hicka förkommer inom palliativ vård, och kan orsaka ett stort lidande för patienten. Återkommande och långvarig hicka påverkar patientens livskvalitet genom bland annat försämrad sömn, ätsvårigheter och smärta. I första hand behandlas den bakomliggande orsaken till hickan, samtidigt som omvårdnadsåtgärder och läkemedel kan ge lindring. Ofta utvecklar patienten strategier för att hantera hickan.
Definition, förekomst och orsaker
Hicka definieras som en okontrollerad spasm i diafragmamuskeln mellan ordinarie andetag. Upp till var tionde patient med avancerad cancer besväras av återkommande hicka, medan det är ännu vanligare vid t.ex. esofaguscancer 491.
Hicka kan bero på lokal irritation av diafragma, nervus frenicus eller nervus vagus. Den kan även orsakas av skador eller sjukdomar i CNS, se tabell 7.
Tabell 7. Exempel på orsaker
|
Organ |
Sjukdom |
|
Hjärta |
Perikardit, hjärtinfarkt |
|
Lungor |
Pleurit, pneumoni, lungcancer, sarkoidos |
|
Ventrikel |
Gastrit, ulcus, hiatushernia, ventrikelretention |
|
Mag-tarm |
Peritonit, subfrenisk abscess, pankreatit, voluminösa levermetastaser eller buktumörer |
|
CNS |
Trombos i basala hjärnartärer, infarkt i hjärnstam, hjärnblödning, andra lesioner i CNS t.ex. hjärntumör eller MS |
Elektrolytrubbningar (t.ex. hypokalemi, hypokalcemi) anses vara en bidragande orsak, liksom hyperventilation eller läkemedelsbiverkan av t.ex. vissa cytostatika eller antiemetika.
Bedömning, anamnes och undersökningar
Anamnes med misstänkt bidragande genes enligt ovan. I undersökningsstatus ingår bukpalpation. Beakta att långvarig hicka kan påverka allmäntillståndet genom att orsaka utmattning. Det kan även påverka lusten och förmågan att äta, och därigenom leda till försämrad nutritionsstatus.
Behandling vid hicka
Orsaksinriktad behandling
Vid kraftigt utspänd ventrikel, överväg insättning av läkemedel eller avlastning med till exempel ventrikelsond.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Vid hicka i samband med palliativ vård bör bakomliggande orsaker utredas och åtgärdas. Omvårdnadsåtgärder kan användas separat eller i kombination med läkemedelsbehandling. Det kan vara svårt att häva hickan, men det finns några åtgärder som kan provas:
- Bryt andningscykeln genom att t.ex. hålla andan eller utföra en valsalvamanöver (tryckutjämning genom att hålla för näsan och med stängd mun ”blåsa ut”).
- Reta nasofarynx genom att t.ex. dricka vatten eller dra i tungan.
- Undvik att reta diafragman. Det kan vara retande att exempelvis sitta framåtlutad eller ha knäna uppdragna mot bröstet 491.
Ett annat tillvägagångssätt enligt praktisk erfarenhet är att stimulera tungroten med en mjuk kateter eller rundad spatel i några sekunder 492. Förvarna patienten om att det kommer utlösa kräkreflex, och hjälp patienten efter manövern att ligga stilla och andas lugnt i cirka 20 minuter. Denna åtgärd bör endast utföras av personer som är väl förtrogna med uppgiften.
Farmakologisk behandling
493Evidensen för farmakologisk behandling är mycket låg. Vid besvärande hicka och utebliven effekt av omvårdnadsåtgärder styrs behandlingen av misstänkt genes, erfarenhet och andra symtom. Någon av följande behandlingar kan övervägas:
- metoklopramid om det inte finns något mekaniskt hinder, t.ex. peroralt 10 mg x 3 alternativt intravenös injektion 5 mg/ml, och 2 ml vid behov
- protonpumpshämmare
- haloperidol peroralt 1 mg x 2–3 alternativt subkutan injektion 1 mg x 2
- betametason främst vid CNS-utlöst hicka, exempelvis Betapred peroralt 0,5 mg, 16 x 1 i engångsdos
- baklofen peroralt 5–20 mg x 3
- gabapentin i låg dos, förslagsvis 100 mg x 2–3
- Hyoscinbutylbromid (Buscopan)eller octreotid (Sandostatin) kan ibland provas för lugnande effekt vid total ileus (ofta specialistnivå).
- Vid tumörväxt i anslutning till diafragma kan avsvällande cortison provas t.ex T Betapred 0,5 mg 12–16 x 1.
I sent palliativt skede kan midazolam ha god effekt genom avslappnande verkan 491.
Patientmedverkan och kommunikation med patient och närstående
Patienter med återkommande hicka har ofta utarbetat egna metoder för att stoppa eller lindra besvären, och deras erfarenheter bör därför ligga till grund för eventuella åtgärder 491.
Illamående och kräkningar
Illamående och/eller kräkningar är vanligt hos patienter med palliativa vårdbehov. Orsaken är ofta multifaktoriell, och olika receptorer är inblandade. Det är viktigt med noggrann anamnes, status och eventuellt laboratorieprover och radiologi för att fastställa orsaken. Om orsaken till illamåendet inte kan identifieras bör behandlingen vara symtomatisk. Vid ospecifikt illamående av oklart ursprung kan behandlingen inledas med en dopaminreceptorantagonist, och haloperidol eller metoklopramid är förstahandsalternativ.
Definition, förekomst och orsaker
Illamående är ett vanligt och besvärande symtom hos patienter i ett palliativt sjukdomsskede. Det drabbar ungefär hälften av cancerpatienterna under de sista levnadsmånaderna, men är även vanligt vid svår hjärtsvikt och njursvikt. Illamående är vanligare hos kvinnor än män och drabbar oftare yngre än äldre.
Orsaken är ofta multifaktoriell, och i utredningen är det viktigt med en utförlig anamnes, status och oftast laboratorieprover. Målet är att hitta behandlingsbara orsaker och få en bas för att välja rätt antiemetika.
Det finns få kontrollerade studier som rör effekten av antiemetikabehandling vid avancerad cancersjukdom, vilket gör att evidensen för behandlingsrekommendationen är svag. Den kliniska erfarenheten av olika läkemedel mot illamående är däremot stor.
Fysiologiska mekanismer
Kräkcentrum är lokaliserat till hjärnstammen och fungerar som ett fysiologiskt kontrollcentrum vid illamående och kräkningar. Hit kommer impulser från fyra olika områden:
- gastrointestinalkanalen
- kemoreceptortriggerzonen (CTZ) i botten på fjärde ventrikeln; den reagerar på toxiner i både blodet och cerebrospinalvätskan
- vestibulära afferenter som är kopplade till balanssinnet
- högre hjärncentrum som aktiveras av oro och ångest, starka känslor, smärta, synintryck samt smak och lukt.
I vart och ett av dessa områden finns receptorer som stimuleras och skickar impulser till kräkcentrum. Ett svagt stimuli leder till ett lätt illamående, och ett starkt stimuli framkallar kräkning. Grundtanken vid läkemedelsbehandling av illamående är att genom anamnes och status förstå vilket eller vilka av dessa fyra områden som skickar impulser. Därefter väljer man det läkemedel som påverkar receptorerna i detta område:
- gastrointestinalkanalen – D2, 5HT4, 5HT3
- kemoreceptortriggerzonen – D2, 5HT3
- vestibulära afferenter – Ach, H1
- högre hjärncentrum – GABA.
Bedömning, anamnes och undersökningar
Utredning av illamående vid palliativ vård består av anamnes, status, handläggning vid utredning och provtagning.
Anamnes
Bedöm i anamnesen om det enbart är illamående eller också kräkning som besvärar patienten, samt karaktären på besvären.
- Illamående
- Är det ständigt pågående eller kommer det och går?
- Svårighetsgrad med VAS eller NRS?
- Koppling till måltid?
i) Bättre av måltid – bakomliggande gastrit eller ulcus?
ii) Sämre av måltid – möjlig ventrikelretention? - Dygnsvariation?
- Samtidig smärta, förstoppning, yrsel, ångest, nyinsatta läkemedel?
- Kräkning
- Vad består kräkningen av?
iii) Den senaste måltiden – trolig ventrikelretention. - Lättar illamåendet efter kräkning?
iv) Om ja – trolig ventrikelretention, nedsatt tarmmotorik.
v) Om nej – troligen illamående som utlösts från kemoreceptortriggerzonen.
- Vad består kräkningen av?
Status
I patientens status ingår:
- allmäntillstånd – uttorkning, ikterus
- munhåla – munhygien, svamp, mycket slem
- buk – ömhet, organförstoring, ascites, tarmljud
- ev. palpation per rektum – förstoppning
- neurologiskt status – balansstörning
- psykiskt status – oro, ångest.
Handläggning vid utredning
- Ta genom anamnes och status reda på sannolik bakomliggande orsak till illamåendet.
- Gå igenom läkemedelslistan. Har det tillkommit något nytt läkemedel eller skett en dosändring? Är det något läkemedel som bör sättas ut?
- Överväg provtagning.
Provtagningar
Provtagningar kan omfatta:
- riktad blodprovstagning för att utesluta infektion och metabol påverkan, exempelvis CRP, elektrolytstatus inklusive kalcium, B-glukos och eventuellt leverstatus
- njurfunktion, såsom eGFR och kreatinin.
Behandling av illamående
Behandling av illamående vid palliativ vård bör omfatta följande:
- Åtgärda om möjligt bakomliggande orsak, till exempel förstoppning, oral candida, hyperkalcemi, reflux eller infektion.
- Ta ställning till icke-farmakologiska behandlingsmöjligheter.
- Grunda läkemedelsbehandling på receptorprofilen i det aktiverade området.
- Om flera antiemetika används, se till att de har olika angreppspunkter.
- Ta kontakt med ett specialiserat palliativt team om patienten har kvarstående illamående trots behandlingsförsök.
Orsaksinriktad behandling
När det är möjligt och lämpligt ska orsaksinriktad behandling kombineras med icke-farmakologisk och/eller farmakologisk behandling.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Omvårdnadsåtgärder kan ha god effekt på illamående. En del av dessa är enbart erfarenhetsbaserade och kan prövas och utvärderas. Besvären kan exempelvis förebyggas om patienten serveras små men attraktiva matportioner som hen själv väljer. Vid kräkningar eller illamående som hindrar patienten från att äta eller dricka kan det vara aktuellt att övervaka patientens intag av vätska med till exempel en vätskelista. Vid kakexi ökar illamåendet ofta av fet mat, och mat och dryck kan behöva individanpassas. Hos en del kan vissa dofter, som t.ex. matos, utlösa illamående och bör då försöka elimineras 494. Illamåendet kan vara lägesberoende och kan i så fall förbättras av lägesändring, eller av att vissa lägen undviks. Vid illamående och kräkningar är det viktigt med god munvård. Att borsta tänderna efter att ha kräkts kan förvärra skadorna då det sker både kemikalisk och mekanisk avverkning av emalj. För bättre smak i munnen kan patienten använda sockerfritt tuggummi, sugtablett eller munskölj – gärna med fluorid. En nedsatt munhälsa kan också orsaka eller förvärra ett illamående.
Rehabåtgärder
Massage, TENS, akupunktur och akupressur kan vara av värde för vissa patienter 495 496 497. Illamåendet kan vara lägesberoende och kan i så fall förbättras av lägesändring, eller av att vissa lägen undviks.
Farmakologisk behandling
Läkemedelsbehandling behövs när det inte är möjligt att åtgärda den bakomliggande orsaken och icke-farmakologisk behandling är otillräcklig. Välj läkemedel baserat på den receptor eller de receptorer som stimuleras och skickar impulser till kräkcentrum 498 499, alltså utifrån dessa fyra områden:
- Gastrointestinalkanalen – försämrad eller upphävd ventrikel- eller tarmpassage och motorik är en vanlig orsak till illamående. Illamåendet är ofta intermittent och lindras av kräkning. Det kan också handla om tryck från omgivande organ, ascites, infektion, retning (gastrit) eller skada.
- Aktuella receptorer: D2, 5HT4, 5HT3.
- Förstahandsval: metoklopramid 10 mg x 3 som tablett eller subkutan injektion, gärna 30 minuter före måltid. Undvik metoklopramid vid mekaniskt ileus.
- Andrahandsval: haloperidol 0,5–1 mg x 2 som tablett eller subkutan injektion.
- Övriga läkemedel:
vi) Ondansetron 4 – 8 mg x 2 används tillsammans med andra läkemedel vid illamående som är utlöst av cytostatika- eller strålbehandling.
vii) Vid tumörorsakad svullnad ges betametason 4–8 mg x 1.
- Kemoreceptortriggerzonen – illamående på grund av ”gifter” är en vanlig orsak till illamående. Illamåendet är ofta konstant och lindras inte av kräkning.
- Aktuella receptorer: D2, 5HT3
- Förstahandsval: haloperidol 0,5–1 mg x 2 som tablett eller subkutan injektion
- Andrahandsval: olanzapin 2,5–5 mg x 1 som tablett
- Övriga läkemedel:
i) Ondansetron 4 – 8 mg x 2 används tillsammans med andra läkemedel vid illamående som är utlöst av cytostatika- eller strålbehandling.
- Vestibulära afferenter – illamående som utlöses av rörelse. Förekommer också vid nyinsatt opioidbehandling.
- Aktuella receptorer: Ach, H1
- Förstahandsval: meklozin 25 mg x 2 som tablett
- Andrahandsval: olanzapin 2,5–5 mg x 1 som tablett
- Tredjehandsval: hyoscin som plåster, byts efter 72 timmar.
- Högre hjärncentrum – illamående som är kopplat till oro och ångest, starka känslor, smärta, synintryck samt smak och lukt. Förekommer även vid hjärnödem.
- Aktuella receptorer: GABA
- Förstahandsval vid hjärnödem: betametason i högdos
- Förstahandsval vid ångest: oxazepam 5–10 mg som tablett vid behov.
Utvärdera och justera behandlingen vid behov.
Opioidutlöst illamående
Vid insättning av opioider får cirka 25 % av patienterna besvär av illamående. Risken för att drabbas är större för yngre personer och uppegående personer, och kvinnor drabbas i högre grad än män. Som profylax ges i första hand meklozin 25 mg x 2, men även metoklopramid och haloperidol fungerar. Tolerans mot illamående utvecklas inom 7–10 dagar. Efter det kan man avsluta kontinuerlig behandling och sätta upp preparatet på vidbehovslistan.
Illamående med oklar genes
Vid ospecifikt illamående av oklar genes kan behandlingen inledas med en dopaminreceptorantagonist- haloperidol eller metoklopramid.
Patientmedverkan och kommunikation med patient och närstående
Informera patienten om förmodad orsak till illamåendet, och utvärdera den insatta behandlingen tillsammans med patienten och de närstående.
Klåda
Klåda är en obehaglig upplevelse som genererar en reflex att riva i huden. Behandlingen består i första hand av att försöka minska utlösande faktorer, i kombination med omvårdnadsåtgärder. Farmakologisk behandling kan prövas men har låg evidens.
Definition, förekomst och orsaker
Klåda är ett relativt ovanligt symtom inom palliativ vård men kan vid bestående besvär påverka patientens livskvalitet mycket negativt, t.ex. genom störd nattsömn 500. Klådan kan ha många olika orsaker, och är inom den palliativa vården inte sällan multifaktoriell.
Vanligt förekommande utlösande faktorer kan vara:
- bakomliggande hudproblem såsom torr hud, atopi, neurodermatit eller eksem samt svampinfektion och skabb
- allergiska tillstånd såsom läkemedelsreaktioner med exantem eller nässelutslag
- läkemedelsbiverkan, till exempel av morfin, molekulär målstyrd onkologisk behandling, penicillin, trimetoprim statiner och NSAID
- endogena metabola sjukdomar såsom njur- och leversvikt och gallstas med ikterus
- infektion såsom hiv eller aids
- cancersjukdom med paramalign klåda, särskilt blodsjukdomar såsom polycytemia vera, leukemi, myelom och lymfom
- psykiatriska och psykosomatiska tillstånd såsom stress, ångest och depression.
Bedömning, anamnes och undersökningar
I anamnesen bör man beakta:
- känd cancersjukdom
- klåda som eventuell komplikation till grundsjukdom
- nyinsatta läkemedel
- duration och utveckling av klådan
- andra nytillkomna symtom.
Vid undersökning utförs palpation av buk (lever, mjälte) och lymfkörtlar. I samband med undersökning inspekteras även huden avseende hudförändringar, rivmärken och ikterus. Bedömning görs även av patientens allmäntillstånd och psykiska status.
Behandling vid klåda
- Handlägg utifrån bakomliggande känd grundsjukdom alternativt lokal dermatologisk orsak.
- Bedöm om klådan är av akut eller kronisk karaktär.
- Gör en genomgång av patientens läkemedel.
- Överväg kompletterande laboratorieprover.
Orsaksinriktad behandling
Behandla om möjligt orsaken, till exempel hudsjukdom, olämpligt läkemedel eller gallvägsstas. Vid mycket besvärande och behandlingsresistent klåda, överväg remiss till en enhet med kompetens i specialiserad palliativ vård. Behandlingsförsök med lågdos propofol kan övervägas.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Oavsett klådans orsak är allmän hudvård en grundläggande del av behandlingen. Beroende på orsaken kan omvårdnadsåtgärder innefatta regelbunden inspektion av huden, smörjning med mjukgörande och återfuktande hudsalva eller applicering av kylbalsam. Tvål bör vara parfymfri och användas sparsamt eller inte alls, och uttorkande hudprodukter bör undvikas. Det kan också upplevas lindrande att bära svala, luftiga kläder och hålla rummet svalt 500.
Farmakologisk behandling
Vid klåda med oklar orsak, eller när den utlösande sjukdomen eller orsaken inte kan behandlas, kan man överväga behandlingarna som beskrivs nedan. Evidensen för lokal och systemiskt farmakologisk behandling är dock svag, eftersom det saknas jämförande studier. I palliativ vård är klåda oftast multifaktoriell och sällan förorsakad av histaminutsöndring, vilket gör att behandling med antihistaminika sällan har effekt.
Lokal behandling
- Ge mjukgörande och klådstillande kräm eller salva, eventuellt grupp 3steroid vid förekomst av inflammatoriska hudförändringar.
- Överväg att behandla lokal klåda utan tecken till inflammation med lokalanestesika i form av kräm eller salva (t.ex. prilokain och lidokain)
Systematisk behandling
Om lokal behandling inte räcker bör man fundera över vilka mekanismer och pruritogener som kan vara aktuella. Detta underlättar val av behandlingsstrategi. Effekt av farmakologisk behandling kan oftast utvärderas efter 1–2 dygn, vilket tillåter snabba byten vid hög symtombörda och avsaknad av effekt. Evidensen för farmakologisk behandling är generellt låg 501.
Tabell 8. Läkemedelsbehandling vid olika typer av klåda
|
Typ av klåda |
Läkemedelsbehandling |
|
Urtikaria |
Tablett antihistamin. Vid kraftigare reaktion, tillägg med kortikosteroid peroralt. |
|
Klåda vid uremi |
Prova låg dos gabapentin 501. |
|
Klåda vid ej åtgärdbar kolestas |
Sertralin. eventuellt naltrexon peroralt |
|
Opioidutlöst klåda |
Prova opioidrotation i första hand, i andra hand tillägg av gabapentin i låg dos |
|
Nattlig klåda |
Tablett hydroxizin alternativt klemastin, men beakta risk för antikolinerga biverkningar i palliativ situation. Tablett levomepromazin till natten. Bensodiazepiner med ofta sinsemellan likvärdig effekt. |
|
Paramalign klåda |
Histamin är sällan mediator vid denna typ av klåda, så man får ofta prova alternativa läkemedel utan evidens: tablett paroxetin tablett sertralin tablett mirtazapin tablett gabapentin tablett prednisolon 30–40 mg dagligen för klåda vid hematologisk malignitet. |
Patientmedverkan och kommunikation med patient och närstående
Patienten kan själv lindra sin klåda genom att generellt vårda huden, undvika irriterande hudprodukter och använda återfuktande hudsalva. Uppmana patienten att inte riva på huden, hålla fingernaglarna kortklippta och eventuellt bära tunna bomullshandskar.
Uppmuntra patienten att ägna sig åt självvalda och meningsfulla aktiviteter för att distrahera sig från klådan.
Munhälsobesvär
Munhälsobesvär är vanligt förkommande i både tidigt och sent palliativt skede. Dålig munhälsa kan påverka patienten både socialt och funktionellt. Särskilt under livets slutskede kan patienten förlora förmågan att själv ta hand om sin munhälsa och uttrycka sina besvär, så munvård och bedömning av munhälsan är en viktig del av den palliativa vården 502.
Definition, förekomst och orsaker
Flera olika munhälsobesvär är vanliga vid palliativ vård, bland annat muntorrhet, svampinfektioner, sväljsvårigheter, smakförändringar, smärta, sår och dålig andedräkt. Det är också vanligt att få problem med tandproteser, t.ex. till följd av viktnedgång 502.
Besvär med munhälsan kan orsakas av viss medicinering och behandling, t.ex. strålbehandling. Läkemedel kan leda till muntorrhet, karies och tandlossning. Nedsatt förmåga att sköta den egna munhygienen kan också påverka munhälsan. Andning med öppen mun orsakar muntorrhet och förekomst av krustor, framför allt i livets slutskede 502. Patienter som får artificiell näringstillförsel kan ha en högre risk för dålig munhälsa jämfört med de som kan äta 503.
Dålig munhälsa kan påverka patienten både socialt och funktionellt. Patienten kan känna skam och oro eller vilja isolera sig till följd av dålig munhälsa. Funktionellt kan det ge sämre förmåga att svälja och tala, samt styra vilken typ av mat patienten kan äta. Detta kan leda till minskad matlust och förmåga att njuta av maten 502.
Bedömning, anamnes och undersökningar
För att bedöma munhälsa hos vuxna används riskbedömningsinstrumentet ROAG (Revised Oral Assessment Guide), som omfattar röst, munslemhinna, tunga, tänder, implantat, proteser, saliv och sväljning. Syftet med bedömningen är att identifiera problem i munnen och tydliggöra behov av munvårdsåtgärder 504.
Under livets slutskede kan det ses som oetiskt att göra en full bedömning enligt ROAG, och en mindre omfattande bedömning kan då utföras i stället. Detta innebär att man regelbundet tittar efter rodnader, sår, sprickor, svamp eller andra synliga besvär i mun och svalg, samt på läppar och i munvinklar.
Behandling vid munhälsobesvär
Orsaksinriktad behandling
I ett tidigt palliativt skede kan kontakt tas med tandvården för stöd och hjälp till en god munhälsa. Tandvården kan vara behjälplig vid till exempel dåligt sittande proteser, problem med karies eller tandlossning.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Om patienten upplever törst kan hen erbjudas att suga på små isbitar eller iskuber smaksatta med mintsirap 505. Att använda läppcerat med mentol eller kallt vatten i sprayflaska kan också motverka törstkänsla, förutsatt att patienten är bekväm med detta 505. För patienter som har smärta i munnen kan det hjälpa att undvika t.ex. starkt kryddad mat. Se även avsnitt 13.5.2.3 Munhälsoproblem.
I ett sent palliativt skede är det vanligt att vårdpersonal eller närstående behöver hjälpa patienten med regelbunden munvård. Om patienten är medvetandesänkt behöver munnen torkas ur och fuktas regelbundet, gärna med vichyvatten eller matolja. Man kan även använda återfuktande och mjukgörande spray eller olja om munnen är torr, samt återfukta läpparna med smörjande cerat 505, 506.
Tänk på att utfärda underlag för Nödvändig tandvård. Intyget ger rätt till ett kostnadsfritt hembesök från tandhygienist med särskild anpassade råd och instruktioner. Ofta finns även möjlighet att få viss nödvändig tandvård utförd i hemmet.
Farmakologisk behandling
Följande behandling kan ha effekt mot muntorrhet: 493507
- Vid kvarvarande funktion i körtelvävnaden är salivstimulerande medel förstahandsalternativ. Preparat som innehåller buffrad äppelsyra och fluorier har här ett användningsområde (Xerodent). Saliversättningsmedel med natriumfluorid apotek produktion och laboratorier (APL), munhålelösning 0,02 % finns att förskriva till patienter vid muntorrhet (vuxna och barn > 12 år).
- Övriga receptfria oljebaserad spray, mungel, sugtabletter. Erbjud patienten försök utifrån hens egna preferenser.
- Viss evidens finns för behandling med pilokarpin för patienter med svår muntorrhet som är relaterad till biverkningar av strålbehandling eller Sjögrens syndrom.
Följande behandling kan ha effekt mot mukosit och smärta:
- prostaglandinsynteshämmare med lokal anestetikum: t.ex. bensydamin munskölj 15 ml vid behov var 1,5–3 timme
- lokala anestetika: lidokain, munskölj med krossad paracetamol ev. med tillägg av 0,5–1 krossad morfintablett, t.ex. blandad i grädde; finns även receptfria sugtabletter som blandar klorhexidin och lidokain.
Följande behandling kan ha effekt vid infektion:
- Vid oral candidiasis: nystatin-suspension 1 ml (100 000 E) x 4 dagligen i 1–2 veckor, kan förlängas till 1–2 veckor vid nedsatt immunförsvar.
- Vid svår svampinfektion i munhåla eller misstanke om candida i svalg och esofagus, överväg tidigt systemisk behandling peroralt med flukonazol, t.ex. 100 mg (ev. 100–200 mg) x 1 i 7 dagar, men var observant på interaktioner.
Patientmedverkan och kommunikation med patient och närstående
Munvård är en omvårdnadsåtgärd som de närstående ofta kan hjälpa till med, vid vård i livets slutskede. Personalen behöver då stötta och eventuellt instruera dem i utförandet.
Obstipation
Obstipation, eller förstoppning, är det vanligaste mag- och tarmproblemet inom palliativ vård. Under livets sista dagar, när patienten kanske inte längre kan eller orkar kommunicera, kan förstoppning orsaka motorisk oro. Ofta behövs laxerande behandling i kombination med behandling av bakomliggande orsaker. Förebyggande åtgärder är grundläggande vid till exempel opioidbehandling.
Definition, förekomst och orsaker
Förstoppning definieras som att ha lång tid mellan tarmtömningar och/eller problem med själva tömningen av tarmen, till exempel överdriven krystning, hård avföring eller känsla av ofullständig tarmtömning. Det är vanligt förkommande inom palliativ vård 508.
För patienter inom palliativ vård är orsaken till obstipation oftast multifaktoriell. Vanliga bidragande och bakomliggande orsaker är immobilisering, läkemedel som minskar tarmens rörelser (opioider, antikolinergika, diuretika), metabola orsaker såsom hyperkalcemi eller hypotyreos, minskat peroralt intag eller obstruktion i eller nära tarmen (tumör).
Bedömning, anamnes och undersökningar
Obstipation kan förorsaka eller bidra till nedsatt aptit, illamående och kräkning, smärta vid tarmtömning, förstoppningsdiarré, blåstömningsbesvär, buksmärta och oro.
I anamnesen ingår:
- avföringsvanor både som frisk och under senaste tiden, inklusive frekvens, smärta och konsistens
- senaste avföringen med tidpunkt, mängd och utseende; bedömning med Bristolskalan kan vara till hjälp 480
- bakomliggande orsaker, särskilt opioidbehandling
- miktionsvanor såsom eventuell urinretention och kateteranvändning.
Efterhör patientens följsamhet till tidigare ordinerade laxantia innan dosen ökas.
Undersökningar som bör ingå i utredningen är bukpalpation för resistenser i tarm och urinblåsa, samt rektalpalpation för att utesluta fekalom i ändtarmen.
Handläggning vid utredning
- Gå igenom patientens kost och medicinering.
- Följ patentens tarm- och urinproduktion regelbundet.
- Vid misstanke om samtidig urinretention, överväg bladderscan eller tappning.
Utebliven avföring kan även vara ett symtom på ileus hos patienter med maligna intraabdominala tillstånd, om de genomgått bukkirurgi eller fått strålbehandling mot buken. Ileus i palliativt skede handläggs individuellt 509.
Behandling vid obstipation
Orsaksinriktad behandling
I behandlingen ingår att se över läkemedelsbehandling och sätta ut läkemedel som inte bidrar till symtomlindring men kan bidra till obstipation. För patienter med behov av opioidbehandling bör samtidigt natriumpikosulfat insättas vid behandlingsstart. Individuell dostitrering är nödvändig, men vid höga doser opioider krävs inte sällan även högre doser natriumpikosulfat, eventuellt även kombinerat med makrogolpreparat. Det kan även vara aktuellt med insättning av en partiell my-antagonist, se avsnitt 15.13.3 Behandling vid smärta.
Vid misstanke om eller risk för mekaniskt tarmhinder bör man vara försiktig med motilitetsstimulerande läkemedel såsom natriumpikosulfat eller metoklopramid.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Förstoppning är det vanligaste mag-tarmproblemet bland svårt sjuka patienter och kan yttra sig som andningsproblem, känsla av hjälplöshet och panik. Under livets sista dagar kan förstoppning orsaka motorisk oro om patienten inte längre kan eller orkar kommunicera. Vid misstanke om förstoppning hos en patient med verbala svårigheter kan man göra en varsam palpation per rektum för att känna efter avföringsklumpar. Åtgärder ska utföras skonsamt och bara i syfte att patienten ska må så bra som möjligt 272 274. Observera även patientens möjlighet att ta sig till toaletten, sitta på toaletten osv. Se även avsnitt 13.4.7 Elimination.
Rehabiliteringsåtgärder
Skapa möjlighet för god och funktionell sittställning vid tarmtömning. Kan underlättas med hjälpmedel, exempelvis toastolsförhöjning, fotstöd eller mobil toalettstol. I tidigt palliativt sjukdomsförlopp rekommenderas lämplig fysisk aktivitet för att motverka immobilisering som bidragande orsak till förstoppning. Kontakta rehabpersonal för bedömning/förskrivning.
Katrinplommondryck samt anpassning av kosten för att till exempel undvika stoppande läkemedel bör övervägas.
Farmakologisk behandling
Laxantia är förstahandsval. Prova ett osmotiskt läkemedel av typ makrogol. Börja med 1 påse 2–3 gånger dagligen. Vid utebliven effekt kan dosen ökas med upp till 8 påsar under en dag. Det kan då även lösa fekalom. Vid begränsat peroralt intag kan patienten ha svårt att få i sig den mängd som krävs för makrogol. Natriumpikosulfat och/eller laktulos kan provas som alternativ.
Rektalt tillförda läkemedel såsom stolpiller eller lavemang kan behöva användas. De verkar dock endast om avföring finns i rektum. Vid hård avföring i rektum kan större volym krävas.
Vid opioidförorsakad förstoppning bör man beakta följande i valet av laxantia 510:
- På grund av den peristaltikökande effekten är natriumpikosulfat förstahandsval mot opioidrelaterad förstoppning och bör tillhandahållas vid utskrivning av opioider.
- Om patienten äter och dricker tillräckligt kan makrogoltillägg vara av värde.
- Vid symtomgivande obstipation trots adekvat laxantiabehandling kan man överväga tillägg av perifer opioidreceptorantagonist såsom naloxegol eller naldemedin peroralt även om evidensen anses vara låg 511 pga. brister i studieuppläggen. Effekt av behandlingen kan vanligen utvärderas inom två veckor.
- Metylnaltrexonbromid finns tillgängligt för subkutant bruk.
- Man bör avstå från kombinationspreparat för opioider och antagonist pga. bristande evidens för bättre effekt och begränsad användning vid nedsatt njur- och leverfunktion. Dessutom går det inte att separat dostitrera opioider och laxantia utifrån deras respektive önskade effekt.
- Observera att bulkmedel inte rekommenderas att användas vid opioidförorsakad förstoppning 512.
Patientmedverkan och kommunikation med patient och närstående
Patienten bör få information om vikten av att ställa in rätt dos laxantia och använda läkemedlet kontinuerligt, särskilt vid opioidbehandling. Patienten bör också uppmuntras att föra dagbok över intagna laxantia, avföringsvanor och eventuella biverkningar såsom koliksmärta och övriga bukbesvär. Detta underlättar valet av laxantia och beslut om dosjusteringar.
Oro och ångest
Ångest och oro är normala delar av kris- och sorgereaktioner och är en naturlig reaktion när man får besked om en livshotande sjukdom och i livets slutskede, oavsett diagnos. Ångest kan behandlas med icke-farmakologiska åtgärder såsom stödjande samtal, närvaro och beröring. Vid svår ångest och vid ångest i livets absoluta slutskede kan behandling med bensodiazepiner behövas. De ger ofta god lindring
Definition, förekomst och orsaker
Man brukar skilja mellan oro och ångest. Oro har en utlösande faktor, och det finns alltså något man oroar sig för. Ångest däremot saknar fokus, och personen kan inte definiera vad som orsakar den obehagliga rädslan. Ångest ger också ofta kroppsliga symtom i form av t.ex. hjärtklappning, yrsel, andnöd, motorisk oro, svettningar, muntorrhet eller skakningar 513. Ångest och oro är normala delar av kris- och sorgereaktioner och är en naturlig reaktion när man får besked om en livshotande sjukdom eller nära förestående död. Behandlingen skiljer sig också åt: oro hanteras framför allt med icke-farmakologiska åtgärder medan ren ångest kan kräva farmakologisk behandling.
Den ångest som uppstår i samband med en livshotadande sjukdom påverkar inte bara patienten fysiskt utan även psykiskt, socialt och existentiellt 514.
Bedömning, anamnes och undersökningar
Oro och ångest bör skattas med ett validerat skattningsinstrument såsom ESASr eller iPOS. Att skatta oro och ångest regelbundet är viktigt för att kunna följa upp om en insats eller behandling har haft bra effekt, och för att följa förändringar i patientens symtom. Det kan också vara värdefullt att ta reda på om patienten tidigare haft besvär med oro eller ångest, och vilka strategier som hen då använde för att hantera det.
Behandling vid oro och ångest
Orsaksinriktad behandling
Ibland går det att identifiera en utlösande faktor till patientens oro. Då är det viktigt att om möjligt behandla, minska eller ta bort denna orsak, och inte enbart behandla symtomet.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
I många fall kan oro och ångest lindras av icke-farmakologiska åtgärder såsom mänsklig närvaro, samtal, avslappning eller andningsövningar 515. Taktil massage kan också vara effektivt 494515.
Allt som skapar trygghet leder i regel till minskad oro och ångest. Därför är en viktig del av vårdens uppgift att just skapa trygghet för personen som befinner sig i en kris- och sorgereaktion. Både patienten och de närstående bör fortlöpande få information om sjukdomen, eventuella behandlingar, förväntat förlopp och prognos eftersom det på sikt brukar minska besvären av ångest och oro samt inge trygghet. Man behöver dock fråga hur mycket information patienten orkar och vill ta emot. Oftast kan man behöva ge lite information i taget, och upprepa den flera gånger. Patienter blir också tryggare och mindre oroliga av att få vara delaktiga i sin vård och kunna påverka den.
Stödjande samtal med en kurator, psykolog eller religiös eller andlig företrädare är värdefullt för många och kan hjälpa till att minska ångesten. Många mår bra av att få sammanfatta sin levnad och få berätta sin livshistoria när de närmar sig livets slutskede. Det bidrar till bearbetning och reflektion och hjälper dem att hantera sin sorg, ångest och oro.
Psykosociala insatser kan vara av stort värde för att lösa praktiska problem som orsakar patienten oro. Det kan gälla frågor om ekonomi, framtidsfullmakt eller begravningsplaner.
Även ångest i livets slutskede kan i många fall lindras av icke-farmakologiska åtgärder såsom mänsklig närvaro, samtal och beröring.
Rehabiliteringsåtgärder
Anpassad fysisk aktivitet, avspännings- och kroppskännedomövningar har visat god effekt på oro och ångest.
Farmakologisk behandling
Ibland blir ångesten så svår att den kräver farmakologisk behandling. Det finns ännu få välgjorda studier om farmakologisk behandling vid ångest hos patienter i palliativt skede 516. Empiriskt vet vi dock att antidepressiv medicinering kan vara en effektiv behandling mot ångest hos patienter i tidigt palliativ skede. Hos cancerpatienter är ofta mirtazapin förstahandsvalet eftersom det även stimulerar aptiten och bidrar till bättre sömn, vilket är gynnsamma sidoeffekter vid cancersjukdom. Man kan även överväga andra SSRI- eller SNRI-preparat. Vid sömnbesvär rekommenderas zopiklon eller zolpidem.
Vid svåra ångestattacker tidigt i sjukdomsförlopp och i livets slutskede kan patienten erbjudas kortverkande bensodiazepiner såsom oxazepam alternativ Midazolam, som vidbehovsdoser.
Vid mycket svår ångest kan man överväga diazepam eller alprazolam som har längre halveringstid men de är sällan förstahandsval eftersom de ofta ger viss sedering. Speciellt diazepam bör undvikas för personer> 75 år på grund av sederingsrisken, som beror på att de aktiva metaboliterna stannar kvar länge i kroppen och gör behandlingen svårstyrd. Diazepam kan t.o.m. ge ökad ångest när det går ur kroppen.
Ångest i döendefasenen behandlas farmakologiskt med midazolam i subkutana injektioner eller i kontinuerlig infusion via pump. Börja med låg dos och titrera sakta upp till lägsta effektiva dos. Ett fåtal patienter får ökad ångest och oro av bensodiazepiner. Då har i regel tillägg av haloperidol (Haldol) god effekt.
Patientmedverkan och kommunikation med patient och närstående
Det är viktigt att tillsammans med patienten och de närstående försöka hitta eventuella utlösande faktorer för ångest och oro. Det är även värdefullt för patienten att få kunskap om olika tekniker och strategier för att hantera symtomen, t.ex. andningsteknik, avslappning och meditation 479.
Smärta
Grunden för en dokumenterad smärtbedömning och behandlingsplan är, oavsett diagnos, anamnestiska fynd samt objektiva fynd utifrån klinisk undersökning och diagnostik.
Valet av smärtbehandling baseras på bakomliggande smärtmekanism. Behandlingen ska vara individanpassad med realistiska mål om att lindra symtom och förbättra livskvalitet och funktion.
Smärtbehandling initieras och utvärderas multiprofessionellt
Vid utebliven smärtlindring, ändrad smärtkaraktär eller lokalisation, eller ökande symtom, görs en ny smärtanalys inför valet av behandling.
Morfin är förstahandsval bland opioider för behandling av nociceptiv smärta. För att utröna om smärtan är opiodkänslig kan man sätta in initial behandling med kortverkande preparat.
Vid start av opioidbehandling bör samtidigt laxantia insättas (förstahandsval natriumpikosulfat) och ev. antiemetikabehandling under första dagarna (t.ex. peroralt meklozin eller subkutant haloperidol).
Smärtbehandling med opioidplåster är enbart lämpligt vid stabil opioidkänslig smärta hos patienter som har cancerrelaterad smärta men svårt att ta tabletter eller osäkert upptag från mag-tarmkanalen. Byte från peroral behandling till plåster bör initieras i god tid innan patienten är oförmögen att inta peroral medicinering.
Vid otillräcklig effekt (ex VAS> 3) av konventionell smärtlindring som beskrivs i detta kapitel bör en enhet med kompetens i specialiserad palliativ vård kontaktas.
Definition, förekomst och orsaker
Smärta är en ”obehaglig sensorisk och emotionell upplevelse förknippad med vävnadsskada, hot om vävnadsskada eller en upplevelse som kan liknas vid denna” (IASP, International Association for the Study of Pain, 2020).
Smärta är ett vanligt symtom i befolkningen, och det blir vanligare mot livets slutskede. En systematisk genomgång från 2023 517 visar att smärta förekommer hos 45 % av patienter med cancersjukdom. Efter botande behandling är andelen 36 %, medan 50 % av dem med pågående cancerbehandling har smärta. Vid avancerad, spridd cancer förkommer smärta hos 55 % av patienterna, och 41 % av patienterna med avancerad cancer har måttlig till svår smärta.
Smärta vid svår hjärtsvikt är ett dominerande symtom som leder till försämrad livskvalitet. Totalt 67 % av patienter med hjärtsvikt uppger att smärta är ett problem. Enligt en studie fick mindre än hälften av patienterna med KOL adekvat smärtlindring. Detta tyder på att patienter med KOL troligen har stor risk för att inte få adekvat smärtlindring 518.
Nociceptiv smärta
Nociceptiv smärta kan också kallas vävnadsskadesmärta. Perifera nociceptiva neuroner (nociceptorer) aktiveras och nervsignalen fortleds av ett normalt fungerande nervssystem vid exempelvis hudpenetration, inflammation eller ischemi.
Visceral smärta, dvs. smärta från inre organ, är ofta diffus och svårlokaliserad medan somatisk smärta från till exempel rörelseapparaten, huden eller slemhinnorna är vällokaliserad och distinkt.
Neuropatisk smärta
Neuropatisk smärta är smärta som orsakas av en skada eller sjukdom i det somatosensoriska nervsystemet. Skada kan uppstå i:
- centrala nervsystemet (hjärna och ryggmärg) vid exempelvis MS, stroke och traumatisk ryggmärgsskada
- perifera nervsystemet vid exempelvis diabetes mellitus, herpes zoster eller diskbråck med rotpåverkan.
Denna smärta beskrivs ofta som brännande, elektrisk eller utstrålande längs ett dermatom eller en perifer nervs utbredningsområde. Känselstörningar finns inom det smärtande området om den påverkade nerven försörjer ett visst hudområde. Spontant svåra huggande smärtor kan också förekomma.
Nociplastisk smärta
En från början akut nociceptiv eller neuropatisk smärta kan över tid medföra plastiska förändringar i smärtsystemen. Dessa kan beskrivas som att volymen på nervsignalen vrids upp. Processen, som kallas centralt störd smärtmodulering eller central sensitisering, leder till:
- smärtspridning, dvs. den initialt lokala smärtan sprider sig över tid till att vara ett regionalt eller ett generaliserat tillstånd
- ökad smärtkänslighet: allodyni (det som normalt inte gör ont, t.ex. lätt beröring, blir smärtsamt) och hyperalgesi (det som normalt är smärtsamt gör ännu mer ont).
Det är också vanligt att symtomen blir allt fler och att smärtan inte är proportionerlig till den ursprungliga skadan eller patologin 519.
Bedömning, anamnes och undersökningar
Bedömning av smärta
Både diagnostik och behandling av smärta ska baseras på den underliggande smärtmekanismen, oavsett bakomliggande diagnos eller diagnoser. Mångdimensionell smärtanalys är grunden för beslut om smärtbehandling. Till stöd för bedömningen kan patienten fylla i en strukturerad smärtskattning, se även Kapitel 12 Att arbeta strukturerat med palliativ vård och behandlingsstrategier.
Smärta vid livshotande sjukdom bör tolkas i ett mångdimensionellt perspektiv, som ett resultat av komplexa interaktioner mellan fysiska, psykiska, sociokulturella och existentiella dimensioner. Det gäller oavsett om det handlar om cancer eller annan kronisk sjukdom, och oavsett om patienten befinner sig i sent eller tidigt palliativt skede 520.
Anamnes
Följande frågor bör besvaras som underlag för smärtanalysen:
- Var är smärtan lokaliserad? Använd gärna smärtteckning
- Hur intensiv är smärtan, mätt med hjälp av smärtskattningsformulär?
- Är smärtan kontinuerlig eller intermittent?
- Är den belastningsrelaterad?
- Är smärtan aktivitetsrelaterad?
- Finns någon förändrad känsel i anslutning till det smärtande området?
- Finns någon dygnsvariation? Uppmärksamma särskilt sömnstörningar.
- Har patienten andra symtom såsom ångest, påverkad sömn eller depression som påverkar smärtupplevelsen?
- Har patienten någon välfungerande strategi för att lindra smärta? Kan den utvecklas vidare?
- Hur påverkar smärtan patientens dagliga liv med arbete, socialt liv, sömn, aptit, sex och humör?
- Finns kommunikationsproblem?
- Vilken sjukdom har patienten? Hur är sjukdomsförloppet? Hur är den beräknade livslängden? Finns någon samsjuklighet?
- Har patienten någon aktuell läkemedelsbehandling?
- Har patienten någon beroendeproblematik?
Undersökning
Smärtanalysens anamnestiska fynd samt objektiva fynd utifrån klinisk undersökning kompletteras efter behov med riktade neurofysiologiska, radiologiska och biokemiska analyser. Utifrån svaren görs en smärtbedömning som ska dokumenteras, och som ligger till grund för den behandling som sedan erbjuds.
Behandling vid smärta
Val av behandlingsstrategi
Smärtbehandling i palliativt skede ska alltid ses som del av en helhet, där smärtan är ett av flera vanliga och oftast samtidigt förekommande symtom. Helhetsperspektivet innebär att uppmärksamma patientens fysiska smärta men också psykiskt lidande, social problematik och separation samt existentiella dimensioner av lidande.
Det är viktigt att identifiera var i sjukdomsförloppet patienten befinner sig för att kunna föra en meningsfull dialog om målet med vård och behandling, och för att kunna erbjuda lämplig smärt- och symtomlindring på rätt vårdnivå.
Den smärtbehandling som väljs ska utgå från bakomliggande smärtmekanism och vara individualiserad med realistiska mål om att lindra symtom och förbättra livskvaliteten och funktionen. Smärtbehandlingen ska innefatta utvärdering och uppföljning. Eventuella biverkningar av analgetika ska bedömas i relation till effekten, och här är det viktigt att patienten får så mycket information som möjligt om smärtbehandlingen, dess fördelar men också risken för biverkningar. Detta för att bästa möjliga smärtbehandling ska kunna erbjudas. Vid utebliven smärtlindring, ändrad smärtkaraktär eller lokalisation eller ökande symtom görs en ny smärtanalys inför valet av behandling.
Vid otillräcklig effekt (VAS> 3) av konventionell smärtlindring som beskrivs i detta kapitel bör en enhet med kompetens i specialiserad palliativ vård kontaktas. Ytterligare smärtlindringsregim, t.ex. med metadon, eller interventionell smärtlindring såsom epidural eller intratekal smärtlindring behöver i regel ges och följas upp i den specialiserade palliativa vården, eller med stöd av den.
I vissa fall behövs en fördjupad smärtbedömning. Det gäller exempelvis vid:
- smärta NRS> 3, antingen konstant eller i besvärande smärtgenombrott minst 3 gånger per dygn som föranleder extrados trots hög dos opioid (total dygnsdos> 200 mg morfinekvivalent)
- svåra biverkningar av smärtmediciner
- ovilja att ta emot smärtbehandling med opioid
- andra speciella situationer, t.ex. att patienten har eller haft beroendeproblem, missbruk eller annan psykiatrisk samsjuklighet
- snabb progress av smärtintensitet
- förväntad svår smärta.
Figur 6. Behandlingsstrategi vid nociceptiv smärta, särskilt cancerrelaterad smärta
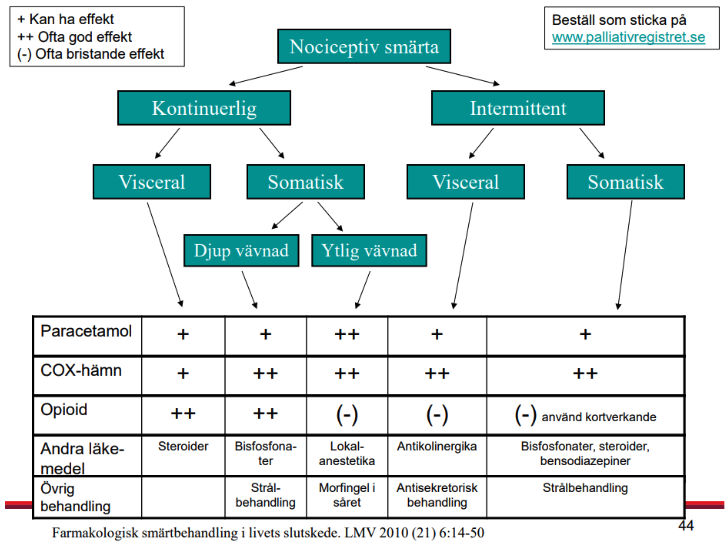
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Icke-farmakologiska smärtbehandlingsmetoder kompletterar de farmakologiska för att optimera smärtlindringen för patienten i sjukdomens olika stadier 521. De är ett komplement för att balansera biverkningar av farmakologisk behandling, till exempel trötthet och nedsatta kognitiva funktioner. Ickefarmakologiska behandlingar ger inte denna typ av biverkningar, vilket innebär att patienten kan ha bättre kontakt med sina närstående i livets slutskede 295. Icke-farmakologiska smärtbehandlingsmetoder kan även minska andra symtom såsom stress, oro och fatigue.
Kommunikation är ett grundläggande redskap för att skapa bättre vård, och en förutsättning för smärtbehandling. Om patienten inte förstår givna råd, eller inte känner tillit eller engagemang, minskar sannolikheten att hen följer råden och den aktuella behandlingsregimen 522. Det goda samtalet kan dock lindra smärtan och hjälpa en person till omorientering. Samtalet ger möjligheter och förutsättningar för hopp och kan vara en lindrande, tröstande och meningsskapande handling i sig självt 523.
Rehabiliteringsåtgärder
Nedan följer en översikt över de icke-farmakologiska smärtbehandlingsmetoder i palliativ vård som är vanligast och som kliniskt visat goda effekter. Olika yrkeskategorier kan involveras i detta utifrån kompetens. En del saker kan patienten och/eller de närstående sköta själva. Metoderna kan användas under hela sjukdomsförloppet och får modifieras efter smärtans ursprung och karaktär. Det finns dock få studier och översiktsartiklar som undersökt effekter av dessa smärtlindringsmetoder, och det finns därför svag vetenskaplig evidens.
Fysisk aktivitet kan upplevas som smärtlindrande under sjukdomsförloppet och behöver individanpassas. Fysisk aktivitet och träning aktiverar kroppens eget smärthämmande system, framför allt i ett tidigt skede då patienten kan konditionsträna regelbundet. I ett senare skede kan fysisk aktivitet minska risken för stelhet, smärta och rörelserädsla, och för att patienten ska fortsätta att känna hopp 295.
Värme och kyla kan provas som komplement till annan smärtlindrande behandling, till exempel tillsammans med TENS-behandling.
TENS kan prövas som smärtlindring vid både nociceptiv och neuropatisk smärta, till exempel vid skelettmetastaser eller smärtsamma såromläggningar (procedursmärta). Det kan också vara en lämplig metod för att ge patienten bättre smärtlindring i aktivitet 524. TENS är dock kontraindicerat för patienter med sänkt medvetandegrad, ICD och pacemaker samt nära arteria carotis (halsens framsida). Vid nedsatt sensibilitet behöver man vara aktsam.
Smärtlindring genom lägesändringar och hjälpmedel: Utifrån patientens behov kan patienten och även de närstående få information och instruktioner om sätt att lindra smärta, till exempel förflyttningsteknik, lägesändringar och viloställningar för att förebygga och lindra smärta. Olika hjälpmedel kan också underlätta såsom ortoser, positioneringskuddar och glidlakan 521.
Akupunktur och öronakupunktur kan användas som tillägg till läkemedelsbehandling vid olika smärttillstånd, och de ger bättre effekt om de kombineras 521. Öronakupunktur har visat måttlig till stor effekt vid neuropatiska smärtor 525. Akupunktur rekommenderas dock inte i smärtstillande syfte vid cancerrelaterad smärta 526.
Massage kan lindra smärta, oro och illamående 527. Den fysiska kontakten kan också minska stress. Inom detta område finns olika tekniker och metoder såsom mjuk massage, taktil massage/stimulering, akupressur och aromaterapi 16. Här kan även närstående göras delaktiga och instrueras, om de och patienten vill det 528.
Interventioner såsom avspänningstekniker, kognitiv beteendeterapi (KBT) och musikterapi kan användas för att minska smärtan och/eller för att patienten ska lära sig att hantera sin smärta 529.
Tejpning med kinesiologitejp kan användas vid både ledsmärta och muskelsmärta 530.
Farmakologisk behandling
Behandling med icke-opioider
Den farmakologiska arsenalen för att lindra smärta innefattar konventionella läkemedel såsom paracetamol, COX-hämmare/NSAID och kortison. Utöver detta används adjuvant läkemedelsbehandling, t.ex. för att behandla neuropatiskt smärta. Adjuvans är icke-opioida läkemedel som har smärtlindrande effekt i sig eller förstärker effekten av opioider. De har oftast annan primär indikation än smärta. Se avsnitt om behandling av neuropatiskt smärta.
För kompletterande specifika onkologiska behandlingsalternativ, se avsnitt 16.7 sjukdomsspecifik behandling – solida tumörsjukdomar.
Paracetamol
Paracetamol har en given plats i behandlingsarsenalen vid lindrig smärta. Doserna behöver reduceras vid lever- eller njursvikt.
Vid cancerrelaterad smärta har paracetamol ingen säker tilläggseffekt när patienten står på stark opioid 531. Man kan dock pröva paracetamolbehandling eftersom många patienter med palliativa vårdbehov har degenerativa sjukdomar som samsjuklighet och även kan drabbas av sekundär muskel- och ledvärk. Effekten bör noga utvärderas och behandlingen ska enbart fortsätta om den ger symtomlindring.
COX-hämmare alternativt NSAID
COX-hämmare är potenta analgetika som har en given plats vid smärttillstånd såsom akut nociceptiv, rörelsekorrelerad och inflammatorisk smärta samt visceral krampsmärta. Deras användbarhet tidigt i ett sjukdomsförlopp begränsas dock av välkända och ibland svåra biverkningar såsom andfåddhet på grund av vätskeretention, blödningsrubbningar, gastrointestinala besvär, njursvikt och ökad risk för förvirringstillstånd. För att minska risken för biverkningar kan intermittent behandling övervägas. Biverkningarna är ofta dosberoende och riskerna ökar med behandlingstiden. Risken för njursvikt är framför allt kopplad till dehydrering. Därför bör man inom några dagar utvärdera effekten och ta ställning till att fortsätta eller avsluta behandlingen. Om patienten inte kan inta läkemedel peroralt kan COX-hämmare ges intravenöst, både selektiva COX-2-hämmare (parecoxib) och traditionella NSAID (ketorolak). Ketorolak kan även ges subkutant. COX-2-hämmare innebär mindre risk för blödningsbiverkningar men ökad kardiovaskulär risk jämfört med COX-1-hämmare. Risken för vätskeretention och njursvikt är lika stor för samtliga COX-hämmare/NSAID.
I sent sjukdomsskede bör risken för biverkningar vägas mot behandlingseffekten, särskild vid god effekt av COX-hämmare.
Kortikosteroider
Kortikosteroider kan ha god effekt vid många smärttillstånd inom palliativ vård, oberoende av diagnos. Detta gäller bland annat vid inflammatoriska tillstånd, skelettsmärta beroende på skelettmetastaser, perineuralt ödem (svullnad och inflammation runt nerver), ryggmärgskompression, subileus eller ileus och engagemang av kapseln till solida organ. Den vetenskapliga evidensen för kortikosteroidernas smärtlindrande effekt är svag, men klinisk erfarenhet talar för effekt vid ovanstående smärttillstånd. Vid längre behandling ökar risken för biverkningar avsevärt. Kortisonbehandlingens effekt bör därför utvärderas efter 3–5 dagar och behandlingen enbart fortsätta vid positiv effekt. Nedtrappning till lägsta möjliga underhållsdos bör eftersträvas. Vid utebliven effekt kan behandlingen avslutas abrupt inom 14 dagar efter insättning. Som initial startdos rekommenderas 4–8 mg betametason på morgonen. Undantag gäller för särskilda tillstånd såsom medullakompression eller hjärnödem, se Kapitel 14.
Betameson har oftast större antiinflammatorisk effekt och ger mer långvarig effekt än andra steroider, och är därför oftast förstahandsval.
Se även avsnitt 15.15.3 Behandling av symtom med kortikosteroider.
Behandling med opioider
Opioider har framför allt en effekt vid nociceptiv visceral smärta av molande karaktär och vid djup somatisk nociceptiv smärta. De har också god effekt vid akuta nociceptiva tillstånd.
Opioidbehandling bör kontinuerligt övervakas och utvärderas, särskilt för patienter i tidig palliativ sjukdomssjukdomsförlopp. I stabil sjukdomssjukdomsförlopp, t.ex. vid god effekt av antitumoral behandling, bör man överväga att minska dosen eller helt sätta ut opioider.
Starka opioider har en likvärdig smärtlindrande effekt på gruppnivå, men framför allt biverkningarna kan skilja sig åt mellan individer. Därför kan det löna sig att byta till en annan opioid vid god smärtlindrande effekt men kvarstående besvärande biverkningar (så kallad opioidrotation). Förstoppning, illamående, trötthet och kognitiv påverkan är de vanligaste biverkningarna, och både förstoppning och illamående kan förebyggas. Det är viktigt att informera patienten om förväntade effekter och biverkningar. Ofta går det att minimera biverkningarna genom att individualisera behandlingen och, förutsatt att det gäller opiodkänslig smärta, noggrant titrera opioiddosen. Samtidigt bör man förskriva laxantia (förstahandsval är natriumpikosulfat) och antiemetika (t.ex. meklozin 12,5–25 mg x 2 i insättningsfas).
Smärtbehandling vid opioidkänslig smärta kan inledas med antingen kortverkande eller långverkande preparat.
Detta är grundprinciperna för behandling med starka opioider:
- Patienten ska alltid ha tillgång till extradoser.
- Fortsatt dostitrering sker med hjälp av mängden extradoser.
- Läkemedel mot förstoppning och illamående ordineras.
- Behandlingen ges i första hand peroralt.
- Vid övergång från peroral till subkutan eller intravenös behandling: titta i konverteringsguiden. Därefter ska behandlingen utvärderas och justeras.
- Vid opioidbyte ska den nya opioiddosen initialt reduceras något, men den ska utgå från den totala dygnsdosen inkluderande intagna vidbehovsdoser.
- Studieresultat för användning av opioider vid (svår) njursvikt är svårtolkade. Riktlinjer råder att iaktta försiktighet vid njurfunktionsnedsättning: Var observant på eventuella biverkningar och var beredd att reducera dos eller frekvens av administrering 532 533
Om det är oklart ifall patienten har opiodkänslig smärta kan man inleda behandling med kortverkande morfin 5–10 mg vid behov. Utvärdera effekten efter 1–2 dygn, och vid opioidkänslig smärta går man över till depåpreparat, och delar den totala dygnsdosen på 2 doser. Vid insättning av långverkande preparat ska patienten ha tillgång till extradoser av kortverkande preparat som motsvarar 1/6 av den totala dygnsdosen.
Morfin
Morfin är referenspreparatet för alla starka opioider; det finns tillgängligt i alla beredningsformer och rekommenderas i regel som förstahandspreparat. Morfin är även ett standardpreparat i ordinationer av palliativa parenterala vidbehovsläkemedel och i läkemedelsförråden. Om man förskriver något annat preparat bör det säkerställas att samtliga involverade vårdgivare har tillgång till det förskrivna preparatet.
Vid eGFR <30 ml/min bör Morfin undvikas. .
Morfin har varierande biotillgänglighet (15–65 %) peroralt, men i parenteral form är det ekvipotent med oxikodon.
Oxikodon
Oxikodon har generellt högre och jämnare biotillgänglighet (60–80 %) än morfin. Den perorala dosekvivalensen mellan oxikodon och morfin är 1:1,5–2.
Hydromorfon
Hydromorfon är 5–7 gånger mer potent än morfin. Preparatet används vid höga opioiddoser, huvudsakligen inom specialiserad palliativ vård. Hydromorfon administreras framför allt i läkemedelspumpar eller ges som subkutana injektioner.
För patienter med injektionsdoser av morfin som överstiger 1,5 ml per dos bör man överväga att gå över till hydromorfon eftersom ekvipotent opioiddos kan ges i mindre volym. Vid tveksamhet, kontakta gärna en enhet med kompetens i specialiserad palliativ medicin.
Fentanyl
Fentanyl är cirka 100 gånger mer potent än morfin. Plåsterbehandling med fentanyl är enbart lämpligt vid stabil opioidkänslig smärta hos patienter som har cancerrelaterad smärta men svårighet att ta tabletter eller osäkert upptag från mag-tarmkanalen.
Plåstret byts normalt vart 3:e dygn, och man bör dagligen kontrollera att plåstret sitter på plats. Vid transdermal behandling ses full effekt efter cirka 24 timmar. Hos kakektiska patienter kan upptaget ändras 534, och då går det inte att förlita sig på konverteringsguiden 535. Dessutom blir upptaget mer ojämnt fördelat över tid. Upptaget ökar vid feber, vilket bör beaktas.
Plåsterbehandling är mindre lämplig till patienter med akut smärta eller instabila smärttillstånd, feber eller rikliga svettningar.
Fentanyl finns även för transmukosal och sublingual som kan användas vid smärtgenombrott där snabb effekt eftersträvas. Effekten ses inom 15 minuter och den kvarstår i cirka 1 timme. Fentanyl i denna beredning bör endast förskrivas efter rådgivning med en specialiserad palliativ enhet.
Buprenorfin
Buprenorfin transdermalt är i styrka jämförbart med svaga opioider; buprenorfinplåster på 5 µg per timme motsvarar en peroral dygnsdos morfin på 5–10 mg. Dess indikation är icke maligna smärtor av måttlig intensitet, och det är inte lämpligt för behandling av akuta smärttillstånd med tanke på att full effekt ses först efter 3 dygn. Plåstret byts var 7:e dag.
Vanliga biverkningar av opioidbehandling
Andningsdepression
Opioider kan hämma andningscentrum hos en frisk, smärtfri person. Smärta stimulerar dock andningscentrum och motverkar denna effekt. Underhållsbehandling med opioider leder relativt snabbt, inom cirka 1 vecka, till en toleransutveckling mot de andningsdeprimerande effekterna, och risken för andningsdepression (att andningen blir påverkad) är mindre hos dessa patienter än för personer som provar opioider för första gången.
Opioidrelaterad andningsdepression kännetecknas av sänkt vakenhet, knappnålsstora pupiller och framför allt en andningsfrekvens på <8–10 andetag per minut. Om patienten snarare har en normal eller förhöjd andningsfrekvens finns troligen en annan orsak till den sänkta vakenheten. Opioidutlöst andningsdepression med <8 andetag per minut kan brytas genom att ge små doser av naloxon. Späd en ampull naloxon till 10 ml och ge 0,5 ml (0,02 mg naloxon) subkutant, varje till varannan minut tills andningsfrekvensen är> 8 andetag per minut. Den korta halveringstiden hos naloxon gör att naloxontillförseln ofta behöver upprepas innan opioidkoncentrationen minskat tillräckligt. Alltför höga doser naloxon bryter den smärtlindrande effekten av opioiden och leder till svår smärta och ångest hos patienten.
Förstoppning
Förstoppning är en närmast ofrånkomlig biverkan av opioider och den kvarstår under hela behandlingstiden. För patienter med palliativa vårdbehov är genesen oftast multifaktoriell (t.ex. nedsatt peroralt intag, immobilisering eller övrig medicinering som bidrar till obstipation). Patienten behöver informeras om det för att inte följsamheten till behandling med opioidpreparat och laxantia ska försämras.
Den opioidrelaterade förstoppningen är en direkt effekt på tarmarna (minskar tarmrörelser) i kombination med ökad tonus (ökad muskelspänning) i glatt muskulatur både i tarmar (t.ex. analsfinkter), urinvägar och gallvägar. Opioidbehandling leder även till minskad sekretion och ökad resorption av vätska i tarmen. På engelska kallas detta syndrom med förstoppning och tonusökning för OIBD (opioid induced bowel dysfunction), och i svåra fall kan patienten också drabbas av buksmärtor, gasbildning, utspänd buk, aptitlöshet och illamående. Behandlingen består av att förebygga besvären genom att påbörja laxantiabehandling direkt vid opioidinsättning. Ofta kombineras motorikstimulerande medel (t.ex. pikosulfat) med osmotiskt verkande laxantia (t.ex. makrogol). Osmotiskt verkande laxantia kräver dock tillräckligt peroralt intag av dryck. Laktulos rekommenderas inte eftersom det ökar gasbildningen ytterligare.
Generellt sett har preparat som hämmar morfinreceptorer perifert i tarmen en effekt som vanliga laxermedel inte har, eftersom de minskar tonusökningen i glatt muskulatur. Kombinationspreparat med oxikodon och naloxon bör undvikas på grund av risken för att naloxon hamnar systemiskt och hindrar smärtlindringen, t.ex. vid interaktion och leverpåverkan av annan genes. Kliniskt finns det även en fördel med att separera preparaten för att möjliggöra individuell dostitrering för behandling mot smärta respektive förstoppning. Vid misstanke om opioidrelaterad förstoppning som inte svarar på sedvanlig laxantiabehandling kan man pröva separat tillägg av perifer opioidreceptorantagonist såsom peroralt naloxegol eller naldemedin alternativt parenteralt metylnaltrexonbromid.
Illamående
Illamående drabbar cirka 30 % av patienterna och risken är högre för uppegående och yngre patienter. Behandlingen ska vara förebyggande och lämpliga preparat är meklozin, metoklopramid eller haloperidol. Tolerans utvecklas oftast mot illamåendet, och efter 7 - 10 dagar kan en besvärsfri patient övergå till medicinering vid behov. Ondansetronbehandling bör undvikas pga. av risken för obstipation
Trötthet
Trötthet och lätt sedering är vanligt i behandlingens inledning. Initial trötthet kan upplevas som en mycket störande biverkan så både patienten och de närstående bör informeras om att tolerans utvecklas inom 7 dagar och besvären brukar då normalt minska. Kvarvarande trötthet bör leda till en ny smärtanalys och utvärdering av behandlingen. Trötthet kan vara en biverkan, men också en effekt av behandlingen som ger patienten bättre möjligheter att slappna av och vila.
Opioidinducerad hyperalgesi
Förutom opioidernas välkända biverkningar finns ett annat viktigt problem: opioidinducerad hyperalgesi (OIH). Det innebär att opioiderna i sig kan ge upphov till mycket svåra smärttillstånd, i stället för att lindra smärtan. Det drabbar framför allt patienter som står på höga opioiddoser. Ju mer opioider man sedan ger till en patient som drabbats av OIH, desto värre smärta. De bakomliggande mekanismerna för detta tillstånd är komplicerade, och den intresserade hänvisas till internationell litteratur. Kliniskt ska tillståndet misstänkas om patienten behöver snabbt stigande opioiddoser, som endast har en kortvarig lindrande effekt, och utvecklar hyperalgesi (ökad smärtupplevelse, så att en smärtsam retning gör mer ont än vad den ”borde” göra) och allodyni (en icke smärtsam beröring utlöser smärta). Även små muskelryckningar kan förekomma. OIH är komplicerat, och vid misstanke ska man kontakta en specialist i palliativ medicin eller anestesiologi. Man bör rent konkret ta ställning till additiv farmakologisk behandling (till exempel NSAID eller COX-hämmare, kortison, NMDA-receptorblockad) samt drastiskt sänka opioiddosen.
Farmakologisk behandling av neuropatisk smärta
Det finns väletablerade rekommendationer för behandling av neuropatisk smärta i flera nationella och internationella riktlinjer, och man bör utgå från dem även för smärta vid cancer. Många patienter med palliativa vårdbehov, särskilt patienter med cancer, har dock blandade smärttillstånd med en mer eller mindre tydligt framträdande neuropatisk smärtkomponent.
Utifrån klinisk erfarenhet rekommenderas att pröva antidepressiva läkemedel (amitriptylin eller duloxetin) företrädesvis vid konstant stickande och brännande smärta. Duloxetin ger även effekt vid perifer neuropati såsom biverkan efter cellgiftsbehandling.
Observera att effekten kan utvärderas först efter cirka 2–4 veckor. Behandlingen är därmed mindre användbar för patienter med begränsad tid kvar i livet eftersom det kräver långsam dostitrering i flera veckor.
Antiepileptika (i första hand gabapentin) kan fungera bättre vid huggande, skärande smärta med snabb acceleration och/eller ischialgiform utstrålning. Effektinträdet är oftast betydlig snabbare än för antidepressiva, vilket möjliggör snabbare dostitrering. Hänsyn behöver tas till nedsatt njurfunktion. Till yngre och njurfriska patienter rekommenderas insättning av startdos 300 mg till kvällen, med upptrappning med ytterligare 300 mg inom 3–7 dagar. Första måldos är 600 mg x 3, och om det inte ger effekt kan preparatet trappas ut under 1 vecka. Till äldre patienter är startdosen 100 mg, med upptrappning i steg om 100 mg.
Observera att gabapentin även har en viss ångestdämpande effekt, vilket kan utnyttjas vid multifaktoriell genes till smärta. Men det behöver också beaktas vid nedtrappning eller utsättning pga. risk för utsättningssymtom i form av stegrad ångest.
Beakta även att antidepressiva och antiepileptika kan öka känsligheten för opioider genom att smärtan lindras genom andra mekanismer. Om patienten har otillräcklig smärtlindring trots höga opioiddoser, och tillägg av antineuropatisk behandling har god effekt, behöver opioiddosen sänkas parallellt.
Övriga adjuvanta läkemedel
Spasmolytika
Obstruktion av njurvägar, gallvägar eller tarmar kan orsaka en spasm eller koliksmärta som är mycket smärtsam. Antikolinerga läkemedel såsom butylskopolamin eller glykopyrron har ofta god effekt vid nociceptiva intermittenta viscerala smärtor. Spasmolytika används också för att minska sekretionen från gastrointestinalkanalen vid ileus. Varken butylskopolamin eller glykopyrron passerar blod-hjärnbarriären och ger därför inga antikolinerga biverkningar från CNS. Glykopyrron ges ofta i dosen 1 ml x 1–2 subkutant.
Lokalanestetika
Lidokainplåster är ett tillskott i behandlingen av neuropatisk smärta, framför allt vid postherpetisk smärta. Det kan även användas vid perifera neuropatier.
Övriga läkemedel inom specialiserad palliativ vård
Om grundarsenalen inte ger tillräcklig smärtlindring behöver man kontakta en läkare med specialistkunskap i smärta (enhet för specialiserad palliativ vård eller smärtenhet). Ytterligare ett antal läkemedel kan då bli aktuella att använda.
Metadon
Vid komplexa och svårbehandlade smärttillstånd kan tillägg av låg dos metadon hjälpa, och detta utnyttjas alltmer inom framför allt specialiserad palliativ vård. Metadon är en opioid som vid rätt användning kan vara mycket effektiv, men det förutsätter specialistkunskaper eftersom preparatet inte är jämförbart med andra starka preparat i morfingruppen. Detta beror på en komplicerad farmakokinetik som innebär att preparatets halveringstid varierar. Det finns också interaktionsrisk med flera läkemedel; exempelvis innebär flukonazol kraftigt ökad koncentration av metadon med risk för överdosering (itrakonazol kan då ofta användas). Om kombinationen inte kan undvikas bör metadondosen reduceras. En svensk studie om metadon som tillägg till pågående opioidbehandling 536 visar att det många gånger går att få en säker och effektiv smärtbehandling med en startdos om 2,5 mg x 2 följd av långsam upptitrering. Vid otillräcklig smärtlindring kan dosen ökas till 5 mg x 2 efter 2–3 dagar, och fortsatt titrering i steg om 2,5 mg x 2 kan göras upp till en dos om 10 mg x 2. Har patienten ingen tilläggseffekt av denna dos avslutar man behandlingen tvärt och överväger behandlingsförsök med ketamin (se avsnitt 3.5.5.2).
I öppenvård bör patienten följas upp varannan eller var tredje dag under upptrappning för att utvärdera effekt och eventuella bieffekter. Om tilläggsbehandlingen ger bra smärtlindrande effekt stannar man på aktuell dos och påbörjar samtidigt en dossänkning av den ursprungliga opioiden i steg om 10–20 % av dygnsdosen för att undvika opioidöverdosering. Bakgrunden är metadonets NMDA-receptorblockerande effekt som minskar central sensitisering och har en opioidsparande effekt. Är patienten bra smärtlindrad men visar tecken på överdosering är det alltså dosen av ursprungsopioiden som ska sänkas medan metadondosen ligger kvar.
Vid tillägg av lågdos metadon till annan opioidbehandling är det ursprungsopioiden som används för eventuella extradoser. Metadondosen behöver inte räknas in i den totala dygnsdosen av opioider eftersom det huvudsakligen är metadonets NMDA-receptorblockerande effekt som eftersträvas.
Ketamin
Ketamin har funnits på marknaden i snart 50 år. Från början introducerades och användes det som ett narkosmedel, men i subanestetiska doser har substansen en god smärtlindrande effekt, huvudsakligen genom en NMDA-receptorblockerande effekt. Dess unika verkningsmekanism med ringa påverkan på andning och cirkulation har gett ketamin en plats även inom palliativmedicinen. Ketamin kan ha en positiv effekt vid opioidinducerad hyperalgesi, svår neuropatisk smärta, central sensitisering och rörelsekorrelerad smärta där NMDA-receptorer är aktiverade. De kliniska erfarenheterna är goda med fallstudier som rapporterar om goda effekter, men än så länge finns svagt vetenskapligt stöd för ketamin inom palliativ vård. Inom palliativ vård med erfaren personal används ketamin eller esketamin vid svåra behandlingsrefraktära smärtor och kan administreras peroralt, nasalt, subkutant eller intravenöst. Ketamin är inte ett rutinpreparat och bör därför hanteras av eller i samråd med erfaren personal, såsom en anestesiolog, smärtläkare eller palliativmedicinare.
Klonidin
Klonidin används huvudsakligen inom barnsmärtvården men kan vara ett alternativ även för vuxna med komplex smärta där det finns ett starkt stresspåslag och sympatikus är aktiverat. Klonidin påverkar noradrenerga neuroner som hämmar nociception via flera mekanismer. Den kliniska effekten beror dels på en egen analgetisk effekt, dels på en potentiering av opioider och lokalanestesimedel. Klonidin har dessutom en ångestdämpande, stressreducerande effekt, och är i högre doser sederande vilket används inom intensivvården 537 Biotillgängligheten är 95 % vid oral tillförsel, vilket betyder att doseringen peroralt och parenteralt är densamma. Klonidin finns som injektionslösning och kan ges både subkutant och intravenöst samt i licensform som tabletter och i plåsterberedning. Inom barnsmärtlindring används klonidinmixtur APL (Apotek Produktion och Laboratorier). Vanlig startdos är 75 µg x 3–4 och maximal dygnsdos är 600 µg. Preparatet kan även ges vid behov.
Biverkningarna är oftast lindriga såsom yrsel, trötthet och ortostatisk hypotension. Bradykardi förekommer vid högre doser. Blodtryckskontroll rekommenderas vid insättning, framför allt till äldre patienter.
Dexmedetomidin, en selektiv alfa-2-receptoragonist som liknar klonidin, har intressanta smärtlindrande och sederande egenskaper och forskning pågår om dess plats i palliativ vård.
Bisfosfonater
Bisfosfonater och monoklonala antikroppar mot RANKL (Receptor activator of nuclear factor kappa-Β ligand) kan minska smärtan från skelettmetastaser, framför allt genom att förebygga skelettrelaterade händelser, och de ingår ofta i den onkologiska behandlingen. Användningen inom den palliativa vården begränsas dock av att det tar lång tid innan full effekt uppnås, även om intravenös tillförsel i högre doser har en snabbt insättande effekt enligt vissa fallbeskrivningar. Den vetenskapliga evidensen för en direkt analgetisk effekt av dessa preparat är svag.
Lokalanestetika systemiskt
Systemiska lokalanestetika har länge använts inom smärtmedicinen, både intravenöst och oralt. Det vetenskapliga stödet har dock varit svagt. Inom palliativmedicinen finns fallrapporter om goda effekter av intravenöst lidokain vid opioidrefraktär smärta. Vanligaste användningen är ensamt eller tillsammans med opioid i epidurala och spinala infusioner.
Cannabinoider och medicinsk cannabis
Det vetenskapliga underlaget för behandling med cannabisrelaterad medicin är heterogent och motsägelsefullt. European Pain Federation gav 2018 ut en rekommendation som är baserad på tillgängliga studier och systematiska översikter. Den visar en marginell men statistiskt signifikant skillnad vid behandling av kronisk neuropatisk smärta, vilket ledde till att behandling med cannabisbaserade läkemedel endast rekommenderas mot kronisk neuropatisk smärta som en del av multidisciplinär, multimodal smärtbehandling, och först när rekommenderade förstahands- och andrahandspreparat inte gett tillräcklig smärtlindring eller gett intolerabla biverkningar 538. För alla andra indikationer bör behandling med cannabisbaserade läkemedel betraktas som experimentell, och vid cancerrelaterad smärta anses denna behandling inte ha någon plats, grundat på tillgängliga studier.
Smärtlindrande blockader i palliativ vård
Spinal smärtlindring bör övervägas vid svår smärta när andra behandlingsmetoder inte ger tillräcklig smärtkontroll eller ger oacceptabla biverkningar. Detta möjliggör administrering av lokalanestetika (till exempel bupivakain) ensamt eller i tillägg av opioid. Klonidin kan läggas till för förstärkt effekt. Spinalkatetrar läggs intratekalt av anestesiolog under sterila förhållanden, och katetern tunneleras under huden och kopplas sedan till en läkemedelspump. Med denna behandlingsmetod kan patienten vårdas i hemmet med hjälp av personal inom specialiserad palliativ hemsjukvård eller enheter med liknande kompetens.
För en systematiskt genomgång av intratekal smärtbehandling av cancerorsakad smärta hänvisas till HTA Syd:s rapport 2024:2 (pdf), även publicerad på Statens beredning för medicinsk och social utvärdering (SBU):s webbsida Intratekal behandling av cancerorsakad smärta.
Epiduralkateter kan vara ett alternativ när inga andra behandlingsmetoder fungerar, när kompetens för att lägga en intratekal kateter inte finns tillgänglig eller vid kort förväntad överlevnad. Bäst är dock om även denna tunneleras. Tyvärr försvårar epidural tillförsel fungerande vård utanför sjukhus med tanke på de stora volymer läkemedel som behöver tillföras och som innebär att läkemedelskassetter till vanliga läkemedelspumpar kan behöva bytas flera gånger per dygn.
Neurolytiska blockader, till exempel celiakusblockad vid pankreascancer eller sakralblockad vid rektala eller urogenitala smärtor, används i begränsad omfattning i Sverige men har god evidens i internationell litteratur 539 .
Läkemedelspumpar för smärtlindring
Läkemedelspumpar med opioider används inom specialiserad palliativ vård för att lindra smärta när patienten har svårt att ta perorala läkemedel, har sänkt medvetandegrad eller har svår smärta som gör att hen behöver frekventa extradoser. Dessa pumpar kan ge en kontinuerlig dos och/eller bolusdos. De flesta är godkända för intravenöst bruk men används framför allt subkutant vid palliativa enheter.
För att beräkna bolusdos kan man utgå från tillräcklig extrados (1/6–1/10 av grunddosen) och halvera denna, vilket lär patienten att våga trycka redan vid uppseglande smärta såsom NRS 4–5 utan att hen blir trött. Dosintervallet (kallas även spärrtid) bör då vara kort (var 15:e minut) så att även svårare smärtgenombrott kan hanteras. Har patienten bra effekt av bolusdoser men behöver ta dessa flera gånger varje dygn kan man överväga att öka den kontinuerliga dosen.
Det är viktigt att patienten och/eller de närstående förstår hur pumpen fungerar om bolusdoser ordineras. Om patienten begärt fler doser från pumpen än vad hen fått ska orsaken undersökas. Detta kan till exempel bero på för låg bolusdos, ångest eller opioidinducerad hyperalgesi (OIH). Vaknar patienten av smärta bör den kontinuerliga dosen ökas. Rekommendationen är att pumpen avläses dagligen, helst vid samma tidpunkt. Syftet är att sjuksköterskan ska se om kassetten eller sprutan behöver bytas, och se om dosen ska justeras enligt ovan.
Enklare läkemedelspumpar för subkutant bruk används i livets slutskede när patienten har flera besvärande symtom som behöver lindras genom att olika läkemedel blandas i pumpen. Läkemedel med liknande pH är ofta blandbara och de flesta palliativa läkemedlen är syror. Furosemid och ketorolak är dock baser och går inte att blanda med övriga läkemedel. Vid blandningar kan lösningen spädas med natriumklorid eller sterilt vatten för att minska risken för hudirritation, utfällningar och inkompatibilitet. Det är viktigt att den berörda personalen är bekant med metoden. Tillgången till smärtpumpar varierar mellan olika delar av landet och mellan olika vårdenheter.
Vid konvertering till läkemedelspump bör man ta hänsyn till om smärtan är opioidkänslig samt till den totala dygnsdosen som även inkluderar intagna vidbehovsdoser. Rekommendationen är att följa upp patienter som smärtbehandlas med pump dagligen under de första dagarna efter uppstart eftersom det finns en överhängande risk för både under- och överdosering i konverteringen.
Särskilda smärttillstånd
Skelettmetastaser
Cancerrelaterad skelettsmärta har både en nociceptiv inflammatorisk komponent och en neuropatisk komponent, och det bör man beakta redan från början. Medikamentellt är COX-hämmare (NSAID, COX-2-hämmare och/eller kortison) förstahandspreparat eftersom opioidbehandling sällan ger fullgod effekt på rörelsekorrelerade smärtgenombrott.
Strålbehandling kan vara indicerad i olika sjukdomsskeden och har ofta god effekt mot rörelsekorrelerad smärta till följd av skelettmetastaser. Effekten av strålbehandling ses vanligen efter 2–4 veckor, vilket är viktigt att informera patienten om. Initialt kan smärtan temporärt öka, varför det är viktigt att optimera övrig smärtlindrande läkemedelsbehandling i väntan på strålbehandlingseffekt. Se även avsnitt 14.7 Solida tumörsjukdomar.
Skelettmetastaser (CIBP, ”cancer induced bone pain”) kan behandlas på följande sätt (utan inbördes ordning):
- Onkologer bör särskilt överväga strålbehandling. hormonbehandling, bisfosfonater, denosumab, cytostatikabehandling eller isotopbehandling i smärtstillande syfte för patienter i tidigt palliativt skede.
- I vissa fall kan stabiliserande kirurgi vara av värde, och får diskuteras med ortopeder.
I övrigt kan man överväga behandling med:
- antiinflammatoriska läkemedel såsom COX-hämmare (NSAID, COX-2-hämmare) och/eller kortison
- antiepileptika
- NMDA-receptorantagonist (se avsnitt specialistpreparat)
- tricykliska antidepressiva eller selektiva noraadrenalinsåterupptagshämmare
- opioider
- TENS (transkutan elektrisk nervstimulering)
- anpassad rörlighetsträning.
Patientmedverkan och kommunikation med patient och närstående
Patient, närstående och ansvarig personal bör vara välinformerade om smärtans orsak och bakgrund till valet av behandling. De ska också få möjlighet att diskutera detta 540.
Smärta vid livshotande sjukdom, speciellt i livets slutskede, är kanske den faktor som skapar mest ångest och oro, inte minst hos patienter kort förväntad överlevnad. Det är angeläget att svårt sjuka patienter vet att smärta och andra plågsamma symtom kan lindras, men man kan inte utlova smärtfrihet. Patienten bör tidigt involveras i diskussion om smärtbehandlingens upplägg, med information om förväntade effekter och biverkningar, för att man ska kunna skräddarsy behandlingen. En patient kan till exempel tycka att biverkningar i form av sänkt vakenhet och nedsatt kognitiv förmåga är ett rimligt pris att betala för att uppnå smärtlindring, medan en annan patient vill vara så pigg som det går och då väljer en annan smärtlindring.
Sömnbesvär
Sömnbesvär är vanligt förekommande hos patienter med palliativa vårdbehov, samtidigt som sömnbehovet ofta ökar i samband med svår sjukdom. Sömnbesvären kan bero på den bakomliggande sjukdomen, eller vara sekundära till de symtom som patienten upplever.
Definition, förekomst och orsaker
Sömn och vila är basala behov för alla människor. Vid sjukdom ökar sömnbehovet 541, samtidigt som sömnsvårigheter och sömnrubbningar är vanliga hos patienter med palliativa vårdbehov. Störd nattsömn kan därför leda till att patientens livskvalitet försämras. Sömnlöshet ökar risken för depressioner, som kan bidra till onormal psykisk trötthet och nedsatt kognitiv förmåga. Det kan vara en differentialdiagnos till cancerrelaterad fatigue 542 543 544 .
Patienter med palliativa vårdbehov kan drabbas av sömnstörningar som bland annat beror på smärta, oro för framtiden, illamående, klåda och ångest. Dessa sömnstörningar inverkar negativt på kognitiva funktioner såsom koncentration och minne samt det allmänna välbefinnandet. Personer som vårdas på sjukhus drabbas ofta av sömnstörningar 541, delvis på grund av nattliga kontroller (till exempel kroppstemperatur och saturation), medpatienter, störande ljud och saknad efter hemmet och närstående.
Bedömning, anamnes och undersökningar
Vid sömnbesvär behöver man kartlägga patientens sömnrutiner och avgöra om hen har insomningsproblem och/eller lätt att vakna på natten. Det kan till exempel göras med skattningsformuläret Insomnia severity index (ISI). Anamnesen bör även omfatta eventuella bakomliggande orsaker till sömnbesvären, exempelvis olika symtom eller läkemedelspåverkan. Även omgivningen såsom säng, rumstemperatur eller störande faktorer kan hindra sömnen. För att identifiera bakomliggande orsaker kan en läkemedelsgenomgång vara till hjälp. Även generella symtomskattningsinstrument såsom ESAS-r kan vara en del av utredningen. Se även Kapitel 12 Att arbeta strukturerat med palliativ vård och behandlingsstrategier.
Behandling vid sömnbesvär
Orsaksinriktad behandling
Vid sömnbesvär behandlas i första hand de bakomliggande orsaker som identifierats i utredningen.
Icke-farmakologisk behandling
Omvårdnadsåtgärder
Centralt i omvårdnaden är att identifiera och behandla möjliga orsaker till sömnstörningarna. Till exempel kan smärta, oro och ångest, illamående eller klåda störa nattsömnen. Även viss läkemedelsbehandling såsom kortison kan påverka sömnen. Effektiv symtomlindring och god sömn kan leda till ökad livskvalitet 16545546. Andra åtgärder är att:
- kartlägga sömn och sömnbesvär genom att be patienten att berätta om sitt sömnmönster
- eliminera störande moment nattetid, såsom kontroller om de inte är nödvändiga
- främja avslappning och en lugn miljö för att underlätta insomnandet
- vädra i sovrummet för att få frisk luft och en sval omgivning.
Rehabiliteringsåtgärder
- Instruera och uppmuntra patienten till fysisk aktivitet dagtid, i den mån det är lämplig och möjligt. Prova att underlätta sömn med hjälpmedel såsom vårdsäng, elsängsryggstöd, lyftbåge, tryckavlastande madrass och glidlakan.
- Erbjud att pröva avspänningstekniker och andningsövningar.
Farmakologisk behandling
Exempel på sömngivande eller lugnande läkemedel att prova är:
- tablett zopiklon 5–7,5 mg till natten
- tablett oxazepam 10–15 mg till natten
- tablett propiomazin 25 mg 1–2 till natten (inte lämpligt för äldre)
- tablett mirtazapin 15 mg till natten.
Vid svåra sömnproblem kan neuroleptika som ex klometiazol eller även det starkare sederande Levomepromazin (ej äldre) övervägas. Överväg även kontakt med enhet för specialiserad palliativ vård om symtomen är svårbehandlade.
Beakta följande:
- Vid svåra sömnstörningar eller paradoxal reaktion på bensodiazepiner, pröva levomepromazin 5–25 mg alternativt olanzapin 2,5–5 mg till natten.
- Vid depressiv komponent eller uppvaknande med svårigheter att somna om, pröva tablett amitriptylin 10–30 mg eller tablett mirtazapin 15–45 mg.
- Bensodiazepin kan ge dagtrötthet nästkommande dag om det tas för sent.
- För sköra äldre avråds behandling med antipsykotiska eller antikolinerga läkemedel och långverkande bensodiazepiner. Överväg Klometiazol 300 mg till natten under begränsad tid och i undantagsfall. Det rekommenderas även behandlingsförsök med Melatonin.
- Kortikosteroider kan ge sömnstörning och bör inte tas sent på dagen.
- Utvärdera behandlingseffekten fortlöpande.
Patientmedverkan och kommunikation med patient och närstående
Störd nattsömn påverkar även de närstående som bor ihop med patienten, eftersom de ofta väcks eller hålls vakna. De kan behöva avlastning, vak eller möjlighet att sova åtskilt för att återhämta sig.
Övriga tillstånd
Hyperkalcemi
Malignitet är den vanligaste orsaken till hyperkalcemi. Alla typer av maligniteter kan ge upphov till hyperkalcemi och de vanligaste är bröstcancer, lungcancer, njurcancer och myelom. Cirka 10–30 % av patienterna med spridd cancersjukdom insjuknar i hyperkalcemi någon gång under sjukdomsperioden. Anledningarna kan vara:
- utsöndring av paratyreoidearelaterat protein (PTHrP) från tumör
- ökad osteoklastaktivitet vid skelettmetastaser som leder till ökad bendestruktion
- ökad produktion av D-vitamin från tumör.
Hyperkalcemi kan förekomma utan förekomst av skelettmetastaser och är ofta korrelerat till en dålig prognos 547 (Nationellt vårdprogram Myelom).
Symtom
Hyperkalcemi kan ge symtom från flera olika organsystem, såsom nervsystemet, gastrointestinalkanalen, njurarna och hjärtat. Snabbt uppkommen hyperkalcemi ger mer symtom. Måttlig hyperkalcemi kan ge törst, ökad urinmängd, illamående, förstoppning, trötthet, muskelsvaghet och nedstämdhet. Vid uttalad hyperkalcemi kan patienten även få huvudvärk, kräkningar, förvirring och intorkning samt i grava fall hjärtpåverkan med hypertoni, arytmi, koma, njursvikt och död. QT-tiden förkortas.
Minskat vätskeintag och samtidig njurpåverkan leder till dehydrering (uttorkning) varför uppvätskning är den primära behandlingen. Ofta ses elektrolytrubbningar såsom förlust av natrium, kalium och magnesium. Äldre patienter utvecklar symtom tidigare på grund av känslighet för redan måttlig hyperkalcemi 547.
Utredning
Vid utredning av hyperkalcemi kontrolleras P/S-Ca och albumin eller kalcium-jon. Vid lågt P/S-Ca bör albumin-korrigerat kalcium uträknas eftersom det är vanligt med lågt albumin hos patienter i palliativt skede, vilket innebär att det är viktigt att albuminkorrigera kalciumvärden alternativt ta kalciumjon. Kreatinin, natrium och kalium kan kontrolleras vid risk för uttorkning.
Uttalade besvär ses ofta vid S-Ca > 3,5 mmol/l 548.
Behandling
Uppvätskning är den viktigaste behandlingen av dehydrerade patienter, t.ex. NaCl 9 mg/ml. Vid uppvätskning bör man ta hänsyn till samsjuklighet, såsom hjärtsvikt, och till hur skör patienten är. Peroral vätska kan ersätta intravenös vätska vid måttliga symtom. Behandlingen bör baseras på symtom. Äldre personer är ofta mer känsliga för högt kalcium, och hur snabbt hyperkalcemin uppkommit påverkar symtomgraden. Symtom kan uppkomma vid S-Ca 3,0 och mer uttalade symtom vid S-Ca över 3,4.
Åtgärder vid hypercalcemi:
- Sätt ut eventuella kalcium- och D-vitaminpreparat.
- Uppvätska patienten med 2–3 liter per dygn, om hen tolererar detta. Vätska kan ges genom ökat peroralt intag eller kompletteras med intravenös vätska.
- Kontrollera S-Ca efter 1–2 dygn.
- Efter uppvätskning, ge bisfosfonater intravenöst, i första hand zoledronsyra 4 g intravenöst. Effekt kan ses efter 2–4 dygn, men maximal effekt först efter 4–7 dygn.
- Ge endast furosemid vid symtom på övervätskning.
- Överväg kortisonbehandling vid hematologiska maligniteter.
- Överväg kalcitonin vid vid behov av snabb symtomlindring.
- Överväg denosumab, speciellt vid njursvikt och vid refraktär hyperkalcemi.
När det gäller patienter med en förväntad längre överlevnad kan onkologisk behandling av grundsjukdomen vara aktuell för att behandla orsaken till hyperkalcemin. Diskussion med behandlande läkare kan vara aktuellt (NVP Akut onkologi och NVP Myelom).
När personen närmar sig livets slutskede ökar risken för övervätskning, och man bör vara försiktig vid vätskebehandling. Det finns risk för njurpåverkan vid behandling med bisfosfonater eftersom patienterna kan vara svåra att rehydrera tillräckligt. Nyttan av behandlingen bör i dessa fall vägas mot riskerna. I livets absoluta slutskede (de sista dagarna och sista veckorna) bör hyperkalcemi inte utredas eftersom vätskebehandling då inte ger önskad effekt. Fokus är god symtomlindring.
Länkar
Nationellt vårdprogram (NVP) Akut onkologi
Nationellt vårdprogram (NVP) Akut onkologi, kapitlet Hyperkalcemi
Infektioner
Bakteriella infektioner
Att behandla infektioner kan vara en livsförlängande åtgärd i både tidig och sen palliativ sjukdomsförlopp samt har en symtomlindrande effekt. Vid okomplicerade bakteriella urinvägsinfektioner, luftvägsinfektioner och hudinfektioner väljs peroral behandling. Vid tarmobstruktion eller kraftig cancerväxt i tarmarna kan dock absorptionen vara påverkad och man behöver då välja intravenös administrering även vid okomplicerade infektioner. Odlingar bör alltid tas innan behandling sätts in.
Vid bakteriella infektioner som ger allmänpåverkan med hög feber och/eller påverkade vitalparametrar väljs intravenös behandling. Cefalosporiner täcker de flesta snabbväxande luftvägs- och hudpatogener och är ett bra alternativ i väntan på resistensbestämning. Om man misstänker bukfokus är i stället piperacillin/tazobaktam (4 g x 3–4) förstahandsval.
Vid cefalosporinbehandling i hemsjukvård är ceftriaxon ett praktiskt alternativ eftersom det har lång halveringstid och behöver bara ges som en injektion en gång om dagen. Endosadministrering (1–2 g x 1) frigör mer tid för patienten och innebär färre sjuksköterskeinsatser.
Neutropen sepsis är ett akut tillstånd som kan uppstå under cancerbehandling eller vid kraftig benmärgssuppression, och det behöver handläggas skyndsamt. Risken för att patienten avlider stiger för varje timme som behandlingen fördröjs. Det är viktigt att sätta in bredspektrumantibiotika direkt efter att odlingar har tagits, och man bör inte invänta provsvar. Man bör vid detta tillstånd alltid behandla med antibiotika med god gramnegativ täckning, vanligen piperacillin/tazobaktam (4 g x 4) eller en karbapenem (imipenem eller meropenem i dosering 0,5g–1 g x 4). Det är viktigt att också ge rikligt med intravenös vätska vid tecken på chock, och att överväga övervakning på intensivvårdsavdelning. Trots fullgod behandling med antibiotika och vätska avlider patienter i sepsis, särskilt patienter med kraftig immunsupression, t.ex. vid hematologisk malignitet.
När det gäller antibiotikabehandling i livets absoluta slutskede (de sista dagarna och veckorna) är effekten av behandlingen mer tveksam. Endast vid behandling av urinvägsinfektioner har man kunnat visa god symtomlindrande effekt 549 550. För övriga infektioner är den positiva effekten mer tveksam under de sista dagarna i livet 549 550.
Studier tyder på att det är svårt att diagnostisera bakteriella infektioner i livets slutskede eftersom odlingsresultaten inte alltid stämmer överens med klinisk respons på behandling 551. Därför är värdet av att ta odlingar i livet slutskede (sista dagarna till veckorna) tveksamt.
Om patienten aktivt vill avstå från infektionsbehandling ska man givetvis respektera det.
Virusinfektioner
När immunförsvaret är nedsatt, till exempel under cancerbehandling, vid hematologiska maligniteter och i livets absoluta slutskede, kan latenta virusinfektioner reaktiveras. Ett exempel på detta är bältros (Herpes zoster) som kan ge mycket besvärande symtom. Aciklovir-profylax kan därför vara relevant att bibehålla även i sent palliativt skede hos hematologiska patienter. Om bältros uppstår bör behandling med valaciklovir sättas in och kan lindra och förkorta symtomen. Valacyklovir behöver då sättas in inom 72 timmar från debuten. Infektionen ger ofta svår smärta som har både en nociceptiv och en neuropatisk komponent. I ungefär hälften av fallen kvarstår den neuropatiska smärtan även när infektionen läkt ut. Den nociceptiva smärtan i akutsjukdomsförloppen kan behandlas med paracetamol och vid behov opioider. Mot den neuropatiska smärtan är amitryptilin förstahandsval, och vid otillräcklig effekt kan man pröva gabapentin, pregabalin eller karbamazepin. Även lidokainplåster kan övervägas.
Vid andra virusinfektioner där antiviral behandling saknas ger man sedvanlig symtomlindrande behandling.
Behandling av symtom med kortikosteroider
Kortikosteroider är en grupp läkemedel med många användningsområden för bl.a. patienter med avancerad cancer eller KOL. Verkningsmekanismerna är fortfarande delvis okända men kortikosteroider har en påtaglig antiinflammatorisk effekt, som utnyttjas vid bland annat smärtbehandling. Vid förhöjt intrakraniellt tryck och ryggmärgskompression minskar kortikosteroider svullnad runt tumörer. Kortikosteroider är också viktiga vid behandling av illamående och kräkningar pga. cytostatikabehandling 552. Vid KOL-exacerbationer förbättrar perorala kortikosteroider andningsfunktionen, minskar symtomen och förkortar sjukdomsperioden (ref Woods).
Flera olika kortikosteroider används, varav betametason är den mest använda inom palliativ vård i Sverige. Ett skäl är den höga antiinflammatoriska effekten och lägre risk för vätskeansamling jämfört med andra kortikosteroider. Olika kortikosteroider har olika antiinflammatorisk effekt, halveringstid och dosekvivalens, vilket ska beaktas vid byte av preparat, se tabellen nedan. Betametason och dexametason anses vara likvärdiga men bra evidens saknas 553.
Tabell 9. Beskrivning av olika kortikosteroider
|
Steroid |
Antiinflammatorisk effekt |
Mineralkortikoideffekt |
Ekvivalent glukokortikoid dos |
Effektduration, timmar |
|
Hydrokortison |
1 |
Ja, dosrelaterad |
20 mg |
8–12 |
|
Prednisolon |
3 |
Lite |
5 mg |
12–36 |
|
Betametason |
25 |
Nej |
0,6 mg |
36–72 |
|
Dexametason |
25 |
Nej |
0,75 mg |
36–72 |
|
Metylprednisolon |
5 |
Nej |
4 mg |
36–72 |
Referens till behandling med kortikosteroider i tabellen ovan. 554
Bedömning, anamnes och undersökning
Vid avancerad cancersjukdom kan många symtom lindras med kortikosteroider:
- illamående och kräkningar: vid onkologisk behandling är kortikosteroider en viktig del av behandlingen 555 ; vid avancerad sjukdom har kortikosteroider använts som tillägg när annan behandling inte gett effekt, men effekten är oklar 556
- trötthet (fatigue) 557
- minskad aptit 552
- strålinducerad pneumonit (inflammation, ej infektion), ibland med tillägg av antibiotika (NVP Lungcancer)
- andnöd (dyspné) – kortikosteroider kan ha effekt hos en del patienter, som vid tumörsvullnad eller KOL 180 397
- vena cava superior-syndrom (tumör som trycker på ett stort blodkärl eller blodpropp i blodkärlet i bröstkorgen) (se kapitel Vena cava superior-syndrom i NVP Akut onkologi)
- smärta – kortison kan ha en tilläggseffekt till annan smärtlindring 552 (se avsnitt 15.13 Smärta)
- förhöjt intrakraniellt tryck vid hjärntumörer eller hjärnmetastaser, högdos kortikosteroider 552 (se kapitel Hjärnmetastaser/hjärntumörer i NVP Akut onkologi)
- ryggmärgskompression 552 (medullakompression, högdos kortikosteroider) (se kapitlet Ryggmärgskompression i NVP Akut onkologi)
- ileus om icke operabelt 552. Hänvisas till kirurgiska åtgärder under avsnitt 16.3 Subileus och ileus.
Vid avancerad KOL blir akuta exacerbationer allt mer frekventa och allt svårare när sjukdomen förvärras:
Inhalerbara kortikosteroider i kombination med långverkande bronkodilatorer kan minska frekvensen av exacerbationer. Risken för pneumonier ökar vid tillägg av kortikosteroider, vilket bör uppmärksammas 558.
Perorala kortikosteroider rekommenderas vid akuta exacerbationer av KOL 362.
Biverkningar
Kortikosteroider ger många biverkningar från olika organsystem så behandlingen behöver noga övervägas, framför allt när patienten har en längre förväntad överlevnad. Högre dos och längre behandling ökar risken för biverkningar. Kroppens egen kortisolproduktion påverkas vid insättning av kortikosteroider; om kortikosteroider ges under mer än 10–14 påverkas binjurebarkens produktion av kortisol så att den egna produktionen inte alltid kommer igång optimalt och långsam nedtrappning av kortikosteroider rekommenderas. Vissa biverkningar kan uppstå efter kort tids användning av kortison, till exempel oral candida och förhöjt blodsocker, medan bland annat osteoporos uppstår efter längre tids användning men kan uppkomma redan efter 3–6 månader. Biverkningar bör monitoreras aktivt hos alla som behandlas med kortikosteroider i längre tid än 14 dagar 552 .
Biverkningar av kortikosteroider kan vara:
- infektioner eftersom kortikosteroider hämmar immunförsvaret 552, t.ex. pneumocystis jirovecii och oral candida 552
- högt blodsocker, försämrad diabeteskontroll 552
- försämrad sårläkning, vilket är viktigt att beakta hos nyopererade patienter (internetmedicin kortikosteroider)
- muskelsvaghet (myopati) framför allt i överarmar och lår, kan uppkomma inom 2 veckor efter insättning 552
- risk för benskörhet (osteoporos) efter längre tids användning, kan uppkomma redan efter 3–6 månader
- gastrit och ulcus: liten risk vid enbart behandling med kortikosteroider, men ökad risk vid spridd cancersjukdom, tidigare ulcus och samtidig användning av COX-hämmare (antiinflammatoriska läkemedel) 559
- psykiatriska biverkningar såsom eufori, insomningssvårigheter, psykos, depression och förvirringstillstånd 559
- endokrina effekter såsom nedsatt funktion av binjurebarken efter 10–14 dagar; efter längre behandling kan för snabb nedtrappning leda till kortisolbrist med allmän trötthet, svaghet och lågt blodtryck 559.
Behandling
Behandlingstiden ska vara så kort som möjligt och dosen den lägsta möjliga som fortfarande ger symtomkontroll. Initialt kan högre doser behövas, men vid god effekt trappas dosen ner och behandlingen sätts om möjligt ut inom 2 veckor. Vid utsättningssymtom bör man återgå till en dos som är högre än den som innebär att patienten upplever symtom. Därefter trappas dosen ner i långsammare takt. Vid hjärnmetastaser, hjärntumörer och ryggmärgskompression är det sällan aktuellt att helt trappa ut kortikosteroider, om inte ursprungsorsaken är behandlad.
Hos patienter med en förväntad längre överlevnad bör man beakta att effekten av kortison är tidsbegränsad och risken för biverkningar stor, varför behandlingstiden för kortison bör begränsas om möjligt. Vid infektion, höj dosen eller återinsätt kortikosteroider om patienten stått på sådan behandling i månader 560 . Om patienten stått länge på kortison kan binjurebarken svikta så att kortisolhalten i blodet inte ökar. En ökad dos kortikosteroider kan minska patients symtom. Vid oral candida rekommenderas behandling med i första hand flukonazol 100–200 mg i 1 vecka eller enligt odlingssvar. Profylax mot oral candida rekommenderas inte. Symtom som beror på högt blodsocker kan uppkomma vid B-glukos > 15–20. Ge i första hand kortverkande insulin vid behov. Vid upprepat behov av kortverkande insulin, överväg att sätta in långverkande insulin. Blodsockret bör mätas under eftermiddagen, då värdet är som högst. Vid långvarig kortisonbehandling, > 3 månader, överväg behandling med D-vitamin och kalk, och vid osteoporos eventuellt behandling med bisfosfonater 561 . Vid gastritsymtom rekommenderas i första hand protonpumpshämmare peroralt eller annars intravenöst.
När personen närmar sig livets slutskede bör risken för biverkningar inte begränsa användningen av kortikosteroider. Vid allvarlig infektion, överväg att öka dosen så som vid längre förväntad överlevnad. Vid oral candida rekommenderas god munhygien och läkemedel mot oral candida om det kan ge effekt. Vid högt B-glukos ska insulin ges endast vid symtomgivande hyperglykemi. Blodsockerkontroller bör avslutas om patienten inte gagnas av dem. Besvärande gastritsymtom kan behandlas med protonpumpshämmare, peroralt eller intravenöst. Den antiinflammatoriska effekten och effekten på ödem av kortikosteroider kan komma inom 24 timmar, varför behandling kan vara aktuell sent i livet 562.
I livets absoluta slutskede är det sällan nödvändigt att fortsätta med kortikosteroider pga. den relativt långa halveringstiden 553 (Internetmedicin glukokortikoider). Vid frekventa kramper pga. tumör i CNS kan kortison ges som subkutana injektioner 1 gång per dygn.
Länkar
Nationellt vårdprogram (NVP) Lungcancer
Nationellt vårdprogram (NVP) Akut onkologi
Internetmedicin: Glukokortikoider, farmakologisk behandling (”kortisonbehandling”) – vuxna (internetmedicin.se)
Internetmedicin: Kroniskt obstruktiv lungsjukdom (KOL) (internetmedicin.se)
Symtomgivande blödningar
Blödning förekommer hos 10 % av patienterna med avancerad cancersjukdom och hos 30 % av dem med hematologiska maligniteter. Det kan röra sig om allt från sivande kontinuerliga blödningar eller återkommande större blödningar, till terminala arteriella blödningar vid exempelvis huvud- och halscancer eller cervixcancer. Blödningar kan vara relaterade till lokal tumörväxt, onkologisk behandling såsom strålbehandling och cytostatikabehandling samt tumörens kärltillväxt. Både synliga blödningar och blödningar inne i kroppen förekommer 563. Vissa läkemedel kan öka blödningsrisken, t.ex. COXhämmare, trombocythämmande läkemedel såsom acetylsalicylsyra (ASA), antikoagulantia, kortison och vissa onkologiska läkemedel såsom bevacizumab 564. Även antidepressiva (SSRI) kan öka blödningsrisken pga. trombocytpåverkan, speciellt i kombination med andra läkemedel som ökar blödningsrisken 565.
Även patienter med andra sjukdomar har ökad risk för blödning, t.ex. patienter med leversjukdomar, koagulopatienter och patienter med lågt TPK. Hög ålder och ökad skörhet innebär ökad risk för fall, vilket i sin tur kan leda till blödningar, framför allt hos patienter med läkemedel som ökar blödningsrisken 563.
Vid risk för blödning bör man redan i tidig palliativ sjukdomsförlopp involvera patienten och de närstående och fråga efter deras önskemål med vården. Vid framför allt akuta blödningar är det viktigt att basera omhändertagandet på i vilket sjukdomsskede patienten befinner sig och vad eventuella åtgärder kan göra för nytta. Det är viktigt att bedöma patientens prognos och allmäntillstånd, och avgöra vilken insatsnivå som kan vara bäst, gärna i dialog med både patienten och den behandlande kliniken.
I tidigt palliativt skede ska akut omhändertagande vara aktivt med målet att stoppa blödningen. Vid akuta blödningar i sent skede ska symtomlindrande behandling prioriteras. Om det finns risk för arteriell blödning från tumör i huvud- och halsområdet är det viktigt att patienten och de närstående är informerade och att nödvändiga förberedelser är gjorda, se Kapitel 18 566.
Symtom
Blödningssymtomen beror på hur stor blodförlusten är och hur länge den pågår. Mindre blödningar med anemi som följd kan leda till trötthet, sänkt ansträngningskapacitet, minskad aptit, yrsel, huvudvärk, tinnitus och nedsatt kognitiv förmåga. Patienter med hjärtsjukdomar har större risk för symtom på grund av sänkt kompensatorisk förmåga. Större akuta blödningar ger takykardi, ortostatisk hypotension och dyspné samt kan leda till cirkulatorisk chock.
Vanliga orsaker till blödning i palliativt skede:
- Övre mag-tarmblödning: blodig kräkning (hematemes), svart avföring (melena), illamående.
- Nedre tarmblödning: färskt blod per rektum i form av blodig eller rödfärgad avföring (hematochezi). Kan också bero på en omfattande blödning i övre mag-tarmkanalen.
- Näsblod.
- Blödning från tumör i huvud-halsområdet (tumör på halsen som infiltrerat stora kärlen): riklig pulserande blödning.
- Blödning från tumör i bronkerna eller lungorna: blodiga upphostningar (hemoptys).
- Blödning från gynekologiska tumörer, framför allt cervix- och vulvacancer: blödning antingen från underlivet alternativ metastas i området.
- Blödning från tumör som infiltrerar de stora kärlen ger en riklig pulserande blödning
- Blödning från tumör i njure, urinblåsa eller prostata: synligt blod i urinen (makroskopisk hematuri), urinretention.
- Intrakraniella blödningar: huvudvärk, förvirring, trötthet (somnolens), medvetslöshet.
En blödning kan vara en förvarning om allvarligare blödningar, så blödningar bör alltid bedömas skyndsamt. Eventuella förebyggande åtgärder bör övervägas, och patienter och närstående bör informeras om risk för nya blödningar och hur dessa ska hanteras.
Behandling
Vid en större blödning hos en patient som inte bedöms vara i livets slutskede:
- Bedöm och behandla patienten skyndsamt.
- Fatta beslut om vårdnivå utifrån prognos och allmäntillstånd. Om detta är diskuterat med patienten tidigare, respektera patientens beslut.
- Överväg intravenös vätskebehandling vid stor blodförlust.
- Applicera tryck på blödningskällan om det är möjligt.
- Kontrollera blodstatus, blödningsstatus och bastest om det finns indikation för transfusion med erytrocyter eller trombocyter.
- Överväg tranexamsyra, men behandla med stor försiktighet vid blödning från urinvägarna.
- Överväg all-rac fytomedadion (Konakion Novum) om patienten står på warfarin, och antidot vid DOAK-behandling, om det finns tillgängligt.
- Vid en tumörblödning, kontakta onkolog vid behov eftersom till exempel palliativ strålbehandling kan ha långtidseffekt mot blödningar.
- Sklerala blödningar (blödningar i ögonvitan) behöver inte åtgärdas.
- Vid arteriell blödning från tumör i huvud-halsområdet hos patienter med obotlig sjukdom, se nedan.
Vid mindre blödning eller risk för blödning:
- Ta ställning till att sätta ut läkemedel som ökar blödningsrisken, och överväg att ge eventuella antidoter vid warfarin- eller DOAK-behandling (direktverkande orala antikoagulantia).
- Överväg att byta COX-1 hämmare till COX-2 hämmare.
- Överväg att sätta in protonpumpshämmare vid risk för blödning i mag-tarmkanalen eller samtidig behandling med COX-hämmare och/eller kortison.
- Överväg att sätta ut eller trappa ner antidepressiva (SSRI).
- Vid hosta, överväg hostdämpande läkemedel.
- Överväg tranexamsyra peroralt, intravenöst eller lokalt vid blödning. Det ger ingen ökad risk för tromboser. Lokal behandling med tranexamsyra kan användas tex vid blödning från tumörsår, munslemhinna eller näsa.
- Följ trombocytnivån. Vid trombocyter <10 eller vid blödning bör man överväga transfusion. Ta vid behov ställning till annan transfusionsgräns vid ökad blödningsrisk såsom feber.
Om patienten befinner sig i livets absoluta slutskede och drabbas av en akut större blödning:
- Stanna hos patienten.
- Behåll lugnet.
- Applicera tryck på blödningskällan om det är möjligt.
- Använd mörka handdukar.
- Om tid finns, ge läkemedel:
- Midazolam 5 mg/ml 1–2 ml intravenöst, subkutant eller nasalt.
- Upprepad dos kan ges efter 5–10 minuter.
- Opioder vid smärta intravenöst eller subkutant.
- Ta hand om de närstående.
Vid mindre blödning eller risk för blödning gör man samma överväganden kring läkemedel som i tidigare palliativa skeden.
Om det finns risk för större blödning bör man förbereda rummet eller bostaden. Patienten och de närstående bör om möjligt vara informerade om blödningsrisken. Mörka handdukar och läkemedel att ge vid akut blödning ska finnas tillgängliga. En plan för omhändertagandet bör tas fram tillsammans med patienten och de närstående. Närstående kan vid behov ge läkemedel och känna sig förberedda på eventuell blödning. Om patienten avlider i en akut större blödning ska de närstående få stöd och utrymmet där patienten befunnit sig ska städas. De närstående ska också följas upp efteråt.
Länkar
Tromboembolism
Tromboembolism omfattar alla former av venös tromboembolism och de vanligaste formerna är djup ventrombos (DVT) och lungemboli. Patienter med cancer har sju gånger högre risk för att få tromboser än andra, och trombos bedöms vara en vanlig orsak till död hos patienter med cancer. Cirka 1 av 200 cancerpatienter per år drabbas av trombos. Risken för trombos är högst vid pankreascancer, hjärntumör, ventrikelcancer, blåscancer, gynekologisk cancer och lungcancer. Andra riskfaktorer är spridd cancersjukdom, immobilisering, större kirurgi och central venkateter. Vissa antitumorala behandlingar såsom cytostatikabehandling och hormonella behandlingar ger också ökad risk. Återfallsrisken för trombos är hög, vilket motiverar livslång behandling vid kvarvarande cancersjukdom.
Risken för tromboembolier ökar kraftigt med åldern. Riskfaktorer för tromboembolism är tidigare trombos, immoblisering, malignitet, koagulationsrubbningar, kirurgi, gipsbehandling, trauma, infektioner och hjärtsvikt.
Symtom
Symtom av tromboembolism beror på lokalisation men patienten kan vara relativt symtomfri. Många har symtom som kan misstolkas som infektion, t.ex. pneumoni eller rosfeber.
DVT ger främst svullnad, ömhet, rodnad och värmeökning (arm eller ben).
Lungemboli ger främst bröstsmärta, dyspné, hemoptys (lunginfarkt) och hjärtklappning.
Utredning
Utredningen bör inkludera
- pulsoximetri
- blodstatus, PK(INR), APT-tid, leverstatus, S-kreatinin
- proximalt ultraljud
- DT med venös angiografi.
- Hos patienter utan malignitet kan Wells score användas och vid Wells score <2 kan D-dimer bli aktuellt.
Behandling
Akut skede
I akut skede för patienter med cancersjukdom rekommenderas i första hand lågmolekylärt heparin (LMH) eller direktverkande orala antikoagulantia (DOAK, termen NOAK kan också användas). För patienter utan cancer rekommenderas DOAK i första hand. Vid cancersjukdom bör man undvika warfarin på grund av högre risk för blödning och sämre effekt. Warfarin bör endast användas i undantagsfall, såsom vid mekanisk klaffprotes. LMH kan kräva dosjustering efter en viss tid. Vid avvikande S-kreatinin, TPK eller blödning, se Sjukdomsförlopps och konsultera vid behov en koagulationskonsult. Hos äldre personer utan malignitet men med eGFR <25 ml/min kan warfarin vara ett alternativ, och ska ges samtidigt med LMH i minst 5 dagar tills PK(INR) är terapeutiskt. DOAK bör undvikas om patienten har svårt att ta läkemedel peroralt samt vid lågt TPK, njursvikt och låg kroppsvikt.
Vid cancersjukdom är DOAK jämförbara med LMH. DOAK har enligt vissa studier bättre effekt för att förhindra återfall men ger däremot en ökad risk för större blödningar. DOAK ska undvikas vid gastrointestinal cancer och i vissa fall vid urologisk cancer pga. ökad blödningsrisk samt vid hjärntumörer och hjärnmetastaser av samma skäl. 567. Reverserande läkemedel saknas för de flesta preparaten. Valet av preparat kan diskuteras med koagulationskonsult.
Stödstrumpor kan vara indicerade vid DVT.
Profylax
Profylax vid cancersjukdom rekommenderas normalt inte. Vid kirurgi bör profylax ges enligt riktlinjer.
Fortsatt behandling
Hos patienter med spridd malignitet rekommenderas livslång behandling med antikoagulantia, vid både DVT och lungemboli. För patienter utan malignitet rekommenderas behandling i minst 3 månader vid DVT i underbenet, minst 6 månader vid DVT ovanför knäet och minst 12 månader vid återkommande DVT. Vid lungemboli rekommenderas behandling i minst 6 månader och vid återfall bör behandlingen pågå livet ut.
Var observant på TPK, s-kreatinin och kroppsvikt vid pågående onkologisk behandling.
Behandling med antikoagulantia kan fortsätta i livets slutskede om det inte finns kontraindikationer. Var observant på s-kreatinin, TPK, viktnedgång och blödningsrisk. Blödningsrisken ökar under det sista året i livet för patienter med palliativt förlopp. Behandlingseffekten bör därför värderas i förhållande till blödningsrisken 192.
I livets absoluta slutskede bör antikoagulantiabehandlingen utvärderas utifrån risken för tromboembolisk händelse. Vid trombos långt tillbaka i tiden bör behandlingen sättas ut.
Vid nylig lungemboli eller symtomgivande DVT kan fortsatt behandling vara indicerad eftersom det annars finns risk för att symtomen återkommer. I dessa fall bör lågmolekylärt heparin användas. Om patienten får en blödning, och behandlingen är nödvändig, kan dosen sänkas. En 2-dosbehandling kan minska risken något för blödning. Vid stor risk för blödning ska behandlingen sättas ut.
