Primär behandling
Cytostatikabehandling
Rekommendationer
- CUP bör behandlas vid eller i samråd med onkologisk klinik med stor erfarenhet av att behandla CUP samt omfattande erfarenhet av att behandla flertalet cancerdiagnoser.
- Evidensgrunden för regimval är svag.
- Kombinationsbehandlingar bör väljas framför singelbehandling.
- Erfarenheten tyder på att sannolik histogenes bör styra regimvalet. Om sådan vägledning saknas kan man överväga kombinationsbehandling, till exempel taxan–platinabaserad behandling eller platinum-gemcitabin.
- Andra linjens behandling har ännu lägre evidens. Målinriktad behandling kan vara aktuell i utvalda fall där kriterierna för den specifika behandlingen är uppfyllda.
Figur 3.Flödesschema för behandling av patienter med cancer utan känd primärtumör (CUP)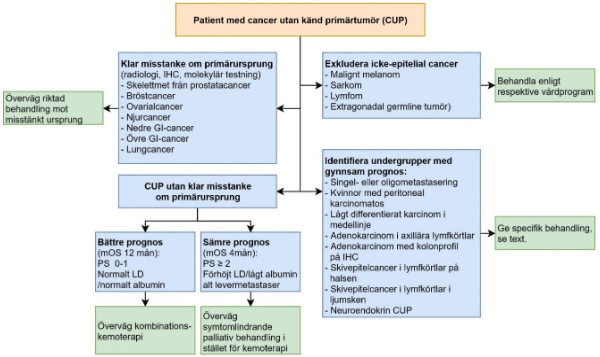
Källa: Modifierad utifrån ESMO Guidelines 2015 24. IHC = immunhistokemisk undersökning,
mOS = medianöverlevnad, PS = performance status, LD = laktatdehydrogenas.
Patienter med CUP bör behandlas inom onkologisk verksamhet med erfarenhet av denna diagnosgrupp. Då patienterna med CUP är mycket få, kan man inte förväntas ha den nödvändiga erfarenheten att behandla dessa vid mindre kliniker. Behandling bör ske vid större kliniker med bred onkologisk kompetens av såväl vanliga som mer ovanliga cancerdiagnoser. Detta ger möjlighet till en god samlad bedömning av såväl kliniska fynd, radiologi, patologi samt onkologisk kompetens om tillgängliga behandlingsmöjligheter. Dessa patienter bör diskuteras multidisciplinärt av ett team med erfarenhet av CUP och onkologer som kan värdera nytta av behandling, kloka och rimliga behandlingsval och, om möjligt i utvalda fall, diskussion på Molecular tumour board eller interna forum för behandling på svaga evidensgrunder.
Organspecifik CUP
Enligt vårdprogramgruppen är det viktigt att identifiera undergrupper av CUP med gynnsam prognos som bör få särskild behandling. Se tabell 2.
Tabell 2.Behandling för patienter med CUP med god prognos 24
|
Undergrupp |
Föreslagen behandling |
|
Högt differentierad neuroendokrin CUP |
Somatostatinanaloger, streptozocin + 5fu, sunitinib, everolimus |
|
Peritoneal adenokarcinom hos kvinnor, särskilt serös papillär histologisk typ av seropapillärt adenokarcinom där primärtumören inte hittats i gynområdet, brösten eller GI-kanalen 2526. Rapporter finns också om tillståndet hos män 4, där cytostatikabehandling ger långtidsremission. |
Optimal cytoreduktiv kirurgi och taxan-platinabaserad kombinationsbehandling |
|
Isolerad axillmetastas av adenokarcinom hos kvinnor |
Axillär kirurgi, mastektomi, strålbehandling och postoperativ cytostatikabehandling och hormonell behandling 2728 |
|
Skivepitelcancer i halskörtel |
Behandlas som huvud-hals-CUP. Nack-dissektion och/eller strålbehandling +/- samtidig platinumbehandling |
|
Lågt differentierad neuroendokrin CUP |
Platinum + etoposid |
|
CUP med kolorektal immunhistokemi |
Systemisk behandling enligt NVP Tjock- och ändtarmscancer |
|
Singel- eller oligometastaserad sjukdom |
PET-DT rekommenderas. Resektion och/eller strålbehandling +/- systemisk behandling. Ablativ behandling bör övervägas om patienten utifrån komorbiditet och allmäntillstånd bedöms ha nytta av ingreppet 29. |
|
Män med skelettmetastas eller tydligt förhöjt PSA |
Behandling enligt NVP Prostatacancer 30 |
Vävnadsspecifik CUP
I de fall där det går att misstänka ett sannolikt ursprung utifrån kliniska, radiologiska och patologiska fynd bör patienterna behandlas enligt gällande vårdprogram för den tumörtypen. För att tydliggöra detta har vårdprogramgruppen valt att benämna denna undergrupp ”vävnadsspecifik CUP”. För t.ex. en CUP med kolorektala molekylära egenskaper, kolorektal-CUP, finns rapporter om att regimer för kolorektalcancer har större effekt än taxan-platinabaserade CUP-kombinationer 3132. Detsamma gäller CUP med annat vävnadsspecifikt ursprung såsom lungcancerliknande CUP och njurcancerliknande CUP.
Singel- och oligometastatisk CUP
Singel- eller oligometastatisk sjukdom har bättre prognos av ablativ behandling, varför detta bör övervägas om patienten utifrån komorbiditet och allmäntillstånd bedöms ha nytta av ett sådant ingrepp 29.
Vidare finns ytterligare några undergrupper med god prognos, för vilka det finns behandlingsrekommendationer 433:
- Lågt differentierad cancer med mediastinal och/eller paraaortal lymfkörtelmetastasering bör behandlas som extragonadal germinalcellscancer med en platinabaserad cytostatikaregim 34. Alla dessa är dock inte germinalcellscancer 30.
- Odifferentierad malignitet som inte kan klassas immunhistokemiskt kan eventuellt behandlas som lymfom i samråd med hematolog eller lymfomonkolog.
- Lymfkörtelmetastasering i ljumsken bör behandlas med första linjens strategi. Se avsnitt 10.1 Kirurgi vid CUP.
Äkta CUP
CUP utanför ovanstående kategorier innebär generellt sett dålig prognos. Det saknas vetenskapligt underlag för behandlingseffekt av antitumoral behandling vid performance status 3 och 4.
Multivariata analyser anger att negativa faktorer för överlevnad framför allt är dåligt allmäntillstånd, levermetastasering och höga nivåer av LD 3335.
Även hypoalbuminemi påverkar prognosen negativt 7. Andra tillstånd med dålig prognos är metastaser i mediastinala lymfkörtlar eller skelett, icke-papillär malign ascites och multipla hjärnmetastaser 4. Man bör i varje enskilt fall noggrant väga chansen till nytta mot de risker som cytostatikabehandling innebär. När riskerna överväger nyttan bör man avstå aktiv onkologisk behandling. Vården bör då i stället inriktas på symtomlindrande palliativ behandling för att optimera livskvaliteten.
Det vetenskapliga underlaget som ligger till grund för val av cytostatikabehandling vid CUP är begränsat. Det finns få fas 3-studier, och aktuella studier omfattar i regel ett litet antal patienter. Ofta har patienter med särskilt god prognos inkluderats.
Om ursprunget till sjukdomen inte går att påvisa bör en kombination av taxan och platina användas. Vårdprogramgruppen föreslår karboplatin-paklitaxel i första hand eftersom denna kombination är väl tolererad. Oftast ger cytostatikabehandling måttlig effekt 333637.
Kombinationen taxan–platina förbättrar sannolikt även resultaten för patienter med CUP som inte ingår i undergrupperna med god prognos 4. I en randomiserad studie påvisades bättre överlevnad och bättre tolerans efter taxan–platinabaserad behandling än efter gemcitabin-vinorelbin 35.
Singelbehandling används sällan vid CUP eftersom svarsfrekvensen är mycket låg. Studier visar att behandling med fluorouracil, cisplatin, metotrexat eller doxorubicin som ensamt läkemedel uppvisar en svarsfrekvens på mindre än 20 % 33. Tidiga kombinationsregimer med fluorouracil och/eller doxorubicin gav en svarsfrekvens på cirka 20 % med medianöverlevnad på ett drygt halvår. Det fanns dock inget samband mellan svarsfrekvens och medianöverlevnad. Andelen kompletta remissioner var låg 436.
Andra linjens behandling har inte varit framgångsrik. Dåligt svar på cisplatin–taxan ansågs i en studie kunna bero på gastrointestinalt tumörursprung, och därför har oxaliplatin–kapecitabin provats, med svarsfrekvens på 13 % och mediantid till progression på bara 2 månader 38. Kombinationen docetaxel–gemcitabin efter cisplatinbaserad första linjens behandling gav en svarsfrekvens på 28 % och en medianöverlevnad på 8 månader från insättandet 36.
Om möjligt bör patienter i gott allmäntillstånd erbjudas deltagande i en klinisk studie.
Målinriktad behandling
Målinriktade behandlingar mot tumörspecifika avvikelser har blivit ett allt vanligare inslag vid behandling av cancer. Då fallen av äkta CUP är få, är det vetenskapliga underlaget för att behandla denna patientgrupp med målinriktad behandling mycket begränsat. Äkta CUP har generellt sett en dålig prognos. Många av patienterna är äldre med dåligt performance status vid diagnos och de blir därför inte föremål för onkologisk behandling. De patienter som är aktuella för behandling bör skötas på en onkologisk enhet med stor erfarenhet av diagnosgruppen. Patienter som kan vara aktuella för andralinjens behandling är således mycket liten, i utvalda fall kan man överväga målinriktad behandling för denna grupp. Hos patienter med vävnadsspecifik CUP kan målriktad behandling vara aktuell i enlighet med gällande vårdprogram för den specifika diagnosen.
Under de senaste åren har målriktade behandlingar mot tumörspecifika avvikelser som till exempel NTRK-hämmare vid NTRK-fusionsgen blivit godkända 3940. I de fall behandlingar avser solida tumörer oberoende av diagnos kan de även vara aktuella till patienter med äkta CUP i de fall de uppfyller kriterierna.
För flertalet målinriktade behandlingar finns ingen indikation för att behandla patienter med äkta CUP. I de fall där tumören uppvisar behandlingsbara avvikelser, som t.ex. BRAF-hämmare vid BRAF V600E-mutation 4142 eller immunterapi vid. MSIH, dMMR, TMBH eller högt PD-L1 4344, blir användandet av dessa behandlingar utanför indikation. De bör handläggas förankrat i verksamheten enligt lokal rutin för off-label behandling.
För immunterapi finns några små studier där patienter med CUP finns inkluderade. I en fas 2-studie med nivolumab vid CUP sågs tendenser till ökad sjukdomsfri överlevnad och total överlevnad, men detta var inte signifikant 45. I en annan fas 2-studie med pembrolizumab, där man inkluderade 25 patienter med CUP som progredierat på tidigare systemisk behandling, såg man respons hos 20 % av patienterna 46.
Strålbehandling
Rekommendationer
- Strålbehandling bör övervägas vid regional- eller oligometastatisk CUP om kirurgi inte bedöms vara lämpligt.
- Strålbehandling bör ges mot metastaser i symtomlindrande syfte, och kan vara aktuellt för patienter som inte tål annan behandling.
- I vissa fall av oligometastatisk intra- och extrakraniell sjukdom kan precisionsstrålbehandling ge en god balans mellan påfrestningar, resursåtgång och den begränsade chansen till lindring eller bot.
En internationell jämförelse tyder på att strålbehandling är underutnyttjad vid CUP i Sverige.
Strålbehandling vid CUP ska användas enligt liknande principer som vid andra tumörformer, men det är svårare att besluta om dosval efter förmodad strålkänslighet.
Kurativ strålbehandling
Vid singel- eller oligometastatisk sjukdom kan precisionsstrålbehandling vara aktuellt, även i kurativt syfte som ett alternativ när kirurgi inte är möjligt.
Postoperativ strålbehandling bör erbjudas efter kurativt syftande kirurgi om kirurgins radikalitet inte kan garanteras. Detta kan t.ex. vara fallet vid lymfkörtelkirurgi där det inte är radikalt makro- eller mikroskopiskt. Strålbehandlingen bör då ges utifrån förmodat spridningsmönster lokoregionalt och med marginal täcka området för tveksam radikalitet. Vid kirurgi av hjärnmetastaser kan postoperativ strålbehandling erbjudas mot operationshålan om övrig tumörsjukdom bedöms vara under god kontroll eller om det var en solitär hjärnmetastas.
Palliativ strålbehandling
Palliativ strålbehandling vid CUP används som vid andra maligniteter.
I en internationell bedömning uppskattades att cirka 25 % av patienter med CUP per indikation behandlades med strålbehandling av skelett- eller lymfkörtelmetastaser, och 6 % för hjärnmetastaser.
Skelettmetastaser
Strålbehandling vid skelettmetastaser är en viktig palliativ åtgärd, liksom vid skelettmetastaser av känd primärtumör. Det finns inga data som talar för att använda något annat än engångsfraktionering med 8 Gy när indikationen är smärtlindring.
I olika studier har behovet av strålbehandling mot i första hand skelettmetastaser varierat mellan 53 % och 70 %. I en svensk genomgång hade dock endast 29 % fått strålbehandling. Palliativ strålbehandling bedöms därför vara underutnyttjat i Sverige.
Intrakraniella metastaser
Nyare prospektiva studier 47visar att strålbehandling av hela hjärnan har begränsad nytta, och patienten har ofta kvarstående behov av steroider för symtomlindring.
Cirka 10 % av alla hjärnmetastaser kommer från CUP. De flesta hjärnmetastaser härstammar från andra cancerformer såsom lungcancer, bröstcancer, cancer i urinvägarna eller melanom.
Vid begränsad hjärnmetastasering kan kirurgi alternativt strålbehandling med stereotaktisk teknik (SRT) övervägas. Vid enbart hjärnmetastaser är kirurgi att föredra eftersom det även ger möjlighet till PAD.
Efterföljande helhjärnsbestrålning efter SRT eller kirurgi är omdiskuterat. Det förlänger inte överlevnaden men ger en minskad återfallsfrekvens. Det är dock tveksamt om det uppväger risken för kognitiva biverkningar 4849.
Medullakompression
För akut handläggning av medullakompression, se Nationellt vårdprogram för akut onkologi.
Vid konventionell strålbehandling för medullakompression vid CUP fann man ingen skillnad mellan kort behandling (8 Gy x 1−4 Gy x 5) och lång behandling (3 Gy x 10–2 Gy x 20) eftersom medianöverlevnaden var kort, 4 månader. Den längre behandlingen tycks dock ge bättre lokal kontroll vid begränsad sjukdom hos patienter med långsam symtomutveckling som förmodas leva längre 50. Vårdprogramgruppen rekommenderar därför flerfraktionsregimer i de senare fallen.
