Kännetecken och tidig utredning
Rekommendationer och evidens
- Upptäckt i tidigt tumörstadium har stor betydelse för att minska dödligheten i melanom. (+++)
Man bör misstänka melanom vid kliniska fynd av en fläck eller knuta (oftast pigmenterad) som:
- är nytillkommen
- har ökat i storlek
- har förändrat sin färg
- har förändrad form
- inte liknar övriga fläckar eller knutor på huden
- växer snabbt, är fast i konsistensen och är upphöjd.
Ofta är ett melanom helt symtomlöst i tidigt skede. Förändringarna som beskrivs ovan bör därför tidigt väcka misstanke om hudmalignitet även om patienten inte har fysiska symtom. Förlust av ögonfransar i ögonlockskanten kan också vara ett tecken på hudmalignitet (men är inte ett exklusivt tecken för hudmelanom).
Om symtom förekommer är de ofta ospecifika, såsom:
- klåda, irritationskänsla eller annan förnimmelse, bestående eller återkommande i enskild lesion
- krusta, fjällning, rodnad, sårbildning eller blödning.
I tre fall av fyra upptäcker patienten själv eller en närstående melanomet, och i många fall sker ett första läkarbesök inom primärvården 56 57 .
När en läkare, oavsett specialitet, upptäcker melanom är de i regel tunnare och i ett tidigare tumörstadium än om patienten själv upptäcker dem 58 . Det är därför viktigt att man som läkare värderar patienters hudförändringar oavsett vilken specialitet man verkar inom. I en internationell genomgång hade 20–33 % av alla patienter med melanom vid ett tidigare tillfälle sökt läkare för samma hudförändring, vilket antyder dels att den primära diagnostiken kan förbättras 59 , dels att patienter alltid bör uppmanas att söka medicinsk bedömning igen om en lesion fortsätter att ge symtom eller förändras, eftersom ett tidigt melanom kan vara svårt att diagnostisera. Se även 1177 om malignt melanom samt bildbilagan bilaga 2 Melanom – kliniska fall med dermatoskopi.
Anamnes och klinisk undersökning
En omsorgsfull anamnes är mycket betydelsefull för att värdera misstanken om melanom, speciellt för melanom som saknar utmärkande egenskaper eller som har ett ovanligt utseende. Anamnestiska uppgifter omfattar de förändringar som har uppträtt i en pigmenterad hudlesion, symtomen från denna och händelseförloppet i tid 60 .
Avvikelser i en lesions makroskopiska utseende, jämfört med normala och patientens övriga nevi, bör leda till vidare utredning (dermatoskopi, remiss till hudläkare och teledermatoskopi till hudspecialist alternativt diagnostisk excision 61 om klinisk misstanke om melanom är hög och teledermatoskopisk konsultationsmöjlighet saknas). För dermatoskopiska ledtrådar och fördjupning, se International dermoscopy societys (IDS) hemsida.
Hela huden och alla patientens pigmentlesioner bör undersökas i god belysning. Undersökningen utförs bäst med patienten liggande på en brits och avklädd till underkläderna. Även naglar, handflator och fotsulor bör bedömas, alternativt status efterfrågas, eftersom akrala melanom ofta upptäcks sent och lätt misstolkas av patienten som en benign förändring 62 63 64 Melanom kan även sitta genitalt, ögonnära eller i ögonen, varför status bör efterfrågas eller bedömas. Innan misstanken om melanom avskrivs bör patienten erbjudas en fullständig hudundersökning, för att inte melanom på andra hudområden än de som patienten söker för ska missas. Studier har visat att 30 % av de melanom som diagnostiseras har påträffats på en annan del av huden än den lokal och förändring som patienten ursprungligen sökte för 65 .
Patienter som bedöms ha ökad risk för melanom bör uppmuntras att själva regelbundet undersöka hela sin hud med hjälp av spegel eller en närstående, och undervisas om vilka tecken som kan förekomma vid tidig melanomutveckling. En god tillgänglighet för tidig läkarbedömning och dermatoskopi av misstänkt hudförändring kan påverka i vilket stadium ett melanom hittas.
Vid hög misstanke om invasivt melanom bör SVF startas, se avsnitt 7.4 Ingång till standardiserat vårdförlopp (SVF).
Dermatoskopi och teledermatoskopi
Rekommendationer och evidens
- Dermatoskopi förbättrar den diagnostiska träffsäkerheten om användaren är tränad i metoden. (+++)
- Digitalfotografering av hudförändringar (helkropps- och dermatoskopibilder) med dermatoskop och uppföljning av förändringarna över tid (månader eller år), är bra tillägg till klinisk bedömning och undersökning hos högriskindivider och patienter med många och stora (> 5 mm) nevi. (+++)
-
Konsultation med stöd av teledermatoskopi mellan vårdgivare bör användas där det finns tillgängligt.
Med dermatoskopi förbättras diagnostiken ytterligare för tränade användare 61 .
Dermatoskopi utnyttjar luppförstoring med polariserat ljus alternativt immersionsgel och icke-polariserat ljus, och förbättrar möjligheten att se tidiga tecken till melanom 66 67 68.
Upprepad digital dermatoskopi kan användas för kort- eller långsiktig monitorering och uppföljning av en hudspecialist. Kortsiktig monitorering (intervall på 3–4 månader) används för att följa enstaka misstänkta melanocytära lesioner 69 . Långsiktig monitorering (intervall på 6–12 månader) används vid kontroll av högriskindivider 70 71 72 73 .
Tid till diagnos och till operation av patienter med melanom kan kortas med hjälp av teledermatoskopi, där misstänkta hudförändringar kan bedömas via bildkonsultation på distans 74 75 76 77 .
Vid teledermatoskopi fotograferar primärvårdsspecialisten den misstänkta hudförändringen makroskopiskt och dermatoskopiskt 75 . Därefter skickas bilderna och görs tillgängliga digitalt för en hudspecialist. Bilder och bakgrundsinformation granskas av hudspecialisten som därmed kan triagera bildremissen och ge ett utlåtande och en rekommendation om fortsatt handläggning. I de fall patienten bedöms behöva komma till hudläkare för ett fysiskt besök, innebär detta arbetssätt en säkrare prioritering och ökade möjligheter att planera inför patientens besök och därmed optimera omhändertagandet 78 . En webbutbildning i teledermatoskopi finns på RCC:s webbplats.
Klassificering av melanom
Den klassificering av de olika undergrupperna av melanom som i dag förordas av WHO utgår från särskiljande kliniska, histopatologiska, epidemiologiska och genetiska kännetecken, progress, associationer till speciella lokaler på huden och graden av kronisk solskada (chronic sun damage, CDS) . Melanom klassificeras som ”low-CSD-melanom” vilka huvudsakligen utgörs av superficiellt spridande melanom (SSM) och karakteriseras av mutationer i BRAFV600E. I gruppen ”high-CSD-melanom” inkluderas LMM som karakteriseras av mutationer i c-KIT, och desmoplastiska melanom (DM) som karakteriseras av mutationer huvudsakligen i NF1. Klassificeringen inkluderar även den större gruppen ”non-CSD-melanom” som innefattar akrala melanom (AM) med mutationer i c-KIT, mukosala melanom (MMM) med mutationer i c-KIT, och ovanliga melanomtyper såsom melanom i stora kongenitala nevi med NRAS-mutationer, Spitz melanom med varierande genetiska avvikelser och melanom i blått nevus med mutationer i GNAQ eller GNA11.
Nodulära melanom (NM) är en snabbväxande melanomtyp som förekommer på olika lokaler och saknar karakteristiska genetiska avvikelser 80 . Nevoida melanom är en melanomtyp som förekommer på olika lokaler och ofta är svårdiagnostiserad pga. likheten med nevi. Mutationer i nevoida melanom är inte väl undersökta, men inkluderar mutationer i BRAF och NRAS.
I bilaga 2 Melanom – kliniska fall med dermatoskopi finns ytterligare fördjupning om de olika melanomtyperna och diagnostik av dessa. För fördjupning avseende dermatoskopi finns International Dermoscopy Societys (IDS) hemsida med kostnadsfritt utbildningsmaterial. Se även bilaga 3 Melanom hos äldre. Kliniska fall med dermatoskopi.
Ingång till standardiserat vårdförlopp (SVF)
Välgrundad misstanke – kriterier för start av utredning enligt SVF
Välgrundad misstanke föreligger vid ett eller flera av följande kriterier:
- dermatoskopisk eller teledermatoskopisk undersökning som inger stark misstanke om invasivt hudmelanom (ICD-10: C43.0–9)
- histopatologiskt fynd av primärt invasivt hudmelanom eller melanommetastas
- undersökningsfynd som talar för nytillkommen melanommetastas (dvs ej vid recidiv av melanom som redan är under behandling).
* Bedömning av vad som är stark misstanke grundas på läkarens kliniska erfarenhet.
Invasivt melanom i huden och melanommetastas omfattas således av SVF, men inte in-situ-melanom. Melanom hos barn (se avsnitt 7.6.2 Melanom hos barn) och melanom som utgår från slemhinna i ögon, genitalier eller andra slemhinnor omfattas inte av SVF. För information om slemhinnemelanom och ögonmelanom var god se bilaga 4 Mukosala melanom respektive bilaga 5. Ögonmelanom – uvealt och konjunktivalt melanom.
Aktuell version av SVF finns i Kunskapsbanken.
Utredning av misstänkt melanom med eller utan start av SVF
Rekommendationer och evidens
- Vid all misstanke om melanom bör snar utredning ske. (+++)
- Dermatoskopi, teledermatoskopisk konsultation, remiss till hudspecialist eller diagnostisk excision (om teledermatoskopisk konsultationsmöjlighet saknas) är tidiga steg i utredningsprocessen.
- Vid stark (välgrundad) klinisk misstanke om invasivt melanom, eller om PAD-svar visar primärt invasivt melanom eller melanommetastas, bör SVF startas.
SVF startas om syftet med utredningen är att ”bekräfta melanom”, det vill säga om den kliniska misstanken är tillräckligt stark.
Stark (välgrundad) misstanke om invasivt melanom är en bedömning som görs av den läkare som startat SVF och som grundas på läkarens kliniska erfarenhet.
SVF bör inte startas om syftet med utredningen är att ”utesluta melanom”, det vill säga vid svagare misstanke om melanom.
Vid svagare misstanke om invasivt melanom bör i stället snar utredning ske med teledermatoskopisk konsultation och remiss till hudspecialist eller med diagnostisk excision och patologbedömning, men utanför ramen för SVF. I dessa fall startas SVF först när diagnosen invasivt melanom ställts efter histopatologisk undersökning och patologisk anatomisk diagnos (PAD).
Sammanfattningsvis grundas graden av klinisk misstanke på en komplex sammanvägning av anamnes om riskfaktorer, förändring och symtom samt kliniskt och dermatoskopiskt utseende.
Diagnostik och behandling av melanom hos gravida och barn
Graviditet och melanom (inklusive hormonell substitution och p-piller)
Rekommendationer och evidens
- Nevi eller nytillkomna hudförändringar som inger misstanke om melanom bör utredas utan dröjsmål, även under en graviditet. (++)
- Melanom hos en gravid kvinna behandlas efter tumörstatus, det vill säga på samma sätt som hos en icke-gravid kvinna. (++)
Inget i litteraturen talar för att nevi ändrar sin biologiska karaktär under graviditeten. Nevi som förändras, och tydligt melanommisstänkta förändringar, bör därför alltid undersökas och handläggas på samma sätt som hos icke-gravida 81 82 83 .
Melanom utgör nästan hälften (46 %) av alla diagnostiserade cancerformer under graviditet i Sverige 84 85 . Incidensen är omkring 2,8–5 per 100 000 graviditeter 86 . Den totala överlevnaden skiljer sig inte mellan gravida kvinnor med melanom och icke-gravida kvinnor med melanom i fertil ålder 85 87 88 89 90 . Ingen skillnad i överlevnad har heller konstaterats mellan kvinnor som blir gravida efter sin melanomdiagnos och de kvinnor som inte genomgått graviditet 91 .
Det finns inga skäl att avråda från en ny graviditet vid diagnos av så kallade tunna (T1) melanom, där risken för återfall är mycket liten. Man kan dock diskutera med patienten om att kanske avvakta med att bli gravid efter ett diagnostiserat högriskmelanom, för att öka möjligheterna att följa upp och behandla patienten avseende ett eventuellt återfall i melanom 87 92 93 . Kvinnor i fertil ålder som har primärbehandlats för melanom bör därför få fullständig information om sin prognos när de överväger en graviditet 85 87 88 89 91 92 93 94 .
Se stöddokument för cancer under graviditet i Kunskapsbanken och avsnitt 12.3.6 Behandling av spritt, icke-operabelt melanom hos gravida och avsnitt 12.3.7 Fertilitetsfrågor i samband med onkologisk behandling med immuncheckpointhämmare, BRAF- eller MEK-hämmare.
Melanom hos barn
Rekommendationer
- Melanocytära förändringar som exciderats hos barn, och som har malignitetsmisstanke, bör undersökas av en patolog med erfarenhet av melanomdiagnostik under uppväxtåldern.
- Melanom hos barn bör diskuteras på MDK.
Melanom är mycket ovanligt i barnaåren 95 . Sjukdomen uppträder vanligen efter puberteten (10–14 år) och incidensen ökar därefter med stigande ålder. SVF hudmelanom gäller inte för barn under 18 år, men misstänkta melanom hos barn bör ändå handläggas med hög prioritet.
En fördubbling av antalet ungdomsmelanom (<20 år) noterades i Sverige 1973–1992 96 97 men antalet tycks ha minskat under följande period, 1993–2002. En svensk studie har visat två gånger högre incidens av melanom hos barn som bor i södra delen av Sverige jämfört med dem i norra delen 98 .
Tabell 2. Antal fall av melanom hos barn i Sverige 2000–2020.
|
Ålder |
Antal |
|
0–9 år |
5 |
|
10–14 år |
16 |
|
15–19 år |
144 (varav 51 pojkar och 93 flickor) |
Primära melanom hos barn kan uppstå från baddräktsnevi (giant congenital melanocytic nevi) som finns hos cirka 1 av 20 000 nyfödda 99. Livstidsrisken för malign omvandling av dessa nevi är 2–20 %, och melanomet uppträder vanligen före puberteten 100 101 . Ärftlighet för melanom och förekomst av ökat antal pigmentnevi är riskfaktorer för utveckling av melanom även hos individer under 18 år 101 102 .
Spitz nevi (spol- och epitelioidcellsnevi) är relativt vanliga hos barn och har ett benignt förlopp trots flera histopatologiska likheter med melanom 103 . Spitz melanocytom (atypisk Spitz tumör (AST) och Spitz tumör med oklar malignitetspotential (STUMP) är förknippade med en hög grad av positiva portvaktskörtelbiopsier (sentinel node-biopsier) (41 %), men paradoxalt nog utan sjukdomsprogression 103 104 . Rekommendationerna är därför att inte genomföra portvaktskörtelbiopsi i dessa fall 104 105.
Då det fortfarande inte finns säkra histopatologiska diagnostiska kriterier som definitivt skiljer ut Spitz melanocytom (AST) och STUMP från Spitz melanom 106 107 , rekommenderas att frikostigt diskutera dessa lesioner på MDK och att dermatopatologer bedömer fallen.
För rekommenderade excisionsmarginaler, se avsnitt 11.1 Kirurgisk behandling av primärt invasivt melanom och tabell 6 Kliniska med linjal uppmätta sidomarginaler som bör användas vid diagnostisk excision (excisionsbiopsi) respektive utvidgad excision.
Behandling och överlevnad
Rekommendationer
- Principer för behandling och uppföljning av melanom hos vuxna kan användas hos barn.
- Portvaktskörtelbiopsi hos barn rekommenderas på samma sätt som för vuxna vid melanom.
- Föräldrar bör informeras om att överlevnaden hos barn är minst likvärdig och troligen bättre än hos vuxna med samma sjukdomsstadium.
Grunden för behandlingen för barn är kirurgisk och följer rekommendationerna för vuxna 108 .
Den relativa sällsyntheten av melanom i barndomen omöjliggör prospektiva studier av behandling och överlevnad hos barn. Den största retrospektiva studien på barn hittills kommer från National Cancer Database i USA, som fått sina fall från sjukhusregister 109 . Studien beskriver den demografiska och kliniska bilden av melanom hos 3 158 unga patienter i åldrarna 1–19 år, för perioden 1985–2003. Den visar att såväl regional som generell metastasering är vanligare vid diagnos hos barn i åldern 1–9 år jämfört med barn i åldern 15–19 år.
Förklaringar som ges till skillnaderna mellan yngre barn och tonåringar är:
- fördröjd diagnostik hos små barn på grund av en låg medvetenhet om möjlig melanomdiagnos
- åldersrelaterade biologiska skillnader
- en överrepresentation av patienter med mer avancerad sjukdom hos en sjukhusbaserad population.
Trots att man ofta finner en mer avancerad sjukdom vid diagnos hos barn än hos vuxna, är överlevnaden densamma eller eventuellt bättre 110 111 .
Överlevnaden hos patienter under 21 år och vuxna är jämförbar, baserat på data från en fallkontrollstudie där 5-årsöverlevnaden var 91 % för personer under 21 år jämfört med 86 % för äldre patienter 112 . Motsvarande andelar för 10-årsöverlevnaden var 89 % jämfört med 79 %. I de fall portvaktskörtelbiopsi var utförd fann man positiva körtlar hos 44 % av de yngre patienterna och hos 29 % av de vuxna. Skillnaden var dock inte statistiskt signifikant på grund av ett litet antal observationer.
Portvaktskörtelbiopsi anses vara motiverat hos barn beroende på melanomtjocklek. I sex rapporterade serier anges att en positiv portvaktskörtel påträffas i 25–60 % av fallen 112 . I ännu en studie där man jämfört barn med vuxna fann man en positiv portvaktskörtel hos 40 % av barnen och 18 % av de vuxna, samt inga återfall eller dödsfall hos barnen men 25 % återfall och 9 % dödsfall hos de vuxna 113 .
Diagnostik och handläggning av övriga melanom
Mukosala melanom
Rekommendationer
- Mukosala melanom, det vill säga melanom som utgår från slemhinnor i näs- och bihålor, munhåla och svalg, esofagus, vulva, glans penis och distala delen av analkanalen, är ovanliga och större studier saknas.
- Mukosala melanom bör frikostigt diskuteras på MDK.
Se bilaga 4 Mukosala melanom och kapitel 12 Systemisk behandling.
Melanom med okänd primärtumör
Rekommendationer
- Utredning av patienter med metastasering av melanom utan uppenbar primärtumör bör diskuteras vid MDK innan behandling, skyndsamt remitteras till onkolog och eventuell utredning av primärtumör bör ske parallellt.
- Fjärrmetastasutredning ska utföras skyndsamt med bilddiagnostik, i första hand positronemissionstomografi (PET) inklusive magnetisk resonanstomografi (MR) eller datortomografi (DT) hjärna.
- Utredning av primärtumör bör ske riktat, främst genom utförlig hudundersökning med stöd av dermatoskopi.
- Mutationsanalys, metastaskarakteristika och metastaslokalisation kan ge vägledning om ytterligare utredning anses behövas.
- Om man därefter inte påvisar primärtumören antas att tumören haft ursprung i huden och genomgått en komplett regress.
Melanom är en av de tumörformer där den primära tumören inte alltid kan påvisas 114 115 . Tumören kan ha en ovanlig lokalisation, till exempel i ögat eller mukosalt (sinonasalt, rektalt eller urogenitalt), men i de flesta fallen har den primära tumören sannolikt spontant försvunnit genom att kroppens immunsystem aktiverats mot densamma 116 . Sannolikt förekommer total regress hos 10–20 % av melanomen, även om man bara diagnostiserat metastasering utan känd primärtumör i cirka 5 % av alla fall 115 117 . Partiell regress av melanom beskrivs i 30–50 % av alla PAD-svar. Studier har visat att patienter med metastaser och okänt primärt melanom har en bättre prognos än de som har metastaser och en känd primärtumör 118 119 120 . Detta tyder på att en patient med okänd primärtumör har ett starkt immunsvar mot tumören.
Patienter med metastaserande melanom utan känd primärtumör bör handläggas inom SVF, diskuteras vid MDK och behandlas enligt principerna för melanom i motsvarande stadium. Diagnosen bör fastställas histologiskt om möjligt. Patienten bör utredas individuellt med riktade undersökningar. Efterfråga till exempel nästäppa och näsblödningar (sinonasala mukosala melanomsymtom), symtom från munhålan, ändrade avföringsvanor, knölar, smärta eller blödning anogenitalt (anogenitala melanomsymtom). Palpera ytliga lymfkörtelstationer för möjlig vägledning. Titta i konjunktiva (bindehinna) och evertera ögonlocken.
Om ingen genetisk information finns tillgänglig för metastaserna, så bör dilaterad ögonundersökning av ögonbotten göras. Om genetisk information finns tillgänglig, och den uppvisar en profil som är typisk för icke - uveala melanom t.ex. mutationer i BRAF, c-kit, NRAS, eller NF1, men inga mutationer i GNA11 eller GNAQ) behöver inte ögonundersökning göras.
Syftet med utredningen är att snabbt kunna fatta ett behandlingsbeslut, så att patienten kan påbörja sin behandling. För att inte denna ska fördröjas rekommenderas i första hand diskussion vid MDK och en komplett hudundersökning med dermatoskopistöd (inklusive undersökning av genito-anal hud, och okulär inspektion av ögon, näsborrar och munhåla) 121 . Parallellt bör en riktad fjärrmetastasutredning (exempelvis med bild- eller funktionsdiagnostik) ske. Patientens funktionsstatus (performance status), metastaslokal, metastaskarakteristika och mutationsanalys av metastasen kan styra utredningen. Mutationsmönster och metastaslokal eller metastasutbredning kan liksom BRAF-analys ge vägledning om ursprung för det primära melanomet (se KVAST-bilaga om tumörklassificering enligt WHO). Detta grundar sig på att majoriteten av patienterna kan antas ha icke-identifierade, regredierade (tillbakabildade) melanom, och att molekylära karakteristika vid melanom med okänd primärtumör motsvarar dem som ses vid melanom i huden. Det kan vara värt att framhålla för patienter och närstående att behandlingen inriktar sig mot den metastatiska sjukdomen och att en icke-identifierad primärtumör inte utgör någon ytterligare risk, samt att prognosen generellt är gynnsammare vid en okänd primärtumör 118 119 120 . Se kapitel 12 Systemisk behandling.
Ögonmelanom – uveala och konjunktivala
Det finns olika typer av ögonmelanom: uveala och konjunktivala.
Uvealt melanom är den vanligaste typen med en incidens på 4–6 fall per år och miljon invånare i de flesta västländer 122 . I Sverige är incidensen cirka 120–130 nya fall per år 123 . Totalt 90 % av uveala melanom utgår från korioidea (åderhinnan), 7 % från corpus ciliare (strålkroppen) och 3 % från iris (regnbågshinnan) 124 .
Incidensen av konjunktivalt melanom (bindehinnemelanom) är bara 0,1–0,3 fall per miljon invånare i de flesta västländer, och i Sverige innebär det cirka 2–3 nya fall per år 125 126 .
Behandlingen av de flesta patienter är centraliserad till S:t Eriks Ögonsjukhus i Stockholm.
Figur 3. Schematisk illustration av ögats anatomi.
Druvhinnans olika delar där uveala melanom kan uppstå samt bindehinnan där konjunktivala melanom kan uppstå.
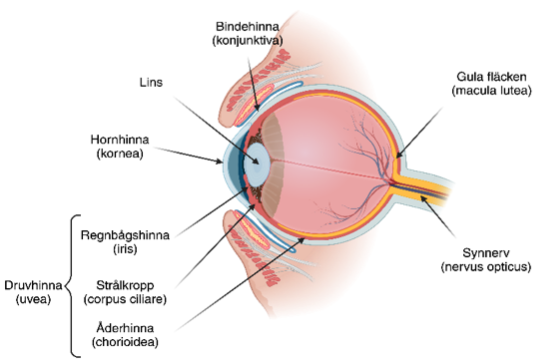
Källa: Illustrationen är skapad av vårdprogramgruppen med biorender.com
För fördjupad information, se bilaga 5. Ögonmelanom – uvealt och konjunktivalt melanom.
