Primär behandling
Översikt
Den primära behandlingen av livmoderhalscancer styrs av en kombination av stadium, histologi och samsjuklighet. Cirka 60 % av de kvinnor som erhåller primär behandling genomgår kirurgi vilket till stor del speglar stadiefördelningen (ca 50 % diagnostiseras i stadium I). Ett fåtal randomiserade studier ligger till grund för rådande nationella och internationella behandlingsrekommendationer. Valet mellan kirurgi och strålbehandling vid stadium I baseras på en italiensk studie som inte visade någon överlevnadsskillnad mellan metoderna 158. Studien slog också fast att de kvinnor som fick adjuvant strålbehandling efter kirurgi hade högst förekomst av allvarliga biverkningar, och dubbelbehandling bör därför undvikas. Studien har kritiserats på grund av hög andel adjuvant behandling (64 %) samt den höga återfallsfrekvensen (25 %). Rekommendationerna kring adjuvant behandling efter primärkirurgi baseras till stor del på GOG92 där man påvisade bättre överlevnad efter strålbehandling vid en kombination av djup stromainfiltration, LSVI och tumörstorlek (”Sedliskriterierna”) 154. Även denna studie har kritiserats på grund av hög återfallsfrekvens (28 %). För primärt behandlingsval vid lokalt avancerad livmoderhalscancer finns inga randomiserade studier men då risken för lymfkörtelmetastaser ökar påtagligt rekommenderas definitiv strålbehandling för att undvika dubbelbehandling.
Kirurgi
Rekommendationer för primär kirurgisk behandling av livmoderhalscancer*
Stadium IA1 utan lymfkärlinväxt (LVSI)
- Enkel hysterektomi** +/- salpingooforektomi*** eller rekonisation v.b.
- Ingen lymfkörteldiagnostik
Stadium IA1 med LVSI, IA2 (med eller utan LVSI)
- Enkel hysterektomi** +/- salpingooforektomi*** eller rekonisation om fertilitetsönskan****
- Pelvin lymfkörtelutrymning eller portvaktskörtelbiopsi enbart
Stadium IB1 med invasionsdjup ≤ 10 mm eller < 50 % stromainvasion på MRT
- Enkel hysterektomi**+/- salpingooforektomi*** eller enkel trakelektomi om fertilitetsönskan****
- Pelvin lymfkörtelutrymning +/- portvaktskörtelbiopsi
Stadium IB1 med invasionsdjup > 10mm eller ≥ 50 % stromainvasion på MRT
- Radikal hysterektomi +/- salpingooforektomi***
- Pelvin lymfkörtelutrymning +/- portvaktskörtelbiopsi
-
Radikal trakelektomi om fertilitetsönskan IB1****
Stadium IB2 samt IIA1
- Radikal hysterektomi +/- salpingooforektomi***
- Pelvin lymfkörtelutrymning +/- portvaktskörtelbiopsi
* För neuroendokrina tumörer (NEC), annan högriskpatologi se avsnitt 10.7 Neuroendokrin livmoderhalscancer (NEC).
** Enkel hysterektomi innefattar adekvat marginal mot vagina för att få med ev kvarvarande dysplasi vid stadium IA eller vid IB1 5 mms marginal se avsnitt avsnitt 10.2.2 Kirurgiska principer.
*** Salpingektomi rekommenderas vid hysterektomi om ovarierna kvarlämnas.
**** Stadium IB1 med fertilitetsönskan ska remitteras och diskuteras på nMDK trakelektomi.
Kirurgiska metoder
Rekommendationer
-
Kirurgisk behandling, förutom slyngkonisering eller enkel hysterektomi vid IA1 utan LVSI, ska utföras på tumörkirurgisk enhet på universitetssjukhus.
-
Enkel hysterektomi i stadium IA kan utföras med valfri kirurgisk teknik under förutsättningar att adekvat marginal mot vagina kan uppnås.
-
Enkel och radikal hysterektomi vid stadium IB1, IB2 eller IIA1 bör utföras med öppen kirurgisk teknik (laparotomi).
-
Trakelektomi utförs antingen vaginalt eller robotassisterat på NHV-enhet.
Vid primär, kurativ kirurgisk behandling av livmoderhalscancer med radikal hysterektomi finns ett flertal metoder som innefattar konventionell laparotomi, konventionell laparoskopi, vaginal radikal hysterektomi (Schauta), robotassisterad kirurgi samt hybrider av dessa metoder. I Sverige används uteslutande laparotomi samt robotassisterad kirurgi och det finns inte anledning att värdera andra metoders lämplighet.
I en Cochraneanalys från 2013 analyserades evidensläget beträffande laparoskopisk radikal hysterektomi jämfört med öppen radikal hysterektomi 159. Man fann en randomiserad studie som dock endast innefattade 15 patienter 160. Man konkluderade att evidensläget var alltför svagt för att man skulle kunna dra några slutsatser avseende operationsmetod. Ett fåtal icke-randomiserade studier har tidigare jämfört det onkologiska utfallet mellan robotassisterad och öppen kirurgi och den sammantagna bilden talade för att återfallsfrekvens och överlevnad var jämförbara mellan metoderna 777879161. 2018 publicerades emellertid resultat från den internationella, randomiserade LACC-studien (”Laparoscopic Approach to Cervical Cancer”) som startade 2008 162. I studien randomiserades kvinnor med operabel livmoderhalscancer till laparotomi eller minimalinvasiv kirurgi. Studien stängde i förtid hösten 2017, och 631 av 740 planerade studiepatienter hade då blivit inkluderade. Resultaten visade överraskande en överrisk för återfall (HR 3,74, 95 % CI 1,63–8,58) och död (HR 6,00, 95 % CI 1,77–20,30) i den minimalinvasiva armen. Överlevnadsresultaten från LACC-studien bekräftades av en populationsbaserad registerstudie från USA som visade en ökad risk för död bland kvinnor som opererats med minimalinvasiv teknik för livmoderhalscancer 163. Mot dessa resultat står data från det svenska kvalitetsregistret för gynekologisk cancer (SQRGC) där ingen skillnad i vare sig återfall eller död observerats för 862 kvinnor opererade med laparotomi eller robotteknik 2011–2017 164. I maj 2019 publicerade ESGO (European Society for Gynecological Oncology) ett expertuttalande där laparotomi framhålls som standardmetod vid kirurgisk behandling av livmoderhalscancer. Mot bakgrund av resultaten från LACC-studien rekommenderas inte längre minimalinvasiv kirurgi vid kirurgisk behandling av tidig livmoderhalscancer. Flera internationella multicenterstudier där kvinnor med stadium IB1–IB2 livmoderhalscancer randomiseras till laparotomi eller robotassisterad laparoskopi pågår 160161.
Avseende kirurgisk metod vid enkel hysterektomi togs i den nyligen publicerade SHAPE studien med randomisering mellan radikal och enkel hysterektomi inte hänsyn till minimalinvasiv eller öppen kirurgi. Den initierades innan LACC studiens resultat var klara och majoriteten (>80%) var opererade med minimalinvasiv teknik 162. Dock bör enkel hysterektomi vid IB1, i väntan på RACC studiens resultat, endast utföras minimalinvasivt inom ramen för kliniska studier.
Vid fertilitetsbevarande ingrepp utöver konisering (trakelektomi) grundas nuvarande kunskapsläge till absolut största del på studier av vaginal radikal trakelektomi (VRT). Emellertid kan även öppen kirurgi (ART) användas liksom laparoskopisk och robotassisterad. I Sverige används vaginal och robotassisterad kirurgi. Beträffande metod för radikal trakelektomi är evidensläget svagare. Det finns ett fåtal studier som jämför öppen och vaginal trakelektomi. I en relativt stor studie från Kina som innefattade 150 patienter (73 ART och 77 VRT) tyckte man sig se ett bättre onkologiskt utfall i ART-gruppen medan det obstetriska utfallet föreföll bättre i VRT-gruppen 166. I den retrospektiva multicenterstudien IRTA jämfördes det onkologiska utfallet mellan kvinnor som genomgått radikal trackelektomi med öppen och minimalinvasiv teknik (n=646) 167. Resultaten visade ingen skillnad i vare sig återfallsfri eller totalöverlevnad och då möjligheten att genomföra en randomiserad studie bedöms vara mycket liten, får man betrakta metoderna som likvärdiga ur ett onkologiskt perspektiv.
Kirurgiska principer
Rekommendationer
- Kirurgins omfattning beror på stadium, tumörstorlek och lokalisation.
- Risken för spridning till ovarier är liten men ökar vid adenokarcinom.
Förutsättningar för behandling med enkel hysterektomi
Målet med primär kirurgisk behandling är att uppnå radikalitet avseende cervixtumören samt identifiera eventuella lymfkörtelmetastaser. Vid stadium IA är risken för metastaser i parametrierna obetydlig och radikal hysterektomi att betrakta som överbehandling. Detta bekräftades i en nyligen publicerad studie baserad på den amerikanska, nationella cancerdatabasen (n = 1530) där ingen överlevnadsskillnad sågs mellan enkel hysterektomi och radikal hysterektomi vid stadium IA2 169. Däremot observerades en signifikant sämre överlevnad efter enkel jämfört med radikal hysterektomi för stadium IB1 < 2 cm (92,4 % vs. 95,3 %). Studien har kritiserats för att det saknades lymfkörteldiagnostik i 19% av fallen samt data för histopatologi var inkompletta. I ConCervstudien ingick100 patienter med tumörstorlek < 2 cm som behandlats med enkel hysterektomi eller konisering och recidivfrekvensen var 3,5 %. Dock inkluderades inte lågt differentierade adenocarcinom, tumörer med LVSI samt preoperativt icke radikala konbiopsier i studien 163.
Den nyligen publicerade SHAPE studien visade ingen skillnad i lokala bäckenrecidiv i en 3-årsuppföljning efter randomisering av 700 patienter till antingen radikal eller enkel hysterektomi (recidivfrekvens (2,17 % mot 2,56 %) vid stadium IA2 eller IB1 med eller utan LVSI 162. Däremot sågs en lägre andel med urininkontinens och urinretention efter enkel hysterektomi. Det talar för att enkel hysterektomi är att föredra mot radikal hysterektomi vid tidig cervixcancer under förutsättning att vissa prognostiska faktorer nogsamt har beaktats:
- Endast vid skivepitelcancer, adenocarcinom, adenoskvamös cancer
- Tumörstorlek ≤ 2 cm
- Invasionsdjup < 10 mm i konpreparat eller < 50 % stromainvasion på preoperativ MRT (om ej koniserad).
Det bör uppmärksammas att SHAPE studien inkluderade få fall av lågt differentierade adenocarcinom och färre än 14% av tumörer med LVSI varför försiktighet bör beaktas vid en kombination av dessa faktorer och särskilt i stadium IB1 162.
För diagnosen mikroskopisk cancer krävs PAD-svar på konpreparat. För att kunna fastslå att det är stadium IA1 eller IA2 krävs att tumören är radikalt avlägsnad avseende infiltrationsdjup och materialet granskat av en referenspatolog. Det är ingen nackdel om slyngkonisering har genomförts även vid stadium 1B1.
MR enligt cervixcancerprotokoll ska genomföras för bedömning av storlek och stromainvasion eller för bedömning om det finns tumör kvar efter slyngkonisering. I MR-remissen bör stromainvasion < 50 % efterfrågas. Vid tveksamhet rörande stromainvasion < 50 % ska radikal hysterektomi tillämpas.
Avseende marginal mot vagina bör det vid trolig kvarvarande tumöri cervix tillämpas en kirurgisk marginal på minst 5 mm. En hysterektomi vid stadium IA bör omfatta en vaginalmanschett för att eventuell kvarvarande dysplasi medtages och därav är det fördelaktigt att kolposkopera innan operationsstart för bedömning av hur mycket av vagina som behöver tas med.
Radikal hysterektomi
Kirurgin bör anpassas efter tumörstorlek och tumörlokalisation samt relateras till den moderna klassifikationen av kirurgin enligt Querleu-Morrow (QM) 168. Enligt denna klassifikation utgörs nervsparande ingrepp av typ A-C1 och de mer omfattande ingreppen C2-D har ingen plats vid behandling av stadium IB1–2 och IIA1. En svaghet med QM-klassifikationen är att uppdelning i övre och nedre parametrier saknas, vg se avsnittet om lymfkörteldiagnostik. De nedre parametrierna/paracolpierna riskerar att vara tumörinvolverade vid tumörväxt per continuitatem vilket torde vara aktuellt endast vid större tumörer (> IB1). Samtidigt är avlägsnandet av de nedre parametrierna behäftat med en risk för skada på autonoma nerver. De övre lymfovaskulära parametrierna vilka följer uterinakärlen till dess avgång och vidare ut mot körtelstationerna på bäckenväggen innehåller däremot uterusnära lymfkörtlar som riskerar att vara tumörinvolverade även vid mindre tumörer. Avlägsnandet av dessa övre, lymfovaskulära parametrier är till skillnad mot de nedre inte behäftat med risk för skada på autonoma nerver och de bör därför avlägsnas även vid mindre tumörer. Få studier har separat undersökt de övre lymfovaskulära parametrierna men en studie på trachelektomerade patienter visade isolerade körtelmetastaser i ett fall av 46 patienter 170. Motsvarande har man i en studie på endometriecancer på fler än 400 patienter funnit lymfkörtlar i de övre parametrierna hos 40 % av patienterna varav isolerade metastaser hos 3 % av körtelpositiva patienter 171. Avlägsnande av de övre lymfovaskulära parametrierna kan därför betraktas som en del av körtelstagingen snarare än en del av den radikala hysterektomin. Se även avsnitt 10.2.3 Kirurgisk lymfkörteldiagnostik.
Operationen inleds med inspektion av buk- och bäckenorgan. Metastaser i bukhålan är mycket ovanligt och bör verifieras med fryssnitt. Vid konstaterad disseminerad sjukdom bör operationen avbrytas till förmån för onkologisk behandling vars intention avgörs av omfattningen av spridningen. Operationen inleds med lymfadenektomi (se nedan) då eventuella fynd av körtelmetastaser påverkar resten av ingreppet. I samband med lymfadenektomi öppnas de presakrala, paravesikala och pararektala spatierna sparande de övre lymfvaskulära körtlarna, och körtlarna avlägsnas stationsvis med försiktighet så att de inte skadas och vid metastaser riskerar att kontaminera bukhålan. Om portvaktskörtelbiopsi används skickas dessa körtlar separat för ultrastaging. Den laterala och distala omfattningen av kirurgin avgörs således enligt ovan och varje operatör bör innan ingreppet ha klargjort vilken typ av QM radikal hysterektomi som planeras.
Beroende på typ av radikal hysterektomi som utförts kan avlastning av blåsan vara nödvändig under upp till 7 dagar. Oavsett tid för postoperativ avlastning bör miktionsförmågan och residualurin kontrolleras. Avlastning kan ske med KAD, RIK eller suprapubisk kateter enligt lokala rutiner.
En relativt ny kirurgisk metod, total mesometrial resektion (TMMR), beskrevs 2010 av Michael Höckel 172. Grunden till TMMR utgörs av omfattande embryologiska studier där relationen mellan cervix och omkringliggande strukturer delas in i compartments. Hysterektomin, som i vissa avseenden är mindre radikal än traditionell RH, kombineras med synnerligen noggrann ”terapeutisk” lymfadenektomi. Oavsett lymfkörtelstatus ges ingen adjuvant strålbehandling. Trots att kvinnor med lokalt avancerade tumörer ingick i denna kohort är resultaten mycket goda med en 5-årsöverlevnad på 89 %. Det saknas emellertid jämförande studier mot nuvarande standardbehandling.
Tabell 1. Klassifikation av radikal hysterektomi enligt Querleu and Morrow (Q/M)
|
|
Typ av hysterektomi |
Uretär-mobilisering |
Lateral dissektion |
Vagina |
Sakrouterin-ligament |
Vesicouterin-ligament |
|
A |
Extrafasciell |
Ingen |
Nära cervix |
Minimal resektion |
Cervixnära dissektion |
Cervixnära dissektion |
|
B |
Modifierad radikal |
Partiell |
Medialt om uretärtunneln |
Ca 10 mm |
Partiell resektion |
Partiell resektion |
|
C |
Klassisk radikal |
Komplett |
Lateralt om uretärtunneln |
15–20 mm |
Rektumnära dissektion efter friläggning av plexus hypogastricus |
Blåsnära resektion och sparande av nervstrukturer |
|
D |
Lateralt utvidgad resektion |
Komplett |
Direkt vid avgång av a. iliaca interna, friläggning av roten till n. ischiadicus |
|
|
|
Nervsparande kirurgi
Radikal hysterektomi är associerat med postoperativa besvär relaterade till nervpåverkan i lilla bäckenet. Dessa komplikationer utgörs främst av urinretention, obstipation samt sexuell dysfunktion. De nerver som främst löper risk att skadas är sympatiska nervfibrer från plexus hypogastricus och parasympatiska nerver från det splankniska systemet (S2–S4). Plexus hypogastricus delas i promontoriehöjd till n. hypogastricus som följer uretären förbi sakrouterinligamenten. Vid kardinalligamenten sammanflätas hypogastricusfibrerna med n. splanknicus nedom den djupa vena uterina. Skador på hypogastricus i samband med delning av sakrouterinligamenten förklarar sannolikt merparten av problemen, även om studier talar för att framförallt postoperativ urinretention orsakas av skador på splanknicusnerverna. Korrekt utförd nervsparande kirurgi förefaller dock minska risken för denna typ av postoperativ komplikation 173. Redan på 1960-talet beskrev Kobayashi vid universitetet i Tokyo en nervsparande teknik som sedan förfinats och även anpassats till minimalinvasiva tekniker. Tillgänglig evidens tyder på att nervsparande kirurgi förbättrar objektiva utfall såsom residualurinvolym, urodynamiska parametrar och vaginalt blodflöde. Patientrapporterade data ger en mer splittrad bild där några mindre studier talar för mindre upplevda besvär efter nervsparande kirurgi. Den största studien hittills, som publicerades från Holland, kunde dock inte påvisa några patientupplevda skillnader mellan konventionell och nervsparande kirurgi 174. Studien har flera svagheter, såsom hög andel adjuvant strålbehandling, och författarna menade att resultaten inte talar emot nervsparande kirurgi då tekniken är så pass enkel. Ett flertal studier kring patientupplevda besvär pågår.
Salpingo-ooforektomi (SOE)
Risken för metastaser till ovarierna ökar med storleken på tumören, och metastaser är vanligare vid adenokarcinom än skivepitelcancer. Risken för metastaser till ovariet vid stadium IB1 var i en japansk studie 1,1 % för adenokarcinom och 0,4 % för skivepitelcancer (n = 578). Risken för ovarialmetastaser ökade påtagligt vid stadium IB2 175. Liknande resultat redovisades i en större retrospektiv studie där 3 500 kvinnor med livmoderhalscancer i stadium IB–IIA opererades med radikal hysterektomi och bilateral SOE 176. En metaanalys av 10 artiklar där 1 204 kvinnor med adenokarcinom opererades visade att frekvensen av ovarialmetastaser vid IB var 2 %. Observera att det i denna grupp även ingår 1B2 men dessa är inte redovisade för sig. Förekomst av metastaser var associerat med riskfaktorer såsom ålder > 45 år, FIGO-stadium > IB, lymfkörtelmetastaser, djup stromainvasion, tumörstorlek > 4 cm. I sex av artiklarna analyserades över 100 fall av adenokarcinom (cancer in situ-IIA) där ovarierna bevarats. Ingen fick ovarialmetastaser under uppföljningen (median 56 månader) 177.
Rekommendationen är att inte avlägsna ovarier hos premenopausala kvinnor med livmoderhalscancer. Detta är okontroversiellt vid skivepitelcancer men bör övervägas även vid adenokarcinom. Det finns inte tillräckligt med kunskap för att kunna ange att någon särskild undergrupp av adenokarcinom skulle vara oförenligt med att bevara äggstockarna. Däremot bör adenoskvamös cancer, lågt differentierad tumör eller LVSI vid adenokarcinom vägas in vid tumörer större än 2 cm. Man bör även väga in kvinnans ålder då fördelarna med att behålla ovarierna minskar vid ökande ålder och SOE rekommenderas hos postmenopausala kvinnor oavsett histologi.
Vid prematur menopaus (< 45 år) utan MHT (menopausal hormone therapy) ökar risken för långsiktiga allvarliga effekter (osteoporos, Alzheimers sjukdom, hjärt-kärlsjukdom, stroke, sexuell dysfunktion) och förtida död 178. I en studie konstateras att SOE vid livmoderhalscancer i stadium IB (adenokarcinom) innan 45 års ålder utan MHT innebär högre risk för kardiovaskulär död än risken för död i livmoderhalscancer 179. En registerstudie på över 5 000 kvinnor med livmoderhalscancer IA där hälften fick behålla sina äggstockar, visade att långtidsöverlevnaden var signifikant bättre för dem som hade äggstockarna kvar. Risken för att dö i cancer var densamma i bägge grupperna . MHT rekommenderas vid ooforektomi < 45 år, se vidare avsnitt 13.14 MHT (menopausal hormonterapi).
Ooforopexi
Kurativ definitiv eller adjuvant kombinerad cytostatika- och strålbehandling resulterar i ovariell insufficiens om ovarierna ingår i strålfältet. Ovarialfunktion efter behandling är emellertid individuell och beror på patientens ålder, given stråldos, strålfält, teknik och eventuell cytostatikabehandling 181. Inför primär strålbehandling kan profylaktisk laparoskopisk ooforopexi utföras i syfte att bevara ovarialfunktionen. Kvarlämnade ovarier vid radikal hysterektomi kan fästas lateralt ovan bäckeningången för att öka möjligheterna till bevarad funktion vid eventuell adjuvant strålbehandling 182. Vid strålbehandling med VMAT-teknik (se bilaga 5 Extern radioterapi) finns större risk att ovarierna ändå får en viss stråldos jämfört med IMRT-teknik, varför det är av stor vikt att så långt som möjligt fästa ovarierna högt upp (ovan aortabifurkationen).
Transponerade ovarier bör clipsmarkeras för att kunna identifieras som riskorgan vid targetritning och dosplanering.
Efter transposition av ovarier förekommer problematik i form av ovariell insufficiens, cystbildning och smärtor 182183, speciellt om adjuvant strålbehandling givits. Huruvida ooforopexi ska utföras rutinmässigt är inte studerat och frågan om ooforopexi bör individualiseras.
Kirurgisk lymfkörteldiagnostik
Rekommendationer
- Stadium IA1 (LVSI-negativa): Ingen lymfkörteldiagnostik.
- Stadium IA1 (LVSI-positiva) + IA2: Fullständig lymfkörtelutrymning alternativt enbart portvaktskörtelbiopsi förutsatt att tekniken är etablerad.
- Stadium IB: Portvaktskörtelbiopsi rekommenderas i kombination med fullständig lymfkörtelutrymning för förbättrad diagnostik.
Lymfadenektomi
Förekomst av lymfkörtelmetastaser ändrar i nya indelningen stadieindelningen, och är den enskilt starkaste postoperativa prognostiska faktorn. Omfattningen har beskrivits i klassifikationen av radikal hysterektomi 184 och ska innefatta utrymning av lymfkörtelvävnad i fossa obturatorius samt vävnaden kring iliacakärlen (kaudalt t.o.m. v. circumflexa) upp ett par centimeter på iliaca communiskärlen (nivå 1–2). Även de presakrala lymfkörtlarna bör ingå i en adekvat pelvin lymfkörtelutrymning. Rekommenderat minimiantal exstirperade lymfkörtlar har dock inte definierats 185.
För att bättre styra eventuell adjuvant strålbehandling bör exstirperad vävnad separeras för respektive lymfkörtelstation (som minst nedom och ovan iliaca communis).
Vid konstaterade lymfkörtelmetastaser peroperativt bör körtelutrymning utföras en nivå kranialt om metastasnivån för att bättre styra postoperativ strålbehandling.
Tabell 2 Klassifikation av lymfkörtelutrymning enligt Querleu/Morrow
|
Nivå 1 |
Arteria iliaca externa, interna, n. obturatorius |
|
Nivå 2 |
Arteria iliaca communis |
|
Nivå 3 |
Aorta nedanför arteria mesenterica inferior |
|
Nivå 4 |
Aorta ovanför arteria mesenterica inferior till v. renalis |
Portvaktskörtelbiopsi
Portvaktskörtelbiopsi (sentinel node-teknik, SLN-teknik) används för att peroperativt identifiera de körtlar som har störst risk för spridning. Portvaktskörtelbiopsi syftar till att undvika fullständig lymfkörtelutrymning vilket i sin tur kan leda till minskning av lymfatiska biverkningar, och även förkorta det kirurgiska ingreppet. Tekniken kan även användas för att identifiera lymfkörtlar utanför de anatomiskt definierade utrymningsområdena.
Studier har visat att den tracer som har bäst teknisk lyckandegrad är Indocyanin grönt, ICG med upp till 98 % bilateral detektionsgrad 171186. I avsaknad av utrustning för detektion av ICG med fluorescens kan andra färgämnen användas. Radioaktiva tracers (Tc99) inte ger möjlighet att på ett strukturerat sätt definiera portvaktskörteln då afferenta lymfbanor inte visualiseras liksom att tekniken omöjliggör detektion av portvaktskörteln i parametrier på grund av strålning från injektionsstället i cervix. Vidare bör en kombination av färgämnen eller en kombination av olika färgämnen eller radiotracer undvikas då det innebär svårigheter att definiera portvaktskörteln. Däremot kan en reinjektion av ICG ske vid otillräckligt upptag efter en injektion 187.
Portvaktskörteldetektion via ICG sker med near infrared light (NIR) som får färgen att fluorescera. En fördel med metoden är att även parametrie-nära lymfkörtlar kan detekteras, eftersom metoden färgar både lymfbanor och lymfkörtlar. Tekniken prövas nu även vid öppen kirurgi med speciellt anpassade produkter eller med hjälp av laparoskopiska kameror för att detektera portvaktskörteln.
I en metaanalys från 2013 188 med 1 112 patienter om portvaktskörtelbiopsi vid livmoderhalscancer var sensitivitet och negativt prediktivt värde 89 % respektive 95 %. Den största retrospektiva multicenterstudien inkluderade 645 patienter (stadium IA1–IIB) med en sensitivitet på 91 % vid ensidig portvaktskörtel och 97 % vid bilateral portvaktskörteldetektion 189 och resultaten har bekräftats i ytterligare studier 190191. I multicenterstudien SENTICOL I inkluderades 139 kvinnor (stadium IA1–IB1) prospektivt och de genomgick portvaktskörtelbiopsi (blåfärg och teknetium) samt ultrastaging med en sensitivitet på 92 % och NPV 98 % och bilateral detektionsgrad på 77 % 192. I SENTICOL II randomiserades sammanlagt 206 kvinnor (stadium IA2-IIA1) till enbart portvaktskörtelbiopsi eller i kombination med full lymfkörtelutymning. Studiearmarna uppvisade lika hög andel lymfkörtelmetastaser men signifikant lägre andel postopertiva biverkningar bland de kvinnor som enbart genomgick portvaktskörtelbiopsi 193.
En nyligen publicerad retrospektiv studie där man jämför patienter som genomgått enbart portvaktskörtelbiopsi (n = 110) med pelvin utrymning (n = 1 078) visade inte på någon skillnad av återfall 194. I den prospektiva observationsstudien SENTIX där enbart portvaktskörtelbiopsi utfördes vid tumörer upp till stadium IB2 redovisades en bilateral kartläggning av portvaktslymfkörtlar på 91% baserat på 395 kvinnor 195. Långtidsdata på onkologiskt utfall rapporterades på ESGO 2024 med återfallsfri överlevnad vid 2 år på 93%, publikation väntas under 2024. I dagsläget finns inga randomiserade multicenterstudier där portvaktskörtelbiopsi enbart ställs mot systematisk körtelutrymning. I SENTICOL III (NCT03386734) planeras 950 patienter att randomiseras mellan enbart portvaktskörtelbiopsi och lymfkörtelutrymning, med primärt utfall PFS och data förväntas tidigast 2027.
Algoritmen för portvaktskörtelbiopsi innefattar att den exstirperade körteln undersöks av patolog med s.k. ultrastaging, vilket innebär avsevärt tätare snitt än traditionell undersökning av körtlar. Detta ger en ökad detektionsgrad av mikrometastaser (< 2 mm) och även isolerade tumörceller (< 0,2 mm) 189196. I de fall ingen portvaktskörtel kan identifieras ska fullständig lymfkörtelutrymning utföras och makroskopiskt misstänkta körtlar ska alltid avlägsnas oavsett lokalisation.
Portvaktskörteln kan analyseras peroperativt med fryssnitt vilket ger möjlighet att intraoperativt ta ställning till avbrytande av kirurgin. Den diagnostiska säkerheten vid fryssnitt av portvaktskörteln är relativt låg (ca 60–70 %) 197, medan den postoperativa portvaktskörtelundersökningen inklusive ultrastaging finner cirka 15 % fler metastaser (inkluderat mikrometastaser och ITC) jämfört med fullständig körtelutrymning 198. I SENTIX noterades att färre än hälften av lymfkörtelmetastaserna upptäcktets peroperativt med hjälp av fryssnitt 195.
Som en del av portvaktskörtelbiopsin bör även de övre lymfovaskulära parametrierna avlägsnas (fram till cervix) för att minimera risken för underdiagnostik av isolerade körtelmetastaser i denna del av lymfsystemet. Se även avsnitt 10.2.2.1 Generella kirurgiska principer.
En övergång till enbart portvaktskörtelbiopsi (”skarp portvaktskörtelbiopsi”) vid stadium IA förutsätter att tekniken är etablerad vid respektive universitetssjukhus. En tydlig struktur för införandet bör finnas och erfarenhet av tekniken från endometriecancer är nödvändig. I en nyligen publicerad studie anges att inlärningskurvan för portvaktskörtelbiopsi vid endometriecancer planar ut efter 40 operationer, vilket kan tjäna som ett riktmärke innan skarp portvaktskörtelbiopsi införs vid livmoderhalscancer stadium IA 199.
I enlighet med aktuella riktlinjer från ESGO, ger aktuell litteratur nu stöd för att införa portvaktskörtelbiopsi enligt följande:
- Körteldiagnostik rekommenderas inte vid stadium IA (LVSI-negativa).
- Portvaktskörtelbiopsi enbart kan rekommenderas förutsatt att tekniken är etablerad vid stadium IA (LVSI-positiva).
- Vid stadium IB rekommenderas fortsatt fullständig körtelutrymning, med tillägg av portvaktskörtelbiopsi för förbättrad diagnostik.
Peroperativa fynd av lymfkörtelmetastaser vid primär kirurgi
Rekommendationer
- Vid peroperativt PAD-verifierad spridning till misstänkt lymfkörtel bör man avstå från primär kirurgi (hysterektomi och lymfkörtelutrymning).
Vid ökande stadium och tumörstorlek ökar risken för lymfkörtelmetastasering, varvid indikationerna för adjuvant kombinerad cytostatika- och strålbehandling ökar; se vidare avsnitt 10.5 och nedan. Kvinnor som genomgår både primärkirurgi och postoperativ strålbehandling har minst dubbelt så hög frekvens av behandlingsrelaterade biverkningar av grad 3–4 än kvinnor som enbart behandlas med ena modaliteten 158174200201202203. Därmed är det viktigt att undvika kombinationsbehandling, men frågan om huruvida man ska avbryta det kirurgiska ingreppet vid en konstaterad lymfkörtelmetastasering är kontroversiell.
Förekomsten av positiva lymfkörtlar efter radikal hysterektomi varierar mellan cirka 5 och 25 % (stadium IA2–IB1) med ett genomsnitt på cirka 15 % 57. Om man konsekvent analyserar lymfkörtlarna innan hysterektomin skulle teoretiskt var sjätte kvinna slippa adjuvant strålbehandling och i stället erhålla primär definitiv kombinerad cytostatika- och strålbehandling; se avsnitt 10.3.1. Det finns emellertid ingen randomiserad studie som visar att överlevnaden är densamma och att sjukligheten minskar om man avstår från radikal kirurgi vid positiva körtlar utan ger strålbehandling i stället. Däremot finns det flera mindre retrospektiva studier där man menar att överlevnaden blir densamma vare sig man avbryter kirurgin vid positiva körtlar eller fortsätter med radikal kirurgi och sedan kompletterar med strålbehandling 204205.
I en studie av Marnitz och medarbetare ingick 448 patienter med livmoderhalscancer i stadium IA–IIA som lymfkörtelutrymdes laparoskopiskt där det gjordes peroperativt fryssnitt. Av de 394 med negativa körtlar där radikal hysterektomi utfördes, erhöll 10 % ändå adjuvant behandling p.g.a. små marginaler, positiva lymfkörtlar i definitivt PAD och andra riskfaktorer som gjorde att man inte kunde avstå från adjuvant behandling 206.
I andra studier utan peroperativ lymfkörtelundersökning sammanfattar Marnitz att motsvarande siffra är 20–30 % 206, vilket talar för att man med peroperativt fryssnitt kan minska andelen patienter som erhåller dubbla behandlingsmodaliteter.
I den retrospektiva observationsstudien ABRAX, studerades återfallsfri överlevnad och behandlingsrelaterad sjuklighet för avbrutna respektive fullföljda operationer vid peroperativt fynd av körtelmetastas. Studien visade att fullföljd hysterektomi inte var förenat med förbättrad överlevnad men högre frekvens komplikationer. Författarna konkluderade att kirurgin bör avbrytas vid peroperativa fynd av verifierade metastaser till förmån för definitiv radiokemoterapi 207.
Fertilitetsbevarande kirurgi
Rekommendationer
- Trakelektomi är ett alternativ till radikal hysterektomi för att bevara fertiliteten hos yngre kvinnor med tumör < 2 cm.
- Högriskhistologi utgör kontraindikation för radikal trakelektomi.
- Fertilitetsbevarande kirurgi vid IB1, bör diskuteras på nMDK fertilitetsbevarande kirurgi för ställningstagande till enkel eller radikal trakelektomi (se MDK kapitel) och vid IA2 vid behov t ex efter upprepade koniseringar.
Tekniken för att bevara fertiliteten vid tidig livmoderhalscancer beskrevs på mitten av 1990-talet och sedan dess har mer än 1 000 fall publicerats. Radikal trakelektomi innebär att en del av cervix med parametrier och vaginalmanschett avlägsnas, men corpus uteri sparas. Vanligen anläggs ett permanent cerklage för att minska risken för förtidsbörd. På detta sätt uppnås radikal kirurgi samtidigt som fertiliteten bevaras. Radikal trakelektomi kan utföras vaginalt (VRT), abdominellt (ART) eller robotassisterat laparoskopiskt 208209210. I en retrospektiv genomgång av patienter som opererats med radikal hysterektomi (RH) i New York, USA, under åren 1985–2001, fann man att 48 % av patienterna kunde varit aktuella för radikal trakelektomi om metoden hade varit etablerad 211. I Sverige är cirka 1/3 av livmoderhalscancerfallen under 40 år. Således kan en stor del av de patienter som får diagnosen vara aktuella för fertilitetsbevarande kirurgi.
Ett flertal riskfaktorer för lokalt återfall efter radikal trakelektomi har identifierats i retrospektiva analyser. I en studie från Frankrike 2002 fann man att en tumörstorlek på > 2 cm innebar en fyra gånger högre risk för återfall jämfört med en tumörstorlek på < 2 cm 212. Liknande resultat har redovisats i senare studier 213.
Risken för lokalt återfall förefaller vara jämförbar mellan kvinnor med adenokarcinom och skivepitelcancer, även om en något högre återfallsfrekvens sågs bland adenokarcinom i en sammanställning från Charitékliniken i Berlin 214. Småcellig neuroendokrin livmoderhalscancer har dålig prognos, och denna samt annan högriskpatologi utgör kontraindikation för radikal trakelektomi 215216.
Om ovanstående urvalskriterier tillämpas är det onkologiska resultatet mycket gott med en återfallsrisk på 1,9 % (ART) och 2,9 % (VRT) 213. I en fall–kontroll-studie från Toronto, Kanada, med 90 patienter där man jämförde VRT med RH var det ingen signifikant skillnad mellan metoderna med en 5-årsöverlevnad på 99–100 % 217.
Det är oklart huruvida man kan överföra SHAPE-studiens resultat till fertilitetsbevarande kirurgi vid stadium IB1. Dock förefaller det säkert att utföra enkel hysterektomi förbehållet vissa kriterier, se ovan avsnitt om kirurgiska principer 162, vilket torde kunna appliceras på fertilitetsbevarande kirurgi på så sätt att ett mindre radikalt ingrepp kan utföras i många fall. Eftersom det i nuläget råder oklarhet kring vilka evidens det går att luta sig mot bör alla fall som är aktuella för fertilitetbevarande kirurgi i stadium IB diskuteras på nMDK trakelektomi, se MDK-kapitlet.
Vid bedömning av obstetriskt utfall efter radikal trakelektomi bör man beakta i vilken grad kvinnorna aktivt försökt bli gravida, och i Speisers material från 2011 var denna andel endast drygt 35 % 218. Kvinnor som genomgått radikal trakelektomi har i första trimestern samma missfallsfrekvens som övrig befolkning, i vissa studier en lätt ökad risk för missfall i andra trimestern (5–14 % risk för missfall), men en klart ökad risk för prematurbörd relaterad till kort cervix 219220.
I en prospektiv studie omfattande 125 kvinnor som genomgått VRT blev 58 kvinnor gravida och totalt förekom 106 graviditeter. 20 % fick missfall i första trimestern, 3 % i andra. 4 % födde prematurt < 32 veckor 221. Resultaten är jämförbara, men något bättre än i uppföljande studier sammanfattade av Plante et al. [222]. I en sammanställning av det obstetriska resultatet efter robotassisterad radikal trakelektomi (RRT) från Sverige, noterades ett mycket högt graviditetsutfall på 81 % med 94 % födslar i tredje trimestern 170. Resultaten har bekräftats i en senare, större sammanställning från både svenska och internationella sjukhus som visade ett graviditetsutfall på 80% samt 86% födslar efter graviditetsvecka 32 223.
Liknande obstetriskt resultat kunde även ses i en retrospektiv studie från Västragötalandsregionen på VRT, där tillika långtidsuppföljd livskvalitet (global health statusscore) påvisades vara hög. Det kunde även konstateras i en senare studie från Skåne på RRT 223. En dansk studie på livskvalitet under det första året efter VRT visade på en försämrad livskvalitet där man jämfört med friska kontroller 224. I alla tre studier på livskvalitet var studiepopulationerna små (18-33 patienter).
Radikal trakelektomi kan övervägas vid tumörer med storlek > 2 cm, företrädesvis skivepitelcancer, förutsatt en gynnsam lokalisation (distal/exofytisk tumör) med tillräcklig (> 10 mm) tumörfri cervixlängd. Dessa fall ska diskuteras på MDK och genomgå såväl MRT som avancerat ultraljud för att så långt som möjligt utesluta mer proximal tumörutbredning.
Neoadjuvant cytostatikabehandling (NACT) i syfte att möjliggöra fertilitetsbevarande kirurgi vid
tumörer > 2 cm används vid ett flertal centra. Efter NACT och tumörutvärdering rekommenderas oftast en inledande portvaktskörteldiagnostik för att utesluta körtelmetastasering. I en översiktsartikel av Kol et al. rapporteras en återfallsrisk på cirka 10 % vilket är jämförbart med utfallet efter radikalkirurgi 225. Fertilitetsutfallet var tämligen lågt och av oklar anledning valde så få som 39 % av kvinnorna att försöka bli gravida efter genomgången behandling. Av dessa lyckades 70 % där 63 % av uppnådda graviditeter resulterade i ett levande fött barn (17 % av behandlade kvinnor). Prematuritetsrisken var 46 %. Erfarenheten av neoadjuvant cytostatikabehandling följt av trakelektomi är begränsad och långtidsresultaten osäkra. Fertilitetsbevarande behandling vid tumörer > 2 cm bör därför användas med stor försiktighet.
Komplikationer efter primär kirurgi
Närheten till stora kärl, uretär, blåsa, tarm och nerver medför risker för såväl peroperativa som postoperativa komplikationer. Olika operationstekniker (öppen, laparoskopisk med eller utan robotassistans) har ett varierande spektrum av komplikationer. Den peroperativa dödligheten är mycket låg, < 1 % 226.
Allmänna komplikationer såsom tromboembolism och ytliga och djupa infektioner förekommer, men har minskat med profylax samt minimalinvasiv kirurgi 227. Större blodförluster liksom behov av blodtransfusion var tidigare relativt vanligt, men har minskat kraftigt efter implementering av minimalinvasiv kirurgi (10–20 %). Robotassisterad kirurgi förefaller vara associerad med lägre blodförluster än traditionell laparoskopisk teknik 228. Skador på nerver som tillhör det autonoma nervsystemet är vanligt med funktionsstörningar av blåsa, tarm och sexuell funktion. Initial avlastning av urinblåsan med noggrann kontroll av residualurin är viktig i det tidiga postoperativa förloppet.
Skador på urinvägar och tarm
Cirka 1–2 % av patienterna med radikal hysterektomi utvecklar uretärfistlar. Robotassisterade ingrepp förefaller vara associerade med lägre frekvens urinvägskomplikationer än konventionell laparoskopisk teknik 228. Tarmfistlar är sällsynta och är associerade med peroperativ skada av rektum. Postoperativa adherenser ledande till ileus har beskrivits hos upp till 5 % efter öppen kirurgi 229.
Skador på nerver
Skador på nerver i lilla bäckenet rapporteras vara 1–2 %. Vanligast är skador på n. obturatorius vid lymfkörtelutrymningen medan andra skador har med uppläggning och självhållande retraktorer att göra 230. N. genitofemoralis är också utsatt vid pelvin lymfadenektomi och skador är relativt vanliga 231.
På grund av det autonoma nervsystemets närhet till cervix finns stor risk för peroperativa skador med effekter på blås-, tarm- och sexualfunktion. Påverkad blåsfunktion med olika grader av neurogen blåsrubbning ses hos upp till 80 % av opererade kvinnor. Den kan variera från en minskad känsla av blåsfyllnad till en komplett förlust av blåsfyllnadskänsla. Successiv förbättring sker inom första året men i en enkätstudie hade 16 % kvarvarande symtom 5 år efter operation och behövde använda bukpress för att tömma blåsan 232. Nervsparande kirurgisk teknik minskar sannolikt riskerna för påverkan på det autonoma nervsystemet, åtminstone gällande blåsfunktion 233.
Ansträngningsinkontinens kan uppstå efter radikal hysterektomi med successiv förbättring under det första året. Eftersom många använder bukpress vid blåstömning måste man ta hänsyn till detta inför en eventuell inkontinensoperation.
Störningar av tarmfunktionen inkluderar förstoppning, lös avföring och besvärande trängning till defekation. Även dessa störningar är kopplade till skador på det autonoma nervsystemet 234.
Vaginaltopp
Defekter i vaginaltoppen, eventuellt med framfall av tunntarm, varierar mellan olika operationsmetoder med en genomsnittlig frekvens på cirka 0,4 % vid laparotomi och en betydligt högre förekomst efter minimalinvasiv kirurgi 235. Efter robotkirurgi finns rapporter på upp till 10 % och man har spekulerat i om detta kan vara ett resultat av elektrokirurgi 236237.
Lymfvägar
I det tidiga förloppet är läckage av lymfvätska vanligt men upphör i regel spontant.
Symtomgivande lymfocelen uppstår i 5–34,5 % 226238 men behöver inte åtgärdas om de inte påverkar urinvägar eller ger symtom. Ultraljudsledd perkutan punktion med inläggning av dränerande kateter kan prövas, men medför viss risk för infektion. Eventuellt kan kirurgisk fenestrering behövas.
Lymfödem kan uppstå efter lymfkörtelutrymning och då ge svullnad, tyngdkänsla, värk och i vissa fall rörelseinskränkningar. I en enkätstudie angav 25 % måttliga till svåra besvär 5 år efter operation 232. Vissa studier har visat att ett ökat antal exstirperade lymfkörtlar ökar risken för lymfödem 239240, medan andra studier inte kunnat bekräfta detta. Stora lymfocelen (> 50 mm) förefaller öka risken för framtida lymfödem 241. Se även avsnitt 13.7.6 Lymfödem.
Kirurgi vid lokalt avancerad sjukdom
Enligt ovanstående rekommendationer ska patienter med lokalt avancerad sjukdom i första hand erhålla kombinerad cytostatika- och strålbehandling. Ett undantag kan emellertid utgöras av lokalt avancerad sjukdom utan engagemang av bäckenväggar (stadium IVA). I dessa relativt sällsynta fall kan kurativ exenteration övervägas som alternativ till kombinerad cytostatika- och strålbehandling om patientens allmänna tillstånd tillåter detta mer omfattande kirurgiska ingrepp; se vidare avsnitt 15.5 Kirurgisk behandling av återfall och 16.5 Tarm- och urinvägshinder, fistlar. Retrospektiva analyser från europeiska centrum talar för en relativt god 5-årsöverlevnad på drygt 50 % 242243.
Hysterektomi vid resttumör efter primär strålbehandling
Rekommendationer
- Där histologi visar resttumör i cervix 3–6 månader efter genomgången kombinerad cytostatika- och strålbehandling bör man överväga i första hand enkel hysterektomi även om det inte finns några randomiserade studier som visar förlängd överlevnad. Målet är ökad lokal kontroll.
Effekten av strålbehandling fortgår i minst 3 månader efter att behandlingen avslutats. Efter definitiv kombinerad cytostatika- och strålbehandling, avsnitt 10.3.1, görs en första behandlingsevaluering efter 3–6 månader med MRT och/eller PET-DT. Vid misstanke om resttumör görs en individuell bedömning som kan innebära histologisk verifiering av viabel tumör alternativt exspektans och ny bilddiagnostik efter ytterligare 3 månader för nytt ställningstagande till histologisk verifiering av resttumör.
Få studier redovisar värdet av kompletterande kirurgi efter primär strålbehandling. En randomiserad studie där patienter med livmoderhalscancer i stadium IB2–IIB behandlades med kombinerad cytostatika- och strålbehandling följt av antingen brachyterapi eller radikal hysterektomi med lymfkörtelutrymning pelvint och paraaortalt visade samma överlevnad i bägge grupperna. Kirurgin utfördes 4–6 veckor efter avslutad extern strålbehandling 244. Eftersom brachyterapi är av avgörande betydelse vid adekvat strålbehandling, behöver resultaten tolkas med försiktighet.
En retrospektiv multicenterstudie från Frankrike 2010 inkluderade 171 patienter med livmoderhalscancer i stadium IB2 och IIA2–IVA. Dessa behandlades på tre centrum där alla fick kombinerad cytostatika- och strålbehandling, men sedan skiljde sig behandlingen åt. Antingen gavs preoperativ brachyterapi följt av enkel eller radikal hysterektomi alternativt enbart brachyterapi. Man fann inga statistiskt säkerställda skillnader i grupperna, men en tendens till bättre överlevnad i kirurgigruppen. Däremot fann man ingen tendens till förbättrad överlevnad i den grupp av patienter som genomgått radikal kirurgi jämfört med enkel hysterektomi och fler biverkningar i den förra gruppen. Konklusionen var att om man ska göra hysterektomi på grund av resttumör är enkel hysterektomi det som rekommenderas 245.
Kirurgisk lymfkörtelutrymning inför definitiv kombinerad cytostatika- och strålbehandling
Rekommendationer
- Det saknas vetenskapligt stöd för att rekommendera lymfkörtelutrymning på patienter med lokalt avancerad livmoderhalscancer inför strålbehandling.
Kirurgisk lymfkörtelutrymning inför kombinerad cytostatika- och strålbehandling kan syfta till att dels styra strålfältet (dvs. utvidgat fält vid spridning till körtlar vid iliaca communis eller paraaortalt), dels avlägsna bilddiagnostiskt upptäckta metastaser. Det är ovanligt att patienter med livmoderhalscancer endast har paraaortal lymfkörtelmetastasering utan samtidiga pelvina körtelmetastaser 113. Paraaortal spridning är korrelerad till lymfkörtelmetastaser vid iliaca communis, bilaterala körtelmetastaser och multipla pelvina körtelmetastaser 135.
Vid makroskopisk pelvin körtelmetastasering beskrev Kupets et al. en teoretisk överlevnadsvinst hos 1 % av patienterna med stadium IB, 2 % med stadium IIB och 4 % med stadium IIIB, och man konkluderade att randomiserade studier skulle behöva vara så stora för att visa signifikanta skillnader att de inte skulle kunna genomföras 246. I en nyligen publicerad retrospektiv analys från Frankrike som omfattade 647 kvinnor observerades en överlevnadsvinst (HR 0,43) för gruppen (n = 377) som genomgått kirurgisk stadieindelning innan definitiv kombinerad cytostatika- och strålbehandling 247. Liknande resultat har även rapporterats av Marnitz som fann att hos de patienter där det gick att avlägsna mer än fem positiva körtlar levde patienterna längre än de där mindre än fem körtlar avlägsnades. Författarna menade att laparoskopisk kartläggning inklusive lymfkörtelutrymning har ett värde för patienten 248. I studien ingick inte utredning med PET-DT och omfattningen av den kombinerade cytostatika- och strålbehandlingen framgår inte, varför resultaten är svårvärderade.
En prospektiv randomiserad studie av lokalt avancerade tumörer i stadium IIB–IV där 29 patienter stadieindelades kliniskt och 32 patienter genomgick laparoskopisk lymfkörtelutrymning fick avbrytas i förtid då den progressionsfria överlevnaden var sämre i gruppen lymfkörtelutrymda. Uppföljningen visade att även överlevnaden var signifikant sämre i kirurgigruppen 217. Studien har kritiserats på grund av stora behandlingsskillnader mellan grupperna. I den prospektiva Uterus-11 studien randomiserades sammanlagt 240 kvinnor med lokalt avancerad livmoderhalscancer stadium IIB–IVA till endera kirurgisk stadieindelning följt av definitiv kombinerad cytostatika- och strålbehandling alternativt enbart definitiv kombinerad cytostatika- och strålbehandling 249. Resultaten från studien visade ingen skillnad i återfallssfri överlevnad mellan armarna, trots att kirurgisk stadieindelning resulterade i stadieuppgradering i 33% av fallen 164.
Kirurgisk behandling efter incidentellt fynd av livmoderhalscancer (ockult livmoderhalscancer)
Incidentell eller ockult livmoderhalscancer innebär att man oväntat diagnostiserar livmoderhalscancer vid hysterektomi p.g.a. annan indikation. Förekomsten är några procent av alla fall av livmoderhalscancer, enligt internationella studier 5–10 % 250251. Fullständig utredning, såsom vid nyupptäckt livmoderhalscancer, rekommenderas inkluderande klinisk undersökning i anestesi och bilddiagnostisk utredning. Ockult livmoderhalscancer kan inte stadieindelas enligt FIGO utan klassificeras enligt TNM 252. Det primära valet av behandling är kirurgi eller adjuvant kombinerad cytostatika- och strålbehandling. Behandlingsvalet bör följa samma principer som angivits för primärbehandling vid livmoderhalscancer.
PAD-verifierad ockult livmoderhalscancer som klassificeras som mikroinvasiv 1a1 kan betraktas som färdigbehandlad 250. Vid förekomst av LVSI eller vid stadium IA2 bör lymfdiagnostik övervägas samt vid 1B1 ≤ 10 mm invasionsdjup bör kompletterande lymfadenektomi genomföras. Fall med en tumörstorlek motsvarande FIGO-stadium ≥ IB1, med invasionsdjup > 10mm, 1B2 eller högre, är otillräckligt behandlade med enbart enkel hysterektomi 250 och bör genomgå resektion av parametrier, övre kolpektomi samt pelvin lymfadenektomi.
Fall av ockult livmoderhalscancer med tumörväxt i resektionsränder eller fynd av makroskopisk tumör i den vaginala resektionsranden (definitionsmässigt motsvarande FIGO-stadium II, dvs. TNM-stadium T2) rekommenderas kombinerad cytostatika- och strålbehandling. Samtliga fall av ockult livmoderhalscancer bör diskuteras på MDK.
Stumpcancer
Rekommendationer
- Den kirurgiska behandlingen följer i princip samma riktlinjer som för livmoderhalscancer i intakt uterus.
Cancerutveckling i cervix efter subtotal hysterektomi utgör en liten men ej försumbar andel av all livmoderhalscancer. Få studier finns publicerade om stumpcancer. I två svenska retrospektiva studier anges andelen till cirka 2 % av all livmoderhalscancer och att den har varierat över tiden men inte överstigit 3 % 253254. I två franska retrospektiva studier anges andelen stumpcancer något högre, 5,5–6,6 % 255256, men här har man också inkluderat fall av cancer in situ.
I en stor svensk retrospektiv studie från Radiumhemmet, omfattande över 8 000 patienter med livmoderhalscancer, hade 161 stumpcancer (2 %). Tiden mellan operationen med subtotal hysterektomi och diagnosen av stumpcancer var i medel 17,6 år, men varierade mellan 1 och 46 år 254.
Över 80 % av patienterna med stumpcancer har symtom i form av olaga blödningar (intermenstruella blödningar, coitusblödningar eller postmenopausala blödningar) eller flytningar. Symtomen har i genomsnitt funnits 3–4 månader innan diagnos. Åldern vid diagnos är cirka 10 år högre än för patienter med intakt uterus. Stadierna vid diagnos är också högre hos patienter med stumpcancer jämfört med patienter med livmoderhalscancer med intakt uterus 253. Dessa patienter har i stor utsträckning inte gått på cytologikontroller, vilket är en faktor att uppmärksamma, dvs. kvinnor som genomgår subtotal hysterektomi behöver tydligt informeras om behovet av fortsatt cellprovskontroll.
Invasiv livmoderhalscancer i en cervixstump diagnostiseras, såsom övrig livmoderhalscancer, med PAD från riktad biopsi vid kolposkopi eller konisering. Utredningen följer därefter den vid livmoderhalscancer med bevarad uterus, dvs. klinisk stadieindelning inklusive bilddiagnostik.
Den kirurgiska behandlingen av stumpcancer finns publicerad huvudsakligen i form av fallbeskrivningar 257258259260261262. De stora retrospektiva studierna innefattar huvudsakligen strålbehandling som primär behandling.
Den kirurgiska behandlingen följer i princip samma riktlinjer som för livmoderhalscancer vid intakt uterus.
Prognosen hos patienter med skivepitelcancer i cervix är densamma hos fall med stumpcancer jämfört med fall som diagnostiseras med livmoderhalscancer med intakt uterus, baserat på patienter som huvudsakligen fått strålbehandling som primär behandling. Fall av stumpcancer med adenokarcinom rapporteras ha en sämre prognos 254255256, men detta är baserat på små material. Risken för komplikationer av strålbehandling är dock större hos fall med stumpcancer jämfört med fall där uterus är intakt. Det beror på förändrad anatomi och adherenser i buken efter subtotal hysterektomi, åtminstone med dåtidens behandlingsmetoder.
Neoadjuvant cytostatikabehandling (NACT)
Rekommendationer
- Det saknas vetenskapligt stöd för NACT följt av radikalkirurgi vid lokalt avancerad livmoderhalscancer. För rekommendationer vid småcellig neuroendokrin livmoderhalscancer och i vissa fall av livmoderhalscancer under graviditet, se respektive kapitel.
Den rådande behandlingen för lokalt avancerad livmoderhalscancer (stadium IB3, IIA2–IIB) i dag i Sverige är kombinerad cytostatika- och strålbehandling se avsnitt 10.3.1 Definitiv kombinerad cytostatika- och strålbehandling. Vid dessa stadier förekommer lymfkörtelmetastasering i hög grad 137263264, se avsnitt 9.2.1 Spridning till lymfkörtlar. För att minimera risken för biverkningar av kirurgi följt av adjuvant behandling har man därför övergivit primärkirurgi vid lokalt avancerad livmoderhalscancer till förmån för definitiv kombinerad cytostatika- och strålbehandling 158.
Ett flertal singelcenter-studier och icke-randomiserade studier finns att tillgå vad gäller NACT följt av kirurgi vid lokalt avancerad livmoderhalscancer. Man har funnit en god tumörreduktion och kunnat minska det kirurgiska traumat och kunnat genomföra operationen med minimalinvasiv teknik. En Cochrane-översikt visar dock att i många studier har ett betydande antal patienter (45–100 %) även fått postoperativ adjuvant strålbehandling 265, vilket medför 2–3 gånger ökad risk för biverkningar av ≥ grad 3 200. Enligt denna Cochraneöversikt är kombinerad cytostatika- och strålbehandling den rekommenderade behandlingen, men NACT kan vara ett alternativ vid bristande tillgång till modern strålbehandling, såsom i utvecklingsländer.
Nyligen presenterades en fas II-studie från Japan där 51 patienter med livmoderhalscancer i stadium IB2–IIB fått tre kurer neoadjuvant cisplatin och dose-dense (veckovis) paklitaxel. Vid komplett eller partiell respons utfördes radikal hysterektomi efterföljt av ytterligare två kurer cisplatin och paklitaxel. Denna metod gav en 2-årig sjukdomsfri överlevnad på 88 % och en total överlevnad på 94 % 266.
I en retrospektiv genomgång av 333 neoadjuvant behandlade patienter med lokalt avancerad livmoderhalscancer (stadium IB2–IIB) diskuteras postoperativ adjuvant behandling 267. För patienter som svarade optimalt på den neoadjuvanta behandlingen gick det lika bra vare sig de fick postoperativ strålbehandling eller cytostatikabehandling eller ingen behandling alls 267, vilket talar för en generell känslighet för eller resistens mot cytotoxisk behandling.
I en nyligen publicerad europeisk fas III-studie (EORTC protocol 55994), där totalt 620 kvinnor med stadium IB2–IIB randomiserades till definitiv radiokemoterapi eller till minst tre cykler neoadjuvant cisplatin-baserad cytostatikabehandling följt av radikal hysterektomi, redovisades negativa resultat med likvärdig överlevnad mellan behandlingsarmarna (PMID 37656948). Resultat från en randomiserad fas III-studie med liknande design där sammanlagt 635 kvinnor med stadium IB2, IIA–B inkluderats 268 rapporterade signifikant bättre överlevnad i standardarmen (definitiv kombinerad cytostatika- och strålbehandling).
Sammantaget finns idag inget vetenskapligt stöd för att rekommendera NACT följt av radikalkirurgi vid lokalt avancerad livmoderhalscancer.
Väntetid till kirurgi
Det finns endast begränsad kunskap om betydelsen av väntetiden från behandlingsbeslut till kirurgi, avseende tumörprogress. I en studie vid livmoderhalscancer i stadium ≤ IB1 (n = 123) sågs tumörprogress (storlek) hos 9 % i hela gruppen. Alla dessa hade en väntetid på > 28 dagar från bedömning av gynekologisk tumörkirurg till kirurgi, medan man inte såg progress hos någon vid en väntetid på < 28 dagar 269. Endast en patient hade ett högre stadium vid kirurgi än vid diagnos (stadium IIB vs. IB1). Baserat på denna enda studie förefaller det ändå rimligt att eftersträva operation inom 1 månad, även om risken för progress är måttlig vid längre väntetid. Dock bör utrednings- och väntetiden minimeras även av psykologiska skäl, varför ingen definitiv maximalt acceptabel tidsgräns kan rekommenderas.
Strålbehandling
Definitiv kombinerad cytostatika- och strålbehandling
I definitiv kombinerad cytostatika- och strålbehandling ingår optimalt en kombination av brachyterapi (BT), extern strålbehandling (EBRT) och konkomitant platinumbaserad cytostatikabehandling.
Indikation: Livmoderhalscancer stadium IB3, IIA2–IVA.
Rekommendationer
- Patienten bör erhålla en total slutdos (EQD2) från extern strålbehandling och cervikal brachyterapi motsvarande D90 % > 85 Gy till primärtumören/cervix (HR-CTV) om möjligt med hänsyn till riskorgan.
- Brachyterapins del utgörs optimalt av D90 % = 35–40 Gy (EQD2) till HR-CTV, t.ex. 4 fraktioner HDR-BT, 7 Gy/fraktion, beroende på fraktionering och dos från extern strålbehandling och dos till riskorgan.
- Patienten bör erhålla extern strålbehandling 1,8–2,0 Gy/fraktion till en slutdos av minst 45 Gy (EQD2) mot elektiv bäckenlymfkörtel- och parametrievolym.
- Bilddiagnostiskt misstänkta lymfkörtelmetastaser bör erhålla en total stråldos (EBRT + BT) motsvarande 55–64 Gy (EQD2) beroende på storlek.
- Vid bilddiagnostiska tecken på spridning till lymfkörtlar vid iliaca communis och/eller paraaortalt bör paraaortal bestrålning övervägas till en slutdos av minst 45 Gy mot elektiv paraaortal lymfkörtelvolym.
- IMRT-/VMAT-teknik bör användas för att minska toxiciteten med beaktande av dosbegränsningar till riskorgan.
- Patienten bör erhålla konkomitant veckovis cisplatin 40 mg/m2 under pågående EBRT, optimalt 6 cykler, maxdos 70 mg per behandling.
- Vid anemi inför och under pågående EBRT bör patienten transfunderas till ett Hb-värde på ≥ 120 g/L.
- Patienten rekommenderas rökstopp.
- Behandlingen bör vara avslutad inom 50 dagar från behandlingsstart.
Bakgrund
Extern strålbehandling (EBRT, external beam radiation therapy)
Sedan 1960-talet har flera studier för olika tumörsjukdomar visat att stråldoser till 45–50 Gy är effektivt för att eradikera subklinisk mikrometastasering med acceptabel toxicitet 165. Resultat från en samlad analys av amerikanska så kallade ”patterns of care”-studier visar att en total stråldos motsvarande D90 % > 85 Gy omräknat i 2 Gy-fraktioner (EQD2) till HR-CTV (high risk clinical target volume; makroskopisk resttumör vid tiden för brachyterapi) behövs för att uppnå lokal kontroll i bäckenet 166. Liknande data har visats i en retrospektiv analys från Wien där Dimopoulos och medarbetare konstaterar att en dos på D90 % > 87 Gy (EQD2) till HR-CTV minskar risken för lokalt återfall från 20 % till 4 % 167.
Vid bilddiagnostisk misstanke om lymfkörtelmetastaser bör dessa erhålla högre stråldos, så kallad boost. Det finns inga randomiserade studier som belyser vilka dosnivåer som anses tillräckliga för att eradikera makrometastaser. I enlighet med tidigare erfarenheter, dos-kontrollstudier vid strålbehandling samt rekommendationer inom ramen för de pågående EMBRACE-studierna rekommenderas en sammanlagd dos (EBRT + brachyterapi) på 55–60 Gy för körtelmetastaser ≤ 2 cm och 60–64 Gy för körtelmetastaser > 2 cm 168. Boost kan ges sekventiellt (direkt i anslutning till den initiala strålbehandlingen) eller integrerat (SIB, simultan integrerad boost). SIB anses kunna minska dosen till OAR med bibehållen god dosfördelning till target.
Konkomitant cytostatikabehandling
Kombinerad cytostatika- och strålbehandling, tillägg av cytostatikabehandling under pågående strålbehandling, syftar till att dels öka tumörcellernas känslighet för strålbehandlingen, dels utplåna eventuell subklinisk spridning utanför strålfältet. 1999 publicerades fem studier som visade att tillägg av platinumbaserad cytostatikabehandling under pågående strålbehandling förbättrade möjligheten till lokal kontroll och total överlevnad för samtliga stadier av livmoderhalscancer 169. Detta har senare bekräftats i två metaanalyser av 24 respektive 15 studier 170171. Generellt sett gäller att studierna är relativt heterogena, att försöksarmarna innehåller delvis olika cytostatikaregimer och att i två fall även adjuvant cytostatikabehandling givits efter avslutad kombinerad cytostatika- och strålbehandling. I en fördjupad analys av Vale och medarbetare finns en trend till att effekten på 5-årsöverlevnaden är större i tidiga än i sena stadier med en tioprocentig överlevnadsvinst för stadium IA–IIA jämfört med tre procent för stadium III–IVA. För hela populationen ses dock en signifikant åttaprocentig sjukdomsfri överlevnadsvinst (från 50 % till 58 %) och en sexprocentig total överlevnadsvinst (från 60 % till 66 %) efter fem år 171.
Strålbehandlingen är grunden för behandlingen och tillägg av konkomitant cytostatikabehandling får inte äventyra att strålbehandlingen kan fullföljas. Vid påverkat allmäntillstånd eller påverkade blodvärden prioriteras således strålbehandlingen över cytostatikabehandlingen, med undantag av strålfältet till paraaortala lymfkörtlar. Se vidare avsnitt 10.3.1.3 Strålbehandling riktad mot paraaortala lymfkörtelstationer (PA-fält).
När platinumbaserad cytostatikabehandling planeras är det nödvändigt med adekvat njuravflöde, vilket medför indikation för nefrostomi vid hydronefros även i avsaknad av symtom eller förhöjt kreatinin.
Brachyterapi
Brachyterapi (BT) är av avgörande betydelse i en framgångsrik behandling av livmoderhalscancer 172173. Ordet brachy kommer från grekiskan och betyder ”nära”, dvs. brachyterapi är närbestrålning. Se vidare avsnitt 10.3.1.5 Brachyterapi (BT).
Targetdefinition EBRT
Dosplanering ska enligt SSMFS 2018:5, Strålsäkerhetsmyndighetens författningssamling : Strålsäkerhetsmyndighetens föreskrifter om medicinsk strålbehandling, göras på underlag från DT eller MRT. Dosplanerings-DT utförs i behandlingsposition från diafragma till nedom tuber ischiadicum, i max 3 mm tjocka snitt. Intravenöst kontrastmedel underlättar definition av target och riskorgan (organs at risk, OAR) om DT används som enda planeringsmetod. Om MRT för volymsdefinitioner finns som tillgänglig metod utförs även denna i behandlingsposition. Även diagnostisk MRT-undersökning kan fusioneras med DT i dosplaneringsprogrammet, men det kräver noggrant överensstämmande undersökningsprotokoll med samma planvinklar och snitt-tjocklek, utförd i behandlingsläge. Om MRT används som dosplaneringsunderlag avstår man från i.v. kontrastmedel vid DT. Bilddiagnostikunderlagen sparas om möjligt i lokalt PACS.
Ett internationellt samarbete mellan de större strålbehandlingsorganisationerna har lett fram till riktlinjer för definition av targetvolymer vid planering av EBRT vid avancerad livmoderhalscancer 175. Författarna konstaterar att cervix inklusive primärtumören, uterus, del av vagina, parametrier, samt pelvina och ev. inguinala eller paraaortala lymfkörtelstationer ska betraktas som målorgan och ingå i ”clinical target volume” (CTV).
Under förutsättning att det inte finns indikation för paraaortal körtelbestrålning, se nedan, eller konstaterad cancerväxt i vagina bör övre begränsning av CTV vara 7 mm under L4–L5-disken och nedre begränsning av CTV 3 cm nedom vaginaltoppen eller 1 cm ovan foramen obturatorius nedre gräns, vilket som är mest kaudalt. CTV får i medellinjen aldrig vara mindre än 1,5 cm i anterior – posterior riktning. Vid FIGO-stadium IIIA bör hela vagina samt inguinala lymfkörtelstationer inkluderas i CTV. Vid PA-fält (paraaortalt fält) är den övre gränsen för elektiva lymfkörtlar som regel i njurkärlsnivå, alternativt 3 cm ovan makroskopiskt misstänkt lymfkörtelmetastas. Se vidare bilaga 1. Marginaler från CTV till den volym som används vid dosplanering för att säkerställa dosen till CTV för EBRT, ”planning target volume” (PTV), skapas utifrån lokala förutsättningar 176. Se vidare bilaga 1 och bilaga 4.
För definitionen av CTV för lymfkörtelstationer i bäckenet har Taylor och medarbetare utarbetat riktlinjer som i korthet innebär att med en modifierad 7 mm-marginal kring de större bäckenkärlen täcks 99 % av berörda pelvina lymfkörtlar 177. Makroskopiska körtlar ska inkluderas och CTV bör nå ut till bäckenväggar och psoasmuskulaturen. En liknande definition av CTV för lymfkörtelstationerna i bäckenet vid adjuvant postoperativ strålbehandling har formulerats av Small och medarbetare inom ramen för RTOG 176. För utförligare definitioner av respektive CTV, se bilaga 1 och bilaga 4.
Strålbehandling riktad mot paraaortala lymfkörtelstationer (PA-fält)
Rekommendationer
- Vid bilddiagnostiska tecken på eller konstaterad spridning till lymfkörtlar vid iliaca communis och/eller paraaortalt bör man ge ett förlängt paraaortalt strålfält med beaktande av dosbegränsningar till riskorgan inklusive benmärg.
- Patienten bör erhålla extern strålbehandling 1,8–2,0 Gy/fraktion till en slutdos av 45 Gy (EQD2) till elektiv paraaortal lymfkörtelvolym.
- Bilddiagnostiskt misstänkta paraaortala lymfkörtelmetastaser bör erhålla en total stråldos (sekventiell eller simultan integrerad boost) motsvarande 55–64 Gy beroende på storlek och med beaktande av dosbegränsningar till riskorganen.
Risken för paraaortal (PA) lymfkörtelmetastasering ökar med stadium. I en stor retrospektiv studie med 621 patienter konstaterar författarna 5 % PA metastasering vid stadium I, 16 % vid stadium II och 25 % vid stadium III. Det är ovanligt att patienter med livmoderhalscancer endast har paraaortal lymfkörtelmetastasering utan samtidiga pelvina körtelmetastaser 111, utan detta är korrelerat till lymfkörtelmetastaser vid iliaca communis, bilaterala körtelmetastaser och multipla pelvina körtelmetastaser 135. Misstänkta körtelmetastaser enligt MRT/DT bör om möjligt verifieras med punktion. Alternativt rekommenderas kompletterande undersökning med PET-DT och vid ökat upptag betraktas positiva körtlar som metastaser även utan punktion. Vid positiva körtlar ändras stadieindelningen enligt nya FIGO-klassifikationen.
Det finns inga entydiga studier om värdet av profylaktisk paraaortal körtelbestrålning vid livmoderhalscancer. 2016 publicerades en metaanalys där endast fyra randomiserade studier som jämför bäckenbestrålning (n = 506) och bäckenbestrålning och paraaortal bestrålning (n = 494) identifierades. I samtliga studier hade behandlingen givits med äldre stråltekniker, och i tre av studierna hade inte någon konkomitant cisplatin givits. I samtliga fall där en preterapeutisk staging utförts (87,5 %) fanns ingen spridning till paraaortala lymfkörtlar. Sammanfattningsvis minskade andelen paraaortala återfall (HR 0,35, p < 0,01) och andelen distansmetastaser (HR 0,69, p = 0,03) signifikant i gruppen som erhållit paraaortal bestrålning medan den cancerspecifika överlevnaden inte påverkades signifikant (HR 0,68, p = 0,06) 178. På grund av olika skattningsskalor av behandlingsrelaterade biverkningar i de olika studierna gick det inte att dra några generella slutsatser rörande toxicitet.
I en förnyad metaanalys från Cochrane 2018 inkluderades endast tre av ovanstående studier p.g.a. metodologiska svagheter i den fjärde studien (ofullständig randomisering). Sammanfattningsvis konstaterade författarna en signifikant överlevnadsvinst vid paraaortal bestrålning (HR 0,67) och minskad risk för paraaortala återfall (RR 0,36). Man identifierade även en fjärde studie i vilken patienterna erhållit konkomitant cytostatikabehandling i båda armarna med en signifikant överlevnadsvinst för patienterna som erhållit paraaortal bestrålning (HR 0,37), men författarna till metaanalysen bedömde att den vetenskapliga kvaliteten på studien var så pass låg att inga övertygande slutsatser bör dras 179.
I en amerikansk studie från 1999 (RTOG 90-01) randomiserades 389 patienter med stadium IB eller IIA med en tumördiameter större än 5 cm, eller stadium IIB till IVA, till kombinerad cytostatika- och strålbehandling med bäckenfält upp t.o.m. kota L4, eller bäckenfält och paraaortalt fält utan konkomitant cytostatikabehandling. En uppdaterad analys av studien visade en tydlig fördel för armen med kombinerad cytostatika- och strålbehandling med en beräknad 5‑årsöverlevnad för stadium IB och II respektive III och IVA på 79 % respektive 59 %, jämfört med 55 % respektive 45 % i armen som enbart erhållit EBRT 180.
Därutöver finns ett antal retrospektiva studier där man tillämpat modernare stråltekniker (IMRT) med konkomitant cisplatin, men med motstridiga resultat. I en liten enkelarmad studie från 2014 erhöll 32 patienter med PET-DT-positiva pelvina lymfkörtlar pelvin paraaortal EBRT. Jämfört med 47 matchade historiska kontroller konstaterar författarna en total respektive sjukdomsfri 3-årsöverlevnad på 87 % respektive 82 %, jämfört med 62 % respektive 54 % till förmån för patienterna som behandlats med paraaortal EBRT. Vidare konstaterade författarna inga PA-metastaser och färre distansmetastaser i gruppen som behandlats med PA-fält 181. En taiwanesisk studie från 2017 visade att patienter i en högriskgrupp, definierade som FIGO 2009 stadium III–IVA eller med positiva pelvina lymfkörtlar, hade en signifikant bättre överlevnad vid både pelvin och paraaortal EBRT (n = 96) jämfört med enbart pelvin EBRT (n = 110) (HR 0,35, p = 0,02) utan någon signifikant skillnad i allvarlighetsgrad eller frekvens av biverkningar 182. I motsats till dessa två studier publicerade Oh och medarbetare en studie 2017 som inte visade någon signifikant skillnad med avseende på paraaortala återfall eller tioårsöverlevnad mellan en kohort som enbart erhållit bäckenbestrålning (n = 74) jämfört med en kohort som behandlats med paraaortalt fält (n = 52), men signifikant högre andel gastrointestinala biverkningar i den senare gruppen 183.
Multipla bäckenlymfkörtelmetastaser, bilaterala körtelmetastaser även om de är få, och metastaser vid iliaca communis ökar risken för paraaortala körtelmetastaser 135. Men indikationerna för vilka patienter som bör erhålla utökad PA-strålbehandling varierar mellan olika riktlinjer. Enligt europeiska ESGO:s riktlinjer från 2018 rekommenderas endast utökat fält vid konstaterad paraaortal metastasering, medan amerikanska NCCN:s riktlinjer från 2019 rekommenderar att patienter med metastasering till lymfkörtlar vid iliaca communis eller paraaortalt bör erhålla ett kompletterande PA-fält 184. Studieprotokollet för EMBRACE II har vidare indikationer och där rekommenderas PA-fält vid metastasering till iliaca communis, vid metastasering till fler än två pelvina lymfkörtlar, vid körtelmetastas över två cm eller vid bilateral pelvin körtelmetastasering.
Vid konstaterad paraaortal lymfkörtelmetastasering ges traditionellt PA-fält samt eventuell boost mot positiva körtlar till en sammanlagd dos av 60–64 Gy. Risken är dessvärre stor för distansmetastaser i denna patientgrupp med en treårsöverlevnad på cirka 40 %, varför behovet av ytterligare studier för att utvärdera effekten av postradioterapeutisk cytostatikabehandling är stort 111185. Behandling med PA-fält ökar även risken för biverkningar av ≥ grad 3 till 34–84 % för akuta biverkningar och till 14–40 % för seneffekter med konventionell teknik. Med IMRT-teknik mot bäckenet har man i små studier sett att biverkningsfrekvensen reduceras till cirka 23–76 % (akuta) respektive 10 % (sena) 185186.
Toleransnivåer och riskorgan vid EBRT
1991 publicerades en av de första artiklarna som försökte definiera toleransnivåerna för olika organ vid EBRT utifrån hur stor volym av organet som bestrålades 187. Därefter har flera retrospektiva studier analyserat förhållandet mellan stråldos, organvolym och komplikationer, inklusive seneffekter. År 2010 publicerades en omfattande genomgång av studier och litteratur på området inom ramen för QUANTEC-nätverket, ”quantative analyses of normal tissue effects in the clinic” 188. Vid EBRT av bäckenet är det framför allt rektum, urinblåsa, tunntarm och höftleder som traditionellt har betraktats som riskorgan, ”organs at risk” (OAR) 189. Ovarierna har en så pass låg toleransnivå att de vid definitiv kombinerad cytostatika- och strålbehandling sällan går att ta hänsyn till. Se även avsnitt 10.3.2 för diskussion kring ooforopexi. Ett ökat intresse finns även för att definiera toleransnivåer för benmärg och vagina inklusive den integrerade dosen från brachyterapi 189190. Vid PA-fält måste man dessutom ta hänsyn till njurar och medulla. Se tabell i bilaga 5.
I en randomiserad fas III-studie publicerad 2021kunde man visa att EBRT given med bildstyrd IMRT-teknik signifikant minskade toxiciteten efter strålbehandling utan att försämra risken för återfall jämfört med konventionell behandlingsteknik 191. I studien hade 300 patienter planerade för adjuvant radio(kemo)terapi randomiserats mellan de två behandlingsteknikerna. Patienterna utvärderades kliniskt, radiologiskt samt med validerade enkäter. Med en median uppföljningstid på 46 månader kunde man visa att den kumulativa 3-årsincidensen av senbiverkningar av grad ≥ 2 var 28,1% efter IMRT jämfört med 42,9% efter konventionell behandling. Mest uttalad var skillnaden vad gäller toxicitet relaterat till tarmkanalen, men för alla rapporterade biverkningar var frekvensen lägre efter IMRT jämfört med efter konventionell behandling. Detta är den första randomiserade fas III-studien i ämnet och ger tydligt stöd för användandet av IMRT-teknik vilket bekräftar vad man tidigare funnit i flera retrospektiva studier.
I en metaanalys av Yang och medarbetare av 13 studier med sammanlagt 222 patienter behandlade med IMRT-teknik jämfört med 233 med konventionell EBRT, konstateras att rektumvolymen hos dem som erhöll 45 Gy (V45Gy) var 39,5 % mindre till förmån för IMRT-gruppen och motsvarande tunntarmsvolym (V45Gy) 17,3 % mindre. Man kunde dock inte konstatera någon signifikant skillnad för motsvarande volymer till urinblåsa eller benmärg 192.
För utförligare definitioner av toleransnivåer och risken för biverkningar för respektive OAR, se bilaga 2 (BT) och bilaga 5 (EBRT).
Brachyterapi (BT)
Brachyterapi är av avgörande betydelse i en framgångsrik behandling av livmoderhalscancer 172173. Då tumörvolymen (gross tumour volume, GTV) är en av de mest betydelsefulla prognostiska faktorerna för lokal kontroll är det av väsentlig betydelse att behandla hela GTV med tillhörande subklinisk tumörvolym (clinical target volume, CTV) till en tillräckligt hög dos. Det snabba dosfallet hos brachyterapi medger en mycket hög dos centralt i bäckenet medan blåsa, rektum, sigmoideum och tunntarm kan sparas till en del.
Intrakavitär brachyterapi (IC BT) vid livmoderhalscancer har tidigare baserats på punktdoser och standardiserade planer, men det senaste decenniet har MRT-baserad tredimensionell planering av IC brachyterapi vunnit fotfäste med förankring i publicerade europeiska data (GEC-ESTRO Recommendations I–IV 193194195196 och amerikanska riktlinjer för 3D-baserad brachyterapi 197198199200, så kallad image-guided brachytherapy, IGBT, eller image-guided adaptive brachytherapy, IGABT, när man tar hänsyn till tumörkrympning över tiden.
En arbetsgrupp inom GEC-ESTRO introducerade år 2000 3D-baserad dosplanering för brachyterapi. En gemensam terminologi utarbetades och MR-baserad behandlingsplanering infördes. Då tumörvolymen ändras påtagligt under den externa behandlingen specificeras den vid dels diagnos (GTVD och CTVD), dels tiden för brachyterapi (GTVBT och CTVBT). Beroende på återfallsrisken och därmed targetdosen delar man in target i högrisk-CTV (HR-CTV) och intermediärrisk-CTV (IR-CTV) 193. IR-CTV är den tumörvolym som föreligger vid start av den externa strålbehandlingen. HR-CTV är den tumörvolym som föreligger vid start av brachyterapi 193; se bilaga 3.
Den primära vinsten vid denna teknik är möjligheten att anpassa och konformera den höga dosen från brachyterapi till anatomin och tumörutbredningen hos varje individuell patient, anpassad till både eventuell tumörkrympning från extern strålbehandling och cytostatikabehandling, samt läge av närliggande riskorgan (blåsa, rektum, sigmoideum och vagina). Seneffekter grad 3–4 från tarm och blåsa har minskat från 10 % med 2D brachyterapi till 2 % med 3D brachyterapi 201202. Det är även möjligt att kombinera intrakavitär (IC) och interstitiell (IS) brachyterapi och uppnå en betydande förbättrad täckning av target vid avancerad tumörutbredning 203204.
Förutom kliniska undersökningar, med angivande av tumörvolym i tre dimensioner (+ teckning), görs i dag MRT för bedömning av tumörstorlek och tumörutbredning både vid diagnos, ”pre-RT-MRT”, och inför brachyterapi, ”BT-MRT”. Marginalerna för targetvolymen bestäms med hänsyn till tumörkrympning.
Brachyterapi ges antingen parallellt under den senare delen av den externa strålbehandlingen eller efter avslutad extern behandling. Bildunderlaget för dosplanering utgörs av MRT-bilder eller DT-bilder.
MRT-undersökning spelar en avgörande roll vid bilddiagnostik inför en lyckad implementering av 3D brachyterapi vid livmoderhalscancer. Med överlägsen bildåtergivning av mjukvävnad visualiseras targetvolymer och riskorganen bättre. Apparatur, patientförberedelser och bildtagningsprotokoll behövs; se nedan och bilaga 2.
Gold standard för bildåtergivning är T2-viktade bilder med transversell, sagitell, coronal och oblique bildorientering. Para-axiala, sagitella och para-coronala bilder är orienterade utmed längsaxeln på cervikala applikatorn:
Figur 7. Hämtat ur: Dimopoulos et al, R&O, 2012 196
 Vid repetitiva MRT-undersökningar bör samma bildåtergivning användas för att underlätta orientering och bedömning av tumörrespons under pågående strålbehandling. För applikatorrekonstruktion rekommenderas en para-transversell bildserie med 1–3 mm mellan snitten. Helst bör targetritning och applikatorrekonstruktion utföras på samma bildserie för att undvika osäkerhet vid fusion av bilder.
Vid repetitiva MRT-undersökningar bör samma bildåtergivning användas för att underlätta orientering och bedömning av tumörrespons under pågående strålbehandling. För applikatorrekonstruktion rekommenderas en para-transversell bildserie med 1–3 mm mellan snitten. Helst bör targetritning och applikatorrekonstruktion utföras på samma bildserie för att undvika osäkerhet vid fusion av bilder.
I GEC-ESTRO:s rekommendationer för 3D IGABT för brachyterapi vid livmoderhalscancer ingår kumulativa dos-volymhistogram (DVH). Dos-volym-parametrarna D90 % och D98 % för GTV, HR-CTV och IR-CTV är den lägsta dosen som givits till 90 och 98 % av respektive volym: 194. Ekvivalent stråldos i 2 Gy/fraktion (EQD2) beräknas för extern strålbehandling och brachyterapi sammantaget.
För riskorganen (tarm, blåsa och vagina) beräknas den lägsta dosen i den med högst dos bestrålade vävnadsvolymen närmast applikatorn i 0,1 cm3, 1 cm3 och 2 cm3.
Lokal tumörkontroll på 96 % för stadium IIB och 86 % för stadium IIIB vid 3-årsuppföljning har rapporterats med 3D ”conformal” EBRT +/- cytostatikabehandling plus MRT-ledd intrakavitär brachyterapi inklusive interstitiella nålar vid avancerad sjukdom, D90 % ≥ 85 Gy. Cancerspecifik 3-årsöverlevnad var 84 % för stadium IIB och 52 % för stadium IIIB 205.
Det pågår multicenterstudier av IGABT utgångna från Universitetssjukhuset i Wien, Österrike: EMBRACE (European study on MRI-guided brachytherapy in locally advanced cervical cancer). I juni 2014 var 1 140 patienter registrerade i EMBRACE. Under 2016 startar EMBRACE II baserat på klinisk evidens från tidigare EMBRACE-studier (EMBRACE I, retro-EMBRACE) 206207.
Typiska biverkningar från brachyterapin såsom lokal inflammation, fibros, telangiektasier, ulceration, nekros och fistlar uppstår huvudsakligen i begränsade volymer i anslutning till applikatorn och vid höga doser (> 70–80 Gy), medan biverkningar från hela organ i form av generell inflammation, fibros och telangiektasier uppkommer efter bestrålning av helt organ med intermediära eller höga doser (60–70+ Gy).
Teknik
Brachyterapi ges med efterladdningsteknik med en stegande strålkälla, där olika dosrater (stråldos per tidsenhet) kan användas. I Sverige används i dag endast högdosrat brachyterapi (HDR-BT) och pulsad dosrat brachyterapi (PDR-BT) där iridium (192Ir) används som strålkälla. HDR-BT ges på en strålbehandlingsavdelning och själva behandlingen tar kort tid, vanligtvis 15–20 minuter, medan PDR-BT ges i strålskyddade rum på en vårdavdelning och där behandlingstiden varierar, beroende på targetdos och antalet pulser. Se vidare avsnitt 13.8 Omvårdnad i samband med brachyterapi. För båda teknikerna tillkommer tid för applikation, bilddiagnostik, targetdefinition och dosplanering.
För tredimensionell (3D) IGABT, med bestämning av tumörutbredning, tillhörande targetvolym och riskorgan samt optimering av dosfördelningen i tre dimensioner, krävs MRT-undersökning med applikatorn på plats, optimalt inför varje fraktion 193, eller som minimum vid första brachyterapi-fraktionen följt av DT vid efterföljande fraktioner 208. Diagnostisk MRT (T2-viktad) utförs därutöver nära före första brachyterapin för utvärdering av tumörutbredning.
Targetvolymen för brachyterapi definieras utgående från bilddiagnostisk information, inspektion och palpation vid start av EBRT och vid applikationstillfället, och dokumenteras på mallar (teckning), som stöd vid planering och monitorering under hela behandlingsförloppet (EMBRACE); se figur 5 i avsnitt 6.3 Palpation i narkos (PIN) och nedladdningsbar bilaga.
Patienten är i generell eller spinal anestesi vid applikation av instrumenten.
För optimalt resultat används applikatorer anpassade till patientens anatomi och tumörutbredning tillsammans med en individuellt optimerad dosplan, där dosplanen är baserad på ett 3D-bildunderlag med inritade strukturer (targets och OAR); se bilaga 2 och bilaga 3.
En tandemapplikator med intrauterin sond och vaginal ringapplikator används som standard. Vid tumörutbredning i parametrier där stråldosen inte täcks av endast dessa instrument används tillägg av interstitiella nålar.
Figur 8. Tandemapplikator med intrauterin sond och vaginalapplikator, utan och med interstitiella nålar (Elekta)
 Vid tumörutbredning vaginalt (stadium IIIA, utbrett stadium IIA) används ofta en intrauterin sond och vaginalcylinder eventuellt med tillägg av interstitiella nålar.
Vid tumörutbredning vaginalt (stadium IIIA, utbrett stadium IIA) används ofta en intrauterin sond och vaginalcylinder eventuellt med tillägg av interstitiella nålar.
Vid applikation bör transabdominalt ultraljud användas som guide, detta för att undvika perforering av uterus. Packning av vagina med tamponad ska göras för att öka avståndet från applikatorn till riskorganen (blåsa och rektum) och för att säkerställa att applikatorn inte glider ur läge.
Targetdefinition brachyterapi (BT)
Targetvolymen utgörs av tumörvolymen och hela cervix så som den bedöms vid en gynekologisk undersökning med inspektion och palpation, samt på MRT inklusive ”grey zones” (intermediär signal på MRT representerande risk för resttumör) vid tiden för brachyterapi (HR-CTVBT) och IR-CTVBT baserad på IR-CTV (initial makroskopisk tumörutbredning) samt HR-CTVBT + 5–15 mm säkerhetsmarginal beroende på tumörstorlek och läge, potentiell tumörspridning, tumörregression, bildunderlag, organrörelser och behandlingsstrategi (fördelning EBRT vs. brachyterapi och beaktande av OAR) 193. Se bilaga 2. Även OAR (blåsa, rektum, sigmoideum samt optimalt vagina) ska definieras.
Figur 9. Frontal och transversell schematisk bild av lokalt avancerad livmoderhalscancer med partiell remission efter extern strålbehandling 194

Total behandlingstid och total dos
Brachyterapi startas tidigast efter 20–30 Gy EBRT, när tumörens storlek har krympt. Brachyterapi och extern strålbehandling ges vanligen inte samma dag, men i sådana fall med minst sex timmars intervall.
Stråldoser vid brachyterapi
Den totala stråldosen, D90 %, inklusive EBRT, till HR-CTV bör vara > 85 Gy 209. Brachyterapins del utgörs optimalt av 35–40 Gy (EQD2).
Enligt den kommande studien EMBRACE II har följande minimi-dosgränser satts upp:
|
HR-CTV |
D90 % > 85 Gy (EQD2, α/β = 10), D98 > 75 Gy (EQD2, α/β = 10) |
|
GTVBT1--- |
D98 % > 90 Gy (EQD2, α/β = 10) |
Ett förslag på fraktioneringsschema för HDR-BT kan vara 4 fraktioner, 7 Gy/fraktion. För PDR-BT kan motsvarande antal fraktioner och dos per fraktion räknas fram, se bilaga 2 under dosberäkningar vid brachyterapi. Se vidare bilaga 2, där det även finns en länk till ett beräkningsark (Excel).
Toleransnivåer och riskorgan vid brachyterapi (BT)
Man bör uttrycka dosen till riskorganen som den lägsta dosen i den delvolym som erhåller högst dos (se figur 10). Dessa volymer bör vara 2 cm3 (D2cc), 1 cm3 (D1cc) och 0,1 cm3 (D0,1cc).
Figur 10. Schematisk bild som visar de mest bestrålade vävnadsvolymerna i anslutning till applikatorn för rektum, sigmoideum och blåsa för 0,1, 1 och 2 cm3 194
 Dosbegränsningar till riskorgan, doser baserade på (EQD2, α/β = 3):
Dosbegränsningar till riskorgan, doser baserade på (EQD2, α/β = 3):
|
|
Dimopoulos, et al. 209 |
EMBRACE II |
|
Blåsa |
D2cc < 90 Gy |
D2cc < 90 Gy |
|
Rektum |
D2cc < 70–75 Gy |
D2cc < 75 Gy |
|
Sigmoideum |
D2cc < 70–75 Gy |
D2cc < 75 Gy |
Om intrauterin brachyterapi inte kan ges (cervixstenos, tumörutbredning där intrauterin brachyterapi inte är möjlig) övervägs i första hand interstitiell brachyterapi (enbart vaginalapplikator och interstitiella nålar, alternativt enbart interstitiella nålar) eller i andra hand fortsätts behandlingen med adaptivt krympande EBRT-boost med måldos 80 Gy (EQD2) mot HR-CTVBT 210 med beaktande av dos till OAR. Vid fortsatt extern boost rekommenderas ny MRT, ny dosplanerings-DT och omplanering. Fall för interstitiell boost utan samtidig intrauterin brachyterapi är en högspecialiserad verksamhet; se vidare kapitel 17 Underlag för nivåstrukturering.
Resurser för IGART
Dosplanerings-DT (EBRT), diagnostisk MRT x 2 (innan behandlingsstart och strax innan brachyterapi), dosplanerings-MRT (BT) samt PET-DT-diagnostik.
Övergång från standarddosplaner baserade på punktdoser till volymbaserad intrakavitär brachyterapi är svår och resurskrävande, och innefattar en betydande inlärningskurva. Intrakavitär volymbaserad brachyterapi bör initieras efter en period där ett dedikerat brachyteam lär sig principerna för targetritning, applikatorrekonstruktion och dosoptimering i dosplaneringssystemet 172194. Brachyverksamheten bör kunna genomföras hela året, även semestertid.
Kompetenskrav
Enligt GEC-ESTRO: Minst två gynonkologer/brachyterapeuter och två sjukhusfysiker med erfarenhet av 3D-brachydosplanering för livmoderhalscancer, minst 10 behandlingar/terapeut och år, minst 15 patienter per centrum och år 172. Det är nödvändigt med ett multidisciplinärt team som innefattar brachyterapeuter, sjukhusfysiker, bilddiagnostiker, onkologisjuksköterskor och assisterande personal.
Protonterapi
Vid definitiv kombinerad cytostatika- och strålbehandling av livmoderhalscancer ges optimalt en kombination av extern strålbehandling och brachyterapi för att ge en så effektiv och riktad behandling som möjligt. Ett mål med behandlingen är också att minimera risken för seneffekter från urinblåsa, tarm och vagina, genom att undvika höga stråldoser till dessa organ. I framtiden är det möjligt att protonterapi på Skandionkliniken i Uppsala i vissa fall kan ersätta fotoner för att minska stråldosen till riskorganen (inom studieprotokoll) med mindre seneffekter än med konventionell strålbehandling med fotoner. Även andra möjliga indikationer för protonterapi kan förutses i framtiden, t.ex. som boost mot den centrala tumören då brachyterapi inte kan ges av tekniska eller anatomiska skäl, vid rebestrålning eller vid metastasering till paraaortala lymfkörtlar. Skandionkliniken har börjat ta emot patienter september 2015, men ännu inte patienter med gynekologisk cancer.
Faktorer som påverkar resultatet vid strålbehandling
Total behandlingstid, OTT
Flera retrospektiva studier har visat att den totala behandlingstidens längd är av betydelse för att uppnå lokal kontroll vid kurativt syftande strålbehandling av livmoderhalscancer. I den största retrospektiva analysen inkluderande 1 227 patienter med stadium IB–III som erhöll minst 70 Gy till punkten A, konstaterar man en minskad lokal kontroll om cirka 0,6–0,9 % per dags förlängd behandling över 7 veckor 211. Man konstaterar en tydlig skillnad med avseende på lokalt återfall inom 10 år för respektive stadium mellan patienter som avslutat all behandling inom 7 veckor, mellan 7 och 9 veckor, respektive efter 9 veckor (7 %, 22 % resp. 36 % för stadium IB; 14 %, 27 % resp. 36 % för stadium IIA; 20 %, 28 % resp. 34 % för stadium IIB samt 30 %, 40 % resp. 50 % för stadium III).
I en retrospektiv analys av 830 patienter med invasiv livmoderhalscancer, som erhållit kurativt syftande strålbehandling ≥ 75 Gy till punkten A (EBRT + BT), fann man en minskad lokal kontroll på cirka 1 % per dags förlängd behandling över 30 kalenderdagar 212. Vanligast var avbrott för helgdagar (förutom lördag–söndag), uppehåll mellan EBRT och BT, samt för apparatservice.
I en annan studie med 837 patienter som erhållit ≥ 65 Gy till punkten A hade de lokala återfallen efter 4 år ökat från 5 % till 20 % när den totala behandlingstiden gick från < 6 veckor till > 10 veckor 213. I de båda senare studierna var effekten tydligast vid stadium III.
I en översiktsartikel från 2007 belyser Bese och medarbetare effekterna av oplanerade uppehåll under pågående strålbehandling för olika maligna diagnoser och konstaterar att en förlängd behandlingstid generellt minskar sannolikheten för lokal kontroll med 0,3–1,6 % per dags förlängd behandling vid livmoderhalscancer. Man betonar dock att studiernas behandlingslängd varierar från 6 till 9 veckor varför siffrorna är något svårvärderade 214.
Oplanerade uppehåll i strålbehandlingen bör så långt som möjligt undvikas. Det är viktigt att både patienter, närstående och behandlingsteam är införstådda med detta och att man ger understödjande behandling vid nedsatt allmäntillstånd. Oundvikliga avbrott i planerad behandling och helgdagar kompenseras. Bäst är att behålla den totala behandlingstiden, den totala dosen och dosen per fraktion genom att behandla lördag eller annan helgdag alternativt ge två behandlingar på fredagar (tidiga avbrott) eller två behandlingar samma dag oavsett veckodag (sena avbrott), båda med tidsintervallet ≥ 6 timmar mellan fraktionerna 214. Vid SIB kan inte dubbelfraktionering ges. En intensifiering av behandlingen mot slutet av strålbehandlingen kan anses ge minst risk för ökade komplikationer i normalvävnad. Då har normalvävnadens kompensatoriska reparationsmekanismer hunnit komma i gång och därmed minskas risken för både akuta och sena effekter 188215.
Det sämsta alternativet för att kompensera för utebliven behandling är att ge några extra fraktioner på slutet eftersom detta förlänger OTT och ökar risken för minskad tumörkontroll. Se vidare bilaga 5.
Väntetid till start av strålbehandling
Tiden från behandlingsbeslut till start av strålbehandling har sannolikt stor betydelse för prognosen, extrapolerat från studier av huvud-halscancer som har en likartad tumörbiologi. Vid i median 4 veckors väntetid från behandlingsbeslut till behandlingsstart sågs i en dansk studie av huvud-halscancer en signifikant tumörprogress 216. Liknande resultat avseende väntetid till start av strålbehandling har även setts vid andra tumörsjukdomar 217 men har inte studerats specifikt för livmoderhalscancer. Förberedelser (bildunderlag, targetritning, dosplanering etc.) medför oundviklig tidsåtgång från beslut till behandlingsstart. Både av prognostiska och psykologiska skäl bör dock tiden till behandlingsstart minimeras. I enlighet med SVF bör strålbehandling påbörjas inom 32 dagar från välgrundad misstanke.
Anemi
Flera studier har visat att patienter med anemi har en sämre prognos vid kurativt syftande kombinerad cytostatika- och strålbehandling 218219, beroende på hypoxi och därmed minskad radiosensitivitet. I ett norskt material från 1940-talet kunde författarna visa att ett lågt hemoglobinvärde (< 110 g/L) innan behandlingsstart var prognostiskt ogynnsamt 220. Dock finns det endast en randomiserad studie från 1980-talet i vilken patienterna i behandlingsarmen transfunderades till en Hb-nivå över 120 g/L under pågående strålbehandling. Studien visade på en ökad lokal kontroll för den transfunderade gruppen, men avslutades i förtid och kritiserades för att inte ta hänsyn till bl.a. stadium eller tumörstorlek 221.
Ett flertal retrospektiva studier har visat att låga Hb-värden (< 120 g/L resp. < 110 g/L) under pågående kombinerad cytostatika- och strålbehandling förefaller vara en oberoende och starkare prognostisk faktor för lokal kontroll och total överlevnad än Hb inför behandlingsstart 218219222. I studierna förefaller blodtransfusioner öka sannolikheten för lokal kontroll och total överlevnad hos de patienter vars Hb-värden kan hållas normala under pågående strålbehandling. Små randomiserade studier med erytropoietin under pågående kombinerad cytostatika- och strålbehandling har visat på en positiv effekt på Hb, men studierna har varit för små för att kunna visa skillnader i lokal kontroll eller total överlevnad. En metaanalys har även visat på en diskret ökning av tromboemboliska händelser vid användandet av erytropoietin 223224. Transfusion rekommenderas därför till Hb-nivå ≥ 120 g/L.
Rökning
Det finns endast få studier på livmoderhalscancer och effekten av rökning under pågående strålbehandling. Mayadev och medarbetare visade i en retrospektiv studie på 96 patienter med lokalt avancerad livmoderhalscancer som behandlades med definitiv kombinerad cytostatika- och strålbehandling att graden av rökning omräknat till paketår (pack years) var av signifikant betydelse för lokoregional kontroll, sjukdomsfri och total överlevnad jämfört med icke-rökare 225. Det finns flera studier på andra tumörsjukdomar såsom huvud-halscancer, lungcancer och prostatacancer som också visar på försämrad lokal kontroll och/eller total överlevnad relaterat till rökning under pågående strålbehandling 226227. Mekanismen antas bero på hypoxi och därmed minskad radiosensitivitet.
I en prospektiv studie av Hoff och medarbetare inkluderande 232 patienter med huvud-halscancer konstaterade författarna att rökare hade ett sämre resultat jämfört med icke-rökare med avseende på lokal kontroll (44 % mot 66 %), sjukdomsspecifik överlevnad (56 % mot 77 %) och total överlevnad (39 % mot 66 %) 226. Författarna konstaterade också att graden av rökning omräknat som paketår (”pack years”) var av betydelse för utfallet. Dessa data stämmer överens med tidigare retrospektiva analyser, där man konstaterar en 5-årsöverlevnad på 23 % respektive 55 % för gruppen rökare jämfört med gruppen icke-rökare.
Vidare har studier visat att andelen sena komplikationer av ≥ grad 3 är signifikant högre hos gruppen rökare jämfört med icke-rökare (49 % resp. 31 %) 228. EBRT vid prostatacancer leder till 2–5 ggr ökad risk för gastrointestinala seneffekter inklusive anal inkontinens hos rökare jämfört med icke-rökare 229, vilket kan antas motsvarar förhållandena vid livmoderhalscancer. Se vidare avsnitt 13.15 Råd vid övriga fysiska biverkningar efter livmoderhalscancer.
Organrörelser
Den tekniska utvecklingen inom den externa strålbehandlingen har medfört möjlighet att öka strålbehandlingsdosen till tumören och minska strålningen till riskorganen (OAR). Detta förbättrar möjligheten till bot och minskar risken för behandlingsrelaterade komplikationer och seneffekter. Tidigare användes standardiserade bäckenfält där strålbehandlingen levererades med visserligen 3D-konform fyrfältsteknik men som gav full stråldos till hela bäckenvolymen inkluderande såväl tumör och lymfkörtlar som OAR. I dag används huvudsakligen IMRT (intensitetsmodulerad strålbehandling) eller VMAT (Volumetric Modulated Arc Therapy, RapidArc) vid EBRT till livmoderhalscancer. Detta ställer högre krav på targetdefinition, vilket i sin tur ställer högre krav på bilddiagnostik och medför en betydligt ökad tidsåtgång för strålplanering och behandling, inklusive kvalitetskontroll.
En utmaning i denna skräddarsydda behandling är att uppnå adekvat stråldos i target och minimal stråldos till OAR. Det finns en betydande organrörlighet mellan fraktioner som leder till varierande dosfördelning till target och OAR. Uterus och cervix läge och form påverkas av blås- och tarmfyllnad. Tumörkrympning medför också att targetvolymen ändras. På grund av tätare blås- och tarmtömningar under behandlingens gång minskar ofta organrörligheten samtidigt som en systematiskt minskande blåsvolym försvårar att behålla en konstant blåsvolym 230231.
Ett flertal studier har genomförts för att standardisera blåsfyllnaden (miktionsscheman, dryckesinstruktioner), med begränsad effekt 231. I EMBRACE föreslås ett standardiserat förfarande: Patienten uppmanas tömma blåsan och får sedan dricka 125 ml. Efter 1 timme görs DT/ges behandling (www.embracestudy.dk).
Diametern på rektum vid DT/behandling bör understiga 4 cm för att minska risken för att target hamnar utanför strålfältet 232. Rutin för bedömning av detta och åtgärder (mikrolavemang, ”pip”) vid bilddiagnostik inför targetdefinition och behandling rekommenderas.
Figur 11.
Övre bild, vänster: Uterus läge (röd) vid blåsfyllnad 550 ml (blå).
Övre bild, höger: Vaginas läge (turkos) vid utspänd rektum (brun).
Nedre bild, vänster: Uterus läge vid blåsfyllnad 75 ml 230.
Nedre bild, höger: Vaginas läge vid liten rektumvolym.

Ett sätt att kompensera för osäkerhet avseende organrörelser är att inkludera generösa marginaler, men därmed förloras möjligheten att minska stråldosen till OAR.
Ett annat sätt att ha kontroll över detta är att göra omplanering en gång per vecka 233, men detta är resurskrävande och leder inte till kontroll över dagliga variationer. En annan möjlighet är att använda individualiserade strategier med flera strålplaner för varje patient, och använda den mest optimala planen vid varje behandlingstillfälle (”plan-of-the-day”) 234235236237238. Vår rekommendation är att organrörelser minimeras genom noggrann kontroll av standardiserad blås- och rektumfyllnad enligt lokala rutiner. Individualiserade strategier med flera strålplaner bör eftersträvas.
Adaptiv strålbehandling (IGART)
Att anpassa strålbehandlingen med hjälp av bilddiagnostik (image-guided adaptive radiotherapy, IGART) kan även användas för att optimera den externa strålbehandlingen över tid med hänsyn till tumörkrympning, men används huvudsakligen för brachyterapi vid livmoderhalscancer. Då inte brachyterapi kan ges, ges adaptiv central boost med EBRT; se vidare slutet av avsnitt 10.3.1.5 Brachyterapi (BT) och bilaga 5. Individualiserat val av dosplan (”plan-of-the-day”) kan också ses som en form av IGART.
Postoperativ adjuvant behandling
Rekommendationer
Postoperativ radiokemoterapi (kombinerad cytostatika- och strålbehandling) med cisplatin
Indikation:
- Lymfkörtelmetastaser:
- Utökat paraaortalt strålfält bör ges vid lymfkörtelmetastaser paraaortalt eller i nivå med a. iliaca communis.
- Boost till kvarvarande lymfkörtelmetastaser.
- Tumörstorlek ≥ 4 cm.
- Spridning utanför cervix (dvs. till parametrier).
- Småcellig neuroendokrin histologi.
- Kirurgiska marginaler < 5 mm i vagina.
- Individuell bedömning vid övriga snäva kirurgiska marginaler där djupväxt i cervix, LVSI, tumörstorlek, histologi och eventuell förekomst av ITC vägs in.
Ordination:
- Extern strålbehandling bör ges till en dos av minst 45 Gy (EQD2).
- Vid snäva resektionsränder/stor tumörstorlek övervägs boost med HDR-BT med vaginalapplikator till kraniella 1/3-delen av vagina. Exempelvis 10 Gy, uppdelat på 2–3 fraktioner, doserat 5 mm från applikatorytan.
- Cisplatin bör ges i dosen 40 mg/m2 (maxdos 70 mg) q1w under strålbehandlingstiden, optimalt 5 cykler.
Postoperativ cytostatikabehandling
Indikation:
- Småcellig neuroendokrin histologi.
Ordination:
- Cisplatin 75–100 mg/m2 dag 1 + etoposid 100 mg/m2 dag 1–3, q3w, 3 cykler*.
* Om ej givet neoadjuvant (NACT).
Bakgrund/indikation
Postoperativ adjuvant behandling har i flera studier visats signifikant minska risken för lokal- och fjärråterfall vid tidig livmoderhalscancer med riskfaktorer. Lymfkörtelmetastasering 239240 och tumörspridning utanför cervix 123124 är etablerade riskfaktorer för återfall, men för övrigt finns inte någon internationell konsensus vad gäller exakt hur varje enskild riskfaktor ska värderas.
Dubbla behandlingsmodaliteter (kirurgi och strålbehandling) bör i enlighet med vad som anförts tidigare undvikas, p.g.a. ökad risk för sjuklighet. Fördelarna med tillägg av adjuvant behandling avseende prognos gör att detta ändå rekommenderas vid indikationer enligt ovan. Dock understryks vikten av korrekt utredning, för att selektera patienter till om möjligt endast en behandlingsmodalitet. Som regel rekommenderas inte vaginal brachyterapi 154, men kan övervägas vid bristande vaginal radikalitet 241. Se även avsnitt 10.3.1.5 Brachyterapi (BT).
Radiokemoterapi (kombinerad cytostatika- och strålbehandling)
Kombinerad cytostatika- och strålbehandling syftar till att dels öka kvarvarande mikrometastasers känslighet för strålbehandlingen, dels utplåna eventuell subklinisk spridning utanför strålfältet. En Cochraneanalys från 2012 slår fast att det finns måttligt stark evidens för att postoperativ adjuvant platinumbaserad kombinerad cytostatika- och strålbehandling förlänger överlevnaden för kvinnor med livmoderhalscancer i stadium I–IIA med riskfaktorer 242. Tillägg av cisplatinbaserad kombinerad cytostatika- och strålbehandling jämfört med enbart strålbehandling ger en absolut vinst i total överlevnad på 12 % och i progressionsfri överlevnad på 16 %. Risken för akuta biverkningar av grad 3–4 är högre vid kombinerad cytostatika- och strålbehandling än vid enbart strålbehandling 243244, men det finns endast sparsam långtidsuppföljning 245246 och det är inte klarlagt om dessa biverkningar är relevanta på lång sikt.
Även om man inte för varje enskild riskfaktor undersökt nyttan med kombinerad cytostatika- och strålbehandling jämfört med enbart strålbehandling, anses tillägget av cytostatikabehandling vara motiverat. Det baseras på fallen med lymfkörtelspridning, där det klart har visats vara fördelaktigare med kombinerad cytostatika- och strålbehandling.
Lymfkörtlar, tumörstorlek, djupväxt, LVSI och kirurgiska marginaler
Spridning till lymfkörtlar är en av de starkare prognostiska faktorerna efter FIGO-stadium 120. Adjuvant kombinerad cytostatika- och strålbehandling rekommenderas följaktligen vid verifierad spridning till lymfkörtlar samt vid överraskande upptäckt av tumörstorlek på 4 cm eller större 241247. Vid spridning till lymfkörtlar på iliaca communis-nivå eller paraaortalt finns studier som visat att kombinerad cytostatika- och strålbehandling till paraaortalt utökat strålfält med doser upp till 50,4 Gy är genomförbart och inte behäftat med allvarlig toxicitet 248. Kombinerad cytostatika- och strålbehandling med utökat PA-fält bör därför övervägas vid lymfkörtelmetastaser paraaortalt eller i nivå med a. iliaca communis. Se vidare avsnitt 10.3.1.3 Strålbehandling riktad mot paraaortala lymfkörtelstationer (PA-fält).
Graden av tumörinfiltration i cervixstromat samvarierar med lymfovaskulär infiltration (LVSI), men rapporteras trots det i flera studier vara en oberoende prognostisk faktor 138249250. I GOG92-studien fann man att adjuvant strålbehandling signifikant minskade risken för återfall för patienter med lymfkörtelnegativ livmoderhalscancer i stadium IB och minst två av följande tre riskfaktorer: stromainfiltration > 2/3, LVSI och tumörstorlek på minst 4 cm 154. I långtidsuppföljningen av samma studie fann man vid subgruppsanalys fortfarande signifikant minskad återfallsrisk för patienter med riskfaktorskombinationen djup stromainfiltration, LVSI och tumörstorlek över 4 cm, medan nyttan av adjuvant behandling inte kunde påvisas för övriga prognostiska subgrupper 241. Patienterna i GOG92 utreddes och behandlades på 1980- och 1990-talen vilket man måste beakta när man värderar resultaten och riskgrupperingarna. Nyligen publicerade data från en retrospektiv genomgång av 294 adjuvant behandlade patienter i stadium IA2–IIA stödjer resonemanget att en kombination av riskfaktorer bör värderas redan före eventuell kirurgi i syfte att minska risken för adjuvant behandling och i stället erbjuda definitiv strålbehandling 251.
Vad gäller LVSI är även detta associerat till risk för lymfkörtelspridning 252. De studier som rapporterat LVSI som riskfaktor har dock använt olika metoder för hur LVSI har analyserats, vilket kan vara en del av förklaringen till de skiftande resultat av dess prognostiska betydelse som presenterats 141.
Sammantaget bedöms varken stromainfiltration eller LVSI vara tillräckligt starka prognostiska faktorer, ensamt eller i kombination, för att kvalificera patienter till adjuvant behandling. Det är emellertid önskvärt att dessa faktorer anges i PAD-utlåtanden, för en sammantagen riskbedömning inför att man tar ställning till eventuell adjuvant behandling. Dessa fall bör diskuteras på MDK.
Snäva kirurgiska marginaler är associerat till sämre överlevnad, liksom tumörväxt utanför cervix i parametrier. Gränsen för vad som ska betraktas som snäva kirurgiska marginaler varierar mellan olika studier 152153. I internationella rekommendationer tar man sällan ställning till om det finns en specifik gräns för när adjuvant behandling bör rekommenderas. I avsaknad av tillräcklig evidens bedömer vi att åtminstone 5 mm kirurgisk marginal i vagina bör uppnås. Övriga marginaler får bedömas tillsammans med övriga riskfaktorer (LVSI, djupväxt, tumörstorlek och histologi). Parametrieväxt utgör indikation för adjuvant behandling.
Högmalign histologi
Neuroendokrin småcellig cancer (NEC) är en högmalign tumör där det föreligger stor risk för återfall 253. Adjuvant kombinerad cytostatika- och strålbehandling rekommenderas därför trots avsaknad av randomiserade studier på denna histologiska undergrupp. Kombinationscytostatika (cisplatin + etoposid) rekommenderas alltid, antingen neoadjuvant eller adjuvant i operabla stadier, eller i kombination med strålbehandling vid definitiv kombinerad cytostatika- och strålbehandling, se vidare avsnitt 10.7 Neuroendokrin livmoderhalscancer (NEC).
För glassy cell carcinoma (GCC) anges i litteratursammanställningar en något lägre 5-årsöverlevnad jämfört med livmoderhalscancer generellt 254255. Det finns inte tillräckligt med evidens för att rekommendera adjuvant behandling enbart baserat på histologi vid GCC.
Targetdefinition
Dosplanering ska göras på underlag från DT eller MRT. Dosplanerings-DT utförs i behandlingsposition från diafragma till nedom tuber ischiadicum, i max 3 mm tjocka snitt. Intravenöst kontrastmedel underlättar definition av target och OAR om DT används som enda planeringsmetod. Om MRT för dosplanering finns som tillgänglig metod utförs även denna i behandlingsposition. Diagnostisk MRT-undersökning kan fusioneras med DT i dosplaneringsprogrammet, men det kräver noggrant överensstämmande undersökningsprotokoll med samma planvinklar och snitt-tjocklek i behandlingsläge. Om MRT används som dosplaneringsunderlag avstår man från i.v. kontrastmedel vid DT. Bilddiagnostikunderlagen sparas om möjligt i lokalt PACS.
Ett internationellt konsensus-dokument har utarbetats som vägledning vid planering av adjuvant strålbehandling för livmoderhalscancer 176.
Övre begränsning av CTV_N (nodes) bör vara 7 mm under L4–L5-disken och nedre begränsning av CTV_N bör vara 3 cm nedom vaginaltoppen eller 1 cm ovan foramen obturatorius nedre gräns, vilket som är mest kaudalt. Vid utökat paraaortalt strålfält är övre begränsningen i nivå med njurkärlen. CTVN får i medellinjen aldrig vara mindre än 1,5 cm i anterior – posterior riktning. Marginaler från CTV_N till PTV_N skapas utifrån lokala förutsättningar.
Följande strukturer bör inkluderas i CTV:
- Lymfkörtelstationer vid iliaca communis, iliaca externa, iliaca interna samt presakralt. Vid utökat PA-strålfält inkluderas även paraaortala lymfkörtelstationer upp till avgång för njurkärlen.
- Eventuella lymfocelen.
- Vaginas övre 3 cm samt paravaginal mjukvävnad lateralt om vagina.
För detaljer, se avsnitt 10.3.1.2 Targetdefinition EBRT och bilaga 4.
Ev. kvarlämnade lymfkörtelmetastaser behöver stråldoser (boost) i nivå med vad som gäller vid primär definitiv kombinerad cytostatika- och strålbehandling; se avsnitt 10.3.1 Definitiv kombinerad cytostatika- och strålbehandling och bilaga 5.
Postoperativ adjuvant brachyterapi: Vid snäva marginaler i vaginaltoppen kan HDR-BT övervägas till kraniella 1/3-delen av vagina, förslagsvis 10 Gy/2–3 fraktioner, doserat 5 mm från applikatorytan, i kombination med EBRT.
Spridd sjukdom, fjärrmetastaser, cytostatikabehandling vid återfall
Rekommendationer
Individuell behandling:
- Cisplatin 50 mg/m2 + paklitaxel 175 mg/m2, q3w i första hand
- Cisplatin 50 mg/m2 dag 1 + topotekan 0,75 mg/m2 dag 1–3, q3w i andra hand
- Ställningstagande till tillägg av pembrolizumab 200 mg q3w till platinuminnehållande cytostatikabehandling ± bevacizumab i upp till 35 cykler för patienter med PD-L1 ≥ 1 enligt ”combined positive score” (CPS) metoden. Vid underhållsbehandling med singel pembrolizumab kan dosen 400 mg q6w övervägas.
- Cisplatin 50 mg/m2 karboplatin AUC 5 vid nedsatt allmäntillstånd, q3–4w
- Topotekan 0,75 mg/m2 dag 1–3 + paklitaxel 175 mg/m2 q3w vid allergi mot cisplatin eller vid påtagligt nedsatt njurfunktion
- ·Vid progress efter platinumbaserad behandling enligt ovan hos patient som ej erhållit pembrolizumab kan singel cemiplimab 350 mg dag 1 q3w upp till 96 veckor vara ett alternativ
- Paklitaxel 80 mg/m2 vid platinumresistens, q1w
- Ställningstagande till strålbehandling
- Ställningstagande till individuellt anpassad kirurgi
Vid primärt spridd sjukdom (fjärrmetastaser, dvs. stadium IVB) bör tumörutbredningen styra den primära behandlingen. Om det finns en symtomgivande lokal tumör med begränsad fjärrspridning ges primärt strålbehandling i syfte att uppnå lokal kontroll, eventuellt i kombination med konkomitant cisplatin. Generellt rekommenderas då sedvanligt behandlingsupplägg i enlighet med avsnitt 10.3.1, men detta kan behöva modifieras utifrån individuella förutsättningar, där accelererad och begränsad strålbehandling i syfte att uppnå lokal kontroll kan förordas (t.ex. 3 Gy x 10–13 mot central tumör enbart), för att därefter övergå till övrig palliativ behandling. Därefter ges cytostatikabehandling i palliativt syfte. Om fjärrmetastaseringen är omfattande rekommenderas primär cytostatikabehandling, för senare ställningstagande till eventuell strålbehandling mot cervix för lokal kontroll och i symtomlindrande syfte. Se även kapitel 15 Behandling av återfall.
Vid bäckenåterfall efter primärkirurgi där strålbehandling inte tidigare givits övervägs i första hand kurativt syftande kombinerad cytostatika- och strålbehandling. Vid isolerat bäckenåterfall efter definitiv kombinerad cytostatika- och strålbehandling övervägs kirurgi. Se kapitel 15 Behandling av återfal.
Vid återfall där inte kirurgi eller strålbehandling är möjlig bör man överväga cytostatikabehandling. Vid bäckenåterfall, tidigare given cytostatikabehandling (konkomitant kombinerad cytostatika- och strålbehandling), återfall inom tidigare strålbehandlat område eller kort tid (< 1 år) sedan primärbehandling, uppnås sämre respons än om dessa omständigheter inte föreligger 256. Vid tidigare cisplatinbehandling konkomitant bör man överväga kombinationscytostatika vid återfallsbehandling.
Förstahandspreparatet är cisplatin, där äldre studier visat en respons på upp till 38 %, med OS 7 månader, vid dosen 50 mg/m2 givet var 3:e vecka 257. Olika doser och dosintensitet har studerats med liknande resultat. Andra preparat har provats som singeldroger, med sämre respons alternativt oacceptabla biverkningar.
Kombinationsbehandlingar har studerats, där man i GOG 169 jämfört cisplatin 50 mg/m2 med cisplatin 50 mg/m2 + paklitaxel 135 mg/m2 24-timmarsinfusion, med respons 19 % vs. 36 %, PFS 2,8 månader vs. 4,8 månader (signifikant skillnad), men OS 8,8 månader vs. 9,7 månader (ej signifikant) 258. I GOG 179 jämfördes cisplatin 50 mg/m2 med cisplatin 50 mg/m2 + topotekan 0,75 mg/m2 (3 dagar) med respons 13 % vs. 27 %, PFS 2,9 månader vs. 4,6 månader (signifikant skillnad) och OS 8,6 månader vs. 9,4 månader (signifikant skillnad) 259. Dessa studier har dock kritiserats p.g.a. jämförelsevis sämre respons i både kontrollarmen och experimentarmen jämfört med andra GOG-studier (i median 12 månader OS).
I den uppföljande studien GOG 204, som avbröts i förtid, jämfördes fyra kombinationsbehandlingar (cisplatin 50 mg/m2 + paklitaxel/vinorelbin/gemcitabin/topotekan) där man inte såg några signifikanta skillnader mellan de fyra olika armarna, men en trend mot bäst effekt för kombinationen cisplatin + paklitaxel med PFS 8,7 månader och OS 12,9 månader och med bäst biverkansprofil. Kombinationen cisplatin + paklitaxel q3w är därför den rekommenderade standardbehandlingen 260, men även cisplatin och topotekan kan övervägas, speciellt vid besvärande neuropati efter tidigare behandling. Av tradition och extrapolerat från andra studier ges i Sverige paklitaxel i dosen 175 mg/m2 på 3 timmar, och inte paklitaxel 135 mg/m2 24-timmarsinfusion.
I en studie har föreställningen att cisplatin är överlägset karboplatin utmanats 261 och man såg här jämförbar effekt mellan de två preparaten (i kombination med paklitaxel). Dock framhålls att patienter som inte tidigare erhållit platinumpreparat bör rekommenderas cisplatin i första hand.
I studien GOG 240 har man studerat cisplatin + paklitaxel respektive topotekan + paklitaxel med eller utan tillägg av bevacizumab. Data talar för en förbättrad OS (16,8 månader vs. 13,3 månader) vid tillägg av bevacizumab till cisplatin + paklitaxel i utvalda fall (vid låg risk för perforationer och andra allvarliga komplikationer) 262. I selekterade fall rekommenderas därför tillägg av bevacizumab. Studien har dock kritiserats p.g.a. osedvanligt god effekt i kontrollarmen, där frågor kring inklusion och kostnadseffektivitet har framförts 263264. I studien avslutades behandlingen vid endera tumörprogress, komplett respons eller svåra biverkningar. Frågan om fortsatt bevacizumab till patienter med kvarvarande tumör men där cytostatikabehandling avslutats p.g.a. biverkningar, är inte studerad. Vid allergi mot cisplatin eller vid kraftigt nedsatt njurfunktion kan paklitaxel + topotekan vara ett alternativ. Denna regim uppvisade endast marginellt sämre tumörrespons i GOG 240 jämfört med den rekommenderade cytostatikaregimen cisplatin och paklitaxel (47 % jämfört med 50 %). Samma övervägande avseende tillägg av bevacizumab gäller för båda regimerna.
Vid påverkat allmäntillstånd bör kombinationsbehandling undvikas och singelbehandling med cisplatin eller karboplatin övervägas som alternativ. Det finns klinisk erfarenhet av behandling med paklitaxel 80 mg/m2 veckovis, med god respons även inom tidigare strålbehandlat område, men denna behandling har bristande dokumenterad evidens.
Under 2021 presenterades två randomiserade fas III-studier som jämförde effekten av immunterapi mot kemoterapi på patienter med spridd livmoderhalscancer eller med canceråterfall. I Empower cervical-1-studien lottades 608 patienter som tidigare erhållit minst en kemoterapibehandling till behandling med checkpointhämmaren cemiplimab eller till standard kemoterapibehandling. Resultaten visare att fler patienter i snitt svarar på behandling med cemiplimab jämfört med kemoterapi, 16,4 % mot 6,3 %, och att dessa patienter lever i snitt 3,5 månader längre (12 månader mot 8,5 månader) 265. I Keynote 826-studien lottades 617 patienter som inte fått någon tidigare kemoterapibehandling till behandling med paklitaxel, platinumpreparat, med eller utan bevacizumab, och med tillägg av studieläkemedlet pembrolizumab 200 mg eller placebo var tredje vecka till progress eller som mest i 35 cykler. De patienter som hade ett ökat uttryck av PD-L1 proteinet på tumör- och immunceller (ca 89% av samtliga patienter) och som erhöll kombinationsbehandling med pembrolizumab hade i snitt bättre effekt av behandling än de som fick placebo både sett till antalet som svarade på behandlingen, 68,1 % mot 50,2 %, och sett till överlevnad där 53 % av patienterna var vid liv i försöksarmen jämfört med 41,7 % i kontrollarmen vid 24 månader 114.
Graden allvarliga biverkningar (≥ grad 3) för checkpointhämmare jämfört med kemoterapi var 45 % mot 53,4 % i Empowerstudien och 68,4 % mot 64,1 % i Keynotestudien. Graden av allvarliga immunmedierade biverkningar var 5,3 % i Empowerstudien med inflammation i sköldkörtel, lever och lungor som vanligaste biverkningar och 11,4 % i Keynotestudien med inflammation i hud, sköldkörtel och tjocktarm som vanligaste biverkningar. Keynote 826-studien godkändes av European Medicines Agency (EMA) i maj 2022 och är ett behandlingsalternativ för vissa patienter med spridd sjukdom eller återfall i sjukdom som tidigare inte fått någon kemoterapibehandling utöver eventuell cisplatinbehandling vid strålbehandling. Behandling med cemiplimab enligt Empower-studien godkändes i Sverige i december 2022 och kan vara ett alternativ för patienter med tumörprogress efter första linjens platinumbaserade recidivbehandling men som inte tidigare erhållit behandling med checkpointhämmare. Behandling gavs i studien oavsett PDL1-status men vårdprogramsgruppen ser gärna att man för framtida bruk analyserar PDL1-status hos patienter som behandlas med immunterapi.
Ytterligare nya målriktade läkemedel testas nu i kliniska studier på livmoderhalscancer. I en fas II-studie har preparatet tisotumabvedotin, som kopplar samman en antikropp mot ett ytprotein på livmoderhalscancerceller med ett cytotoxiskt läkemedel, testats på 34 patienter med visad effekt hos 9 patienter 266. En mer omfattande studie pågår och ytterligare studier planeras. Därutöver pågår tester med ett terapeutiskt vaccin ADXS11-01 som aktiverar immunförsvaret mot HPV-infekterade celler. En fas II-studie med 109 patienter med avancerad livmoderhalscancer där vaccinet gavs som singelbehandling eller i kombination med cisplatin har visat på en effekt hos 17,1 % respektive 14,7 % av patienterna med studierelaterade biverkningar hos 16,2 % 267. Ytterligare preparat som prövas inom ramen för kliniska studier är PARP-hämmare och andra former av immunterapi såsom aktiverade T-celler 268. Det är viktigt att påpeka att inga av dessa immunmodulerande behandlingar ges idag utanför kliniska studier och det är ännu för tidigt att säga om några av dessa behandlingar kommer att vara aktuella i kliniken i framtiden.
NACT innan strålbehandling
Ett flertal små äldre icke-randomiserade studier med kort uppföljningstid har publicerats i vilka man inte har kunnat påvisa någon nytta med NACT innan strålbehandling. En metaanalys publicerades 2004 i vilken författarna konstaterade att de inkluderade studierna är alltför heterogena för att några säkra slutsatserna ska kunna dras 271. 2013 publicerades en enkelarmad prospektiv studie (n = 46) som visade på god effekt av kombinationen veckovis karboplatin AUC 2 + paklitaxel 80 mg/m2 i sex veckor innan strålbehandling, med en komplett eller partiell respons hos 70 % av patienterna utan att den efterföljande kombinerade cytostatika- och strålbehandlingen påverkades negativt 272. Resultaten har föranlett en randomiserad fas III-studie (INTERLACE) för patienter med FIGO 2009 stadium IB2–IVA (n = 500) i vilken man jämför kombinerad cytostatika- och strålbehandling med NACT efterföljt av kombinerad cytostatika- och strålbehandling. Studien har inkluderat 381 patienter och beräknas stänga våren 2020, med ett sannolikt första preliminärt resultat 2022 (personlig e-post från huvudprövare Dr Mary McCormack, 9 juni 2019).
Neuroendokrin livmoderhalscancer (NEC)
Rekommendationer
- Randomiserade, kontrollerade studier saknas som underlag för behandlings-rekommendationer vid neuroendokrin småcellig livmoderhalscancer (NEC). Det finns bara små observationsstudier av låg evidensstyrka med osäkra skattningar (⊕)–(⊕⊕).
- NEC är en högmalign tumörtyp. Snabb remiss för eftergranskning av PAD av referenspatolog med kompletterande immunhistokemisk diagnostik är central.
- PET-DT rekommenderas i primärdiagnostik p.g.a. hög metastaseringstendens (⊕⊕).
- NEC behandlas bäst med multimodal behandlingsstrategi med kirurgi, kombinationscytostatika med etoposid/cisplatin (EP) + tillägg av strålbehandling (⊕⊕).
- Kirurgi rekommenderas i tidigt stadium IA1–IB2 med resektabel tumör (⊕⊕).
- Radiokemoterapi (kombinerad cytostatika- och strålbehandling) rekommenderas vid stadium ≥ IB3 (⊕⊕).
- Cisplatin/etoposid rekommenderas alltid. Ges neoadjuvant och/eller postoperativt, eller övervägs inom definitiv kombinerad cytostatika- och strålbehandling vid primärtumör > 4 cm eller avancerad sjukdom (⊕⊕).
- Enbart kirurgi och/eller strålbehandling utan cytostatikabehandling rekommenderas inte p.g.a. nedslående behandlingsresultat (⊕⊕).
Figur 12. Behandlingsstrategi vid neuroendokrin småcellig livmoderhalscancer (NEC) (Modifierad efter Gardner 2011) 273
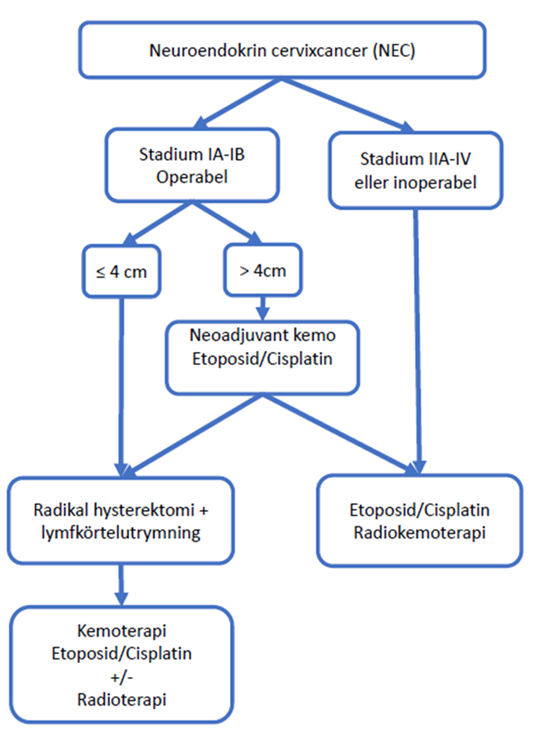
Neuroendokrina tumörer omfattar ett spektrum av olika tumörtyper som härstammar från det diffusa neuroendokrina cellsystemet. Gemensamt är att de uttrycker neuroendokrina markörer, oftast synaptofysin och kromogranin. Man särskiljer två huvudgrupper. Väl differentierade neuroendokrina tumörer (NET), dvs. karcinoid och atypisk karcinoid, förekommer i ovarierna, men är sällsynta i cervix. Lågt differentierad högmalign neuroendokrin cancer (NEC) förekommer primärt i cervix eller corpus uteri. NEC kan förlora uttrycket av synaptofysin eller kromogranin. De allra flesta, upp till 90 %, uttrycker dock neuronspecifikt enolas (NSE) 273274275.
Differentialdiagnostik, klinik och utredning
Neuroendokrin småcellig livmoderhalscancer (SCNEC) är synonym med småcellig livmoderhalscancer, men måste skiljas från lågt differentierad skivepitelcancer med neuroendokrina inslag, samt från andra typer av småcelliga maligna tumörer, som kan uppstå i cervix som:
- basaloid skivepitelcancer
- embryonalt rabdomyosarkom
- lymfom
- odifferentierat karcinom med ursprung i istmus uteri 273274275.
Differentialdiagnostiken bygger på immunhistokemiska färgningar. En sällsynt storcellig variant av neuroendokrin livmoderhalscancer finns (LCNEC) 276277. SCNEC karakteriseras av hög mitosfrekvens, utbredda nekroser, lymfkärlsinvasion och ett starkt samband med HPV 18 278.
SCNEC är nära besläktad med småcellig lungcancer morfologiskt, immunhistokemiskt och kliniskt. Tumörtypen kan förekomma samtidigt med vanlig skivepitelcancer eller adenokarcinom i cervix. Om inte enbart enstaka celler har neuroendokrin differentiering ska tumören klassas som neuroendokrint karcinom, eftersom det är den neuroendokrina komponenten som avgör prognosen, om områden med karakteristiskt växtmönster och mikroskopisk bild ses.
NEC utgör cirka 1 (1–2) % av all livmoderhalscancer 273279. Debutsymtomen är desamma som vid vanlig livmoderhalscancer, men dessutom kan i sällsynta fall kliniska eller biokemiska tecken på ektopisk hormonproduktion förekomma, t.ex. av corticotropin (Cushings syndrom), vasopressin (SIADH, syndrome of inappropriate ADH secretion, ADH = antidiuretiskt hormon (vasopressin)), insulin, serotonin eller parathormon 273274275278.
Diagnos kan ställas med cervixbiopsi, men blir uppenbar ofta först efter konisering eller hysterektomi. Utredning och stadieindelning är i princip densamma som vid vanlig livmoderhalscancer, men risken för tidig lymfkärlsinvasion och tumörspridning är stor. Risken för hematogen spridning till lungor, lever, skelett och hjärna är också klart ökad. Därför rekommenderas PET-DT i den initiala diagnostiken 280. Däremot är inte DT hjärna nödvändig om inte lungmetastaser redan föreligger 281282. Observera att ordinarie FDG-PET avses och inte 5-HTP-PET (används vid t.ex. GI-/pankreas-NEC).
Prognostiska faktorer
Tumörstorlek, stadium, förekomst av och antal lymfkörtelmetastaser samt ren neuroendokrin histologi och rökning är kopplade till prognos 283. Vid tidigt stadium av småcellig livmoderhalscancer är cirka 36 % av patienterna långtidsöverlevare 274275284. Cirka 40 % av patienterna diagnostiseras i stadium I, 20 % i stadium II och cirka 50 % av patienterna har lymfkörtelmetastaser vid diagnos 275279. Vid tidigt stadium behandlat med multimodal kombinationsbehandling har en 3-årsöverlevnad på upp till 80 % rapporterats 275282285, medan 3-årsöverlevnaden vid lokalt avancerad eller spridd sjukdom är mycket låg 281.
Handläggning
Handläggningen av neuroendokrin småcellig livmoderhalscancer influeras delvis av erfarenheterna från behandling av småcellig lungcancer. Kirurgi används för att dels få diagnos, dels behandla tidig begränsad sjukdom. Publicerade data under senare år stöder användning av cisplatinbaserad kombinationscytostatika, särskilt tillsammans med etoposid (EP) vid både småcellig och storcellig NEC. Initial responsrat är hög, 50–79 %, men återfall eller progressiv sjukdom utvecklas ofta 275279281286. Om strålbehandling används, kombineras den oftast med EP-regimen 275282; se avsnitt 10.3.1 Definitiv kombinerad cytostatika- och strålbehandling.
Kirurgi
Radikal hysterektomi med regional lymfkörtelutrymning rekommenderas vid tidigt stadium av NEC med resektabel primärtumör, som del i en multimodal behandlingsstrategi inkluderande cytostatikabehandling och strålbehandling 274275280281284285.
Kombinerad cytostatika- och strålbehandling
Det finns inga prospektiva data som jämför kirurgi med primär kombinerad cytostatika- och strålbehandling vid små resektabla NEC-tumörer. Vid mer avancerad icke-resektabel sjukdom är primär kombinerad cytostatika- och strålbehandling rimlig vid gott allmäntillstånd med samtidig etoposid/cisplatin (etoposid 40 mg/m2 + cisplatin 25 mg/m2/dag, 5 dagar/cykel, q2w, 4 cykler med start 2 veckor före strålbehandling) och brachyterapi. Hoskins rapporterade goda resultat med en sådan regim given vid NEC i stadium IA–IVB, men också mycket hög toxicitet (neutropeni grad 3–4: 70 %; emesis/diarré grad 4: 36 %). Fjärrmetastasering var den vanligaste formen av återfall (28 %) och behandlingsresultatet var korrelerat till initial sjukdomsutbredning 282.
Ett alternativt behandlingsschema kan vara neoadjuvant etoposid/cisplatin 2–3 cykler enligt avsnitt 10.7.6 nedan, efterföljt av kombinerad cytostatika- och strålbehandling (alt. strålbehandling), med beaktande av toxicitet, allmäntillstånd och tumörutbredning.
Cytostatikabehandling
Cytostatikabehandling rekommenderas av många författare. Vid tidigt stadium rekommenderas adjuvant eller neoadjuvant cytostatikabehandling. I första hand rekommenderas cisplatin/etoposid (EP) i enlighet med småcellig lungcancer, dvs. förslagsvis cisplatin 100 mg/m2 dag 1 + etoposid 100 mg/m2 dag 1–3, q3w, men också regimer med cisplatindosen uppdelad på 3–5 dagar, som beskrivs ovan under rubriken kombinerad cytostatika- och strålbehandling.
Hos patienter som fick vinkristin/adriamycin/cyklofosfamid alternerande med etoposid/cisplatin (VAC/EP) rapporteras 68 % 5-årsöverlevnad jämfört med 33 % (p = 0,0078) i gruppen som fick cisplatin/vinblastin/bleomycin (PVB) {Chang, 1998 #514}. Andra författare har rapporterat liknande resultat. De förbättrades inte av strålbehandling 281. I en sammanställning var 3-årsöverlevnaden 83 % efter adjuvant cytostatikabehandling jämfört med 0 % om inte sådan gavs 285.
Vissa författare har föreslagit neoadjuvant cytostatikabehandling, men jämförelser med enbart postoperativ adjuvant cytostatikabehandling saknas 287288.
Strålbehandling
Enbart adjuvant bäckenbestrålning efter kirurgi vid positiva lymfkörtlar eller andra högriskfaktorer visade nedslående resultat i en liten studie av 14 patienter. Alla fick återfall och 12 av 14 rapporterades döda 289. I flera andra studier rapporterades liknande resultat. Endast patienter med små primärtumörer och som fick strålbehandling överlevde 283284. Dessa studier inkluderade inte cytostatikabehandling och stöder inte användning av enbart adjuvant strålbehandling efter kirurgi vid NEC.
Profylaktisk strålbehandling mot hjärnan används vid småcellig lungcancer och har föreslagits även vid NEC. Dock har studier visat en relativt låg frekvens av hjärnmetastaser vid NEC, och de har påvisats bara i närvaro av lungmetastaser, varför profylaktisk hjärnbestrålning endast rekommenderas i denna situation 273281282.
Brachyterapi vid lokalt avancerad sjukdom
I en sammanställning av 621 fall av neuroendokrin livmoderhalscancer stadium II–IVA, hämtade ur National Cancer Database i USA, och behandlade åren 2004–2014, var brachyterapi signifikant associerad med förbättrad överlevnad (OS, p = 0,03). Bara 38 % av dessa patienter genomgick dock brachyterapi, som bedömdes vara underutnyttjad 290.
Behandling vid avancerad sjukdom och återfall
Kombinationscytostatika med etoposid/cisplatin i tillägg till samtidig strålbehandling kan användas vid avancerad sjukdom 282. Stadium var enda prediktiva faktor för sjukdomsfri överlevnad. Treårsöverlevnaden var 80 % vid stadium I–II och 38 % vid stadium III–IV. Patienter med fjärrmetastasering eller återfall kan behandlas med alternerande EP-/VAC-regim (kombinationen vinkristin/doxorubicin/cyklofosfamid) som vid småcellig lungcancer 282291. Även topotekan kan övervägas 292 och karboplatin/paklitaxel 282 vid återfall eller spridd sjukdom. I en icke-randomiserad studie har kombinationen topotekan 0,75 mg/m2 dag 1–3/paklitaxel 175 mg/m2 dag 1 samt bevacizumab 15 mg/kg dag 1, givits var 3:e vecka till 13 patienter med återfall av NEC, med god palliativ effekt, jämfört med en kontrollgrupp med 21 patienter, som fick annan behandling. Man rapporterade progressionsfri medianöverlevnad 7,8 månader i försöksgruppen jämfört med 4 månader i kontrollgruppen (HR 0,21) 293.
I en översiktsartikel från MD Anderson Cancer Center i USA och Spanien, publicerad 2019, presenteras detaljerade behandlingsalgoritmer, som används där, för såväl primärbehandling som vid återfall 294.
Målriktad och immunmodulerande terapi nytt forskningsfält
I en studie av tumörvävnad från 10 patienter med NEC har uttrycket av p16, p53, synaptofysin och kromogranin analyserats med immunhistokemi, och med in situ-hybridisering och polymerase-chain-reaction-uttrycket av högrisk-HPV. Man fann p16 och synaptofysin hos alla 10 tumörer, medan 9 av 10 tumörer var positiva för kromogranin.
HPV 18 påvisades i 6 av 10 och HPV 35 i en tumör. Minst en ”driver mutation” påvisades i 8 av 10 tumörer, varav TP53 somatisk mutation i 4, och 4 olika PIK3CA-mutationer i 3 tumörer. Onkogena ”driver-mutationer”, som KRAS, Erbb2, c-Myc, NOTCH1, BCL6 eller NCOA3, påvisades i 4 av 10 tumörer. Mutationer i ”caretaker”-suppressorer PTEN, RB1, BRCA1, BRCA2 och ARID1B påvisades också i 4 tumörer, som ofta samtidigt hade andra aktiverande mutationer. Dessutom kunde man med ”Next-generation Sequencing” påvisa förändringar i MAPK, PI3K/AKT/mTOR och TP53/BRCA-signalvägarna.
Enligt författarna öppnar det möjligheter till individualiserad, målriktad behandling av NEC 295.
Småcellig neuroendokrin livmoderhalscancer (NEC) visar vissa likheter med en annan virusassocierad cancer, merkelcellscancer. Denna tumör har visat högt uttryck av ”programmed death ligand”, PD-L1, och har behandlats med immunterapi. Därför har man i en färsk studie av 10 fall av NEC analyserat uttrycket av PD-L1, RB1, MLH1, MSH2, MSH6, PMS2, CD3, CD20 och HPV med in situ-hybridisering. PD-L1-uttrycket analyserades i tumörceller samt i lymfocyter. PD-L1-uttryck påvisades i 7 av 10 fall av NEC, medan förlust av MMR-uttryck sågs i en tredjedel av fallen. PD-L1-uttryck i mer än 10 % av tumörcellerna sågs i några av tumörerna med förlorad MMR-uttryck. Dessa patienter bedömdes kunna ha möjlig nytta av immunterapi med ”checkpoint-hämmare” 296.
I en fallbeskrivning rapporteras behandling med PD-1-hämmaren nivolumab av en patient med recidiverande, metastaserad PD-L1-negativ småcellig neuroendokrin livmoderhalscancer. Behandlingen resulterade i komplett respons, som kvarstod 4 månader efter utsättning p.g.a. biverkningar. Författarna konkluderar att immunterapi vid NEC har visats ha kapacitet att påverka den underliggande orsaken, högrisk-HPV, på sådant sätt att klinisk effekt kan uppnås, men att mer forskning behövs för att avgöra om HPV-infektion är en prediktiv markör för immun- checkpoint-hämmare 297.
