Behandlingsteknik vid brachyterapi
Behandlingsteknik
Rätt val av applikatorkonfiguration, implantation och bildhantering är grundläggande aspekter för behandlingstekniken [1, 2] . Tredimensionell (3D-) avbildning med MRT eller DT ska användas för dosplanering. Dosplanering med nytt 3D-bildunderlag bör upprepas vid varje fraktion innan behandlingen genomförs, optimalt med MRT inför varje fraktion [1], eller som minimum vid första BT-fraktionen och annars med DT (Nesvacil 2013). I tillägg till det applikatorset som används bör interstitiella nålar användas där så krävs för optimal targettäckning [3].
Vid applikation bör transabdominalt ultraljud användas som guide, detta för att säkerställa att man undviker perforering av uterus. Packning av vagina med tamponad ska göras för att öka avståndet från applikatorn till riskorganen (blåsa och rektum) och för att säkerställa att applikatorn inte kan glida ur läge vid transporten till och från MRT och DT, under MRT- eller DT-undersökningen, överflyttningar och under behandling. Beroende på rekonstruktionsteknik kan det vara lämpligt med blöta tamponader för att lättare visualisera applikatorerna. MR-kompatibla markörer i applikatorn används ibland, beroende på applikatortyp.
Applikatorer
Det finns i dag två stycken applikatorkonfigurationer. De består av en intrauterin applikator (sond) och en vaginalapplikator eller två ovoid-applikatorer sammankopplade till en tandemapplikator. I Sverige används i dag inte ovoider. Om interstitiella nålar används måste ringen vara anpassad för detta.
Figur 1. Tandemapplikator med intrauterin sond och vaginalapplikator, utan och med interstitiella nålar.

3D-bildunderlag
Bildunderlagen för dosplaneringen bör bestå av MRT eller DT. Snittjockleken bör vara 3 mm eller mindre. Bilderna bör orienteras så att de är vinkelräta mot den intrauterina applikatorn. För MRT bör en sekvens med T2-viktade bilder användas. Volymen rekonstrueras parallellt med vaginalapplikatorn. Undersökningen sparas optimalt i PACS. För mer information se Dimopoulos et al. [4].
Targetinritning brachyterapi
Targetinritning görs enligt (GYN) GEC-ESTRO guidelines (se text i huvuddokumentet). Strukturer som ska ritas in är GTV, HR-CTV, IR-CTV, blåsa, rektum, sigmoideum samt optimalt vagina (punktdos) [1].
Doser vid brachyterapi
Doser till target och riskorgan
Slutdosen för brachyterapin, antal BT-fraktioner och dos per fraktion, bestäms utifrån den totala dosen (den radiobiologiska effekten) till tumör och riskorgan (urinblåsa, sigmoideum och rektum) från både extern radioterapi och brachyterapi.
Den totala stråldosen, D90 %, inklusive EBRT, till HR-CTV bör vara > 85 Gy [5]. Brachyterapins del (HDR och PDR) utgörs optimalt av D90 % = 35–40 Gy (EQD2) till HR-CTV. Ett förslag på fraktioneringsschema för HDR-BT kan vara 4 fraktioner, 7 Gy/fraktion. För PDR-BT kan motsvarande antal fraktioner och dos per fraktion räknas fram, se bilaga 2 under dosberäkningar vid brachyterapi. Doser till riskorganen bör rapporteras som den lägsta dosen till de högst bestrålade vävnadsvolymerna i anslutning till applikatorn för rektum, sigmoideum och blåsa för 0,1 cm3, 1 cm3 och 2 cm3 (se figur 3 och tabell 1).
Utförligare rekommendationer för dosberäkning ges under rubriken ”Dosberäkningar vid brachyterapi” (se nedan).
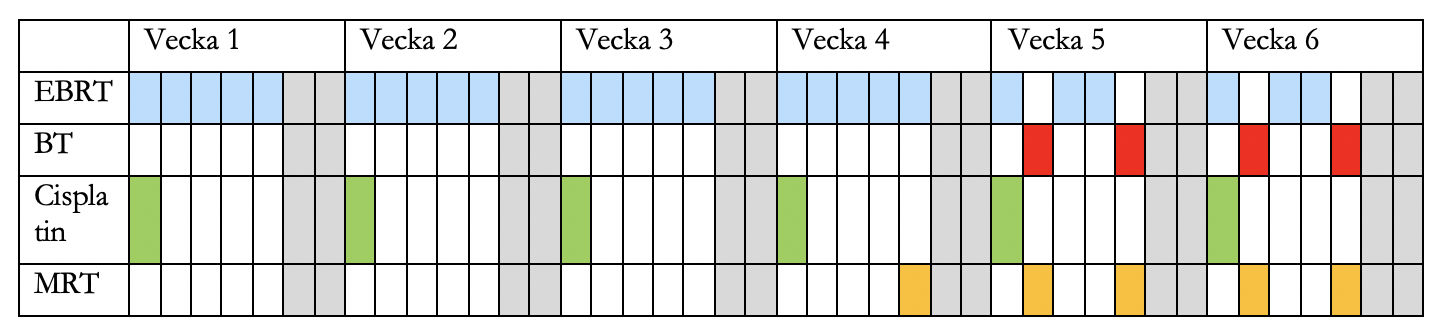
Figur 2 Ex. på flödesschema (modifierat utifrån EMBRACE)
 Tabell 1. Gränser för slutdosen till target och riskorgan. Doserna är beräknade som EQD2 baserat på α/β = 10 (target) och α/β = 3 (riskorgan).
Tabell 1. Gränser för slutdosen till target och riskorgan. Doserna är beräknade som EQD2 baserat på α/β = 10 (target) och α/β = 3 (riskorgan).
|
Volym |
Dosgränser |
Referens |
|
HR-CTV |
D90 % > 85 Gy |
Pötter et al. (5) |
|
Blåsa |
D2 cm3 < 90 Gy |
Pötter et al. (5) |
|
Rektum |
D2 cm3 < 70-75Gy |
Pötter et al. (5) |
|
Sigmoideum |
D2 cm3 < 70-75Gy |
Pötter et al. (5) |
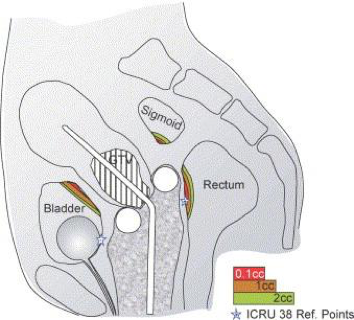
Figur 3. Schematisk bild som visar de mest bestrålade vävnadsvolymerna i anslutning till applikatorn för rektum, sigmoideum och blåsa för 0,1, 1 och 2 cm3 (6)
Dosplanering
Dosoptimering vid brachyterapi
Vid varje fraktion görs en individuell dosplanering utifrån i bildunderlaget beskrivna targetvolymer och riskorgansvolymer och dessa volymers stråldosbegränsningar. Rekonstruktionen av applikatorerna bör om möjligt göras i samma bildunderlag som targetvolymen och riskorganen är beskrivna i. Detta för att undvika osäkerheter vid registrering mellan olika bildunderlag [6]. Vid rekonstruktion av applikatorerna riktas MR-bilden parallellt mot den intrauterina sonden i paracoronal- och sagittalplanet och parallellt med ringen i paraaxialplanet. Om interstitiella nålar används bör man först optimera så att merparten av stråldosen kommer från den intrakavitära applikatorn och sedan optimera stråldosen i nålarna för att finjustera dosfördelningen med avseende på målområde och riskorgan. Bidraget från nålarna bör inte överstiga 10–20 % av den totala behandlingstiden [7].
Stråldosoptimeringen görs med fördel genom invers- och/eller grafisk optimering. Utvärderingen av dosfördelningen bör ske med dosvolym-histogram (DVH). Stråldoser till target och riskorgan bör registreras för varje fraktion så att den ackumulerade dosen kan följas och anpassas till de angivna dosgränserna.
Dosberäkningar vid brachyterapi
Den totala biologiska dosen (EQD2) från extern radioterapi och brachyterapi bör beräknas med den linjärkvadratiska modellen. Exempel på beräkningsark som kan användas är de som tillhandahålls av Medical University of Vienna (LQ spread sheet och Reporting GYN HDR BT sheet via http://www.americanbrachytherapy.org/guidelines/).
För tumöreffekt och tidiga biverkningar används α/β = 10 och för riskorgan och seneffekter α/β = 3. Vid PDR-beräkningar används T1/2 repair half time = 1,5 h [7].
Kvalitetssäkring av behandling vid brachyterapi
Verifikation av strålbehandlingsplan
Kontroller inför start av brachybehandlingen: För behandlingen godkänd dosplan utförs i enlighet med klinikens gängse rutiner.
Kontroller innan behandling
Före start av behandling bör relevanta dosplaneringsparametrar kontrolleras så att de är rätt överförda till behandlingsutrustningen. I övrigt bör kvalitetssäkring utföras i enlighet med t.ex. A practical guide to quality control of brachytherapy equipment, European guidelines for quality assurance in radiotherapy. ESTRO Booklet No. 8. [8].
Registrering och rapportering vid brachyterapi
För närvarande gäller registrering och rapportering enligt ICRU 38. Under 2016 kommer ICRU 89 att publiceras, vilken därefter är normen för rapportering. Sannolikt kommer bl.a. stråldoser och volymer att rapporteras. Detta finns också beskrivet i ESTRO Rec. 2 [9]
Nationella riktlinjer för inrapportering till nationellt register ska följas (INCA), men det är även viktigt att varje klinik har rutiner för intern uppföljning av att kliniska protokoll följs när det gäller behandlingsresultat, biverkningar m.m. Se t.ex. checklistan i bilaga 6 (CTC AE/RTOG). En nationell strålbehandlingsdatabas (DICOM- och DVH-data) är under utarbetande (MIQA).
Referenser
- Haie-Meder C, Potter R, Van Limbergen E, Briot E, De Brabandere M, Dimopoulos J, et al. Recommendations from Gynaecological (GYN) GEC-ESTRO Working Group (I): concepts and terms in 3D image based 3D treatment planning in cervix cancer brachytherapy with emphasis on MRI assessment of GTV and CTV. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2005;74(3):235-45.
- Viswanathan AN, Beriwal S, De Los Santos JF, Demanes DJ, Gaffney D, Hansen J, et al. American Brachytherapy Society consensus guidelines for locally advanced carcinoma of the cervix. Part II: high-dose-rate brachytherapy. Brachytherapy. 2012;11(1):47-52.
- Mohamed S, Kallehauge J, Fokdal L, Lindegaard JC, Tanderup K. Parametrial boosting in locally advanced cervical cancer: combined intracavitary/interstitial brachytherapy vs. intracavitary brachytherapy plus external beam radiotherapy. Brachytherapy. 2015;14(1):23-8.
- Dimopoulos JC, Potter R, Lang S, Fidarova E, Georg P, Dorr W, et al. Dose-effect relationship for local control of cervical cancer by magnetic resonance image-guided brachytherapy. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2009;93(2):311-5.
- Pötter R, Georg P, Dimopoulos JC, Grimm M, Berger D, Nesvacil N, et al. Clinical outcome of protocol based image (MRI) guided adaptive brachytherapy combined with 3D conformal radiotherapy with or without chemotherapy in patients with locally advanced cervical cancer. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2011;100(1):116-23.
- Hellebust TP, Kirisits C, Berger D, Perez-Calatayud J, De Brabandere M, De Leeuw A, et al. Recommendations from Gynaecological (GYN) GEC-ESTRO Working Group: considerations and pitfalls in commissioning and applicator reconstruction in 3D image-based treatment planning of cervix cancer brachytherapy. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2010;96(2):153-60.
- Trnková P, Pötter R, Baltas D, Karabis A, Fidarova E, Dimopoulos J, et al. New inverse planning technology for image-guided cervical cancer brachytherapy: description and evaluation within a clinical frame. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2009;93(2):331-40.
- Thames HD. An 'incomplete-repair' model for survival after fractionated and continuous irradiations. International journal of radiation biology and related studies in physics, chemistry, and medicine. 1985;47(3):319-39.
- Pötter R, Haie-Meder C, Van Limbergen E, Barillot I, De Brabandere M, Dimopoulos J, et al. Recommendations from gynaecological (GYN) GEC ESTRO working group (II): concepts and terms in 3D image-based treatment planning in cervix cancer brachytherapy-3D dose volume parameters and aspects of 3D image-based anatomy, radiation physics, radiobiology. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2006;78(1):67-77.
