Primär behandling av prostatacancer med spridning
Oligometastatisk prostatacancer (inklusive cN1M0)
Rekommendationer: Primärt oligometastatisk prostatacancer (inklusive cN1M0)
- Vår definition av oligometastatisk sjukdom är ≤ 4 skelettmetastaser och ingen visceral metastasering.
- Handläggningen bör diskuteras på MDK.
- Män med nyligen påvisade fjärrmetastaser bör genomgå både skelettskintigrafi och skiktröntgen av torax-buk för kartläggning av metastasutbredning, åtminstone om tillägg av systemisk behandling eller lokal strålbehandling kan bli aktuell (⊕).
- Män med metastaserad prostatacancer som kan vara aktuella för tillägg av systemisk behandling och/eller strålbehandling bör träffa en uroonkolog (⊕⊕).
- Strålbehandling mot primärtumören: Män med mer än 5 års förväntad kvarvarande livstid bör erbjudas primär strålbehandling mot primärtumören (⊕⊕⊕), om de inte har samsjuklighet som kraftigt ökar risken för biverkningar av strålbehandlingen. Strålbehandling bör kombineras med hormonell behandling. Hormonbehandlingen kan ges som kontinuerlig bikalutamid- eller kastrationsbehandling under ca 2 år, eller (vid cN1M0) med STAMPEDE:s kombination av GnRH-agonist under 2–3 år och abirateron plus prednisolon under 2 år.
- Om strålbehandling mot primärtumören inte är lämplig (t.ex. på grund av analfistlar eller urinretention), kan radikal prostatektomi med lymfkörtelutrymning övervägas, förutsatt att spridningen är begränsad till regionala lymfkörtlar (cN1M0) och patienten har minst 5 års förväntad kvarvarande livstid (⊕).
- Hormonbehandling bör ges (⊕⊕⊕), med undantag för de patienter med cN1M0 som väljs ut för radikal prostatektomi med eller utan lymfkörtelutrymning (t.ex. på grund av urinretention) och därefter har PSA < 0,1 µg/l (⊕⊕).
- För patienter med genomgången allvarlig kardiovaskulär händelse (t.ex. hjärtinfarkt eller hemorragisk eller ischemisk stroke) bör man överväga GnRH-antagonist (i första hand relugolix då degarelix endast är subventionerat vid behov av snabb kastrationseffekt) vid kastrationsbehandling då det förefaller ge lägre risk för ytterligare kardiovaskulära händelser (⊕⊕).
- Abirateron (alternativt, om abirateron inte är lämpligt: apalutamid eller enzalutamid) bör erbjudas i kombination med kastrationsbehandling till patienter i gott allmäntillstånd (ECOG 0–1) (⊕⊕⊕), se avsnitt 12.2 Primär behandling vid fjärrmetastaser (M1, ej oligometastatisk prostatacancer). Ett alternativ när fulldos strålbehandling ges mot primärtumören vid cN1 är att ge 2 års abirateron plus prednisolon. De som inte bedöms tåla eller som avböjer denna kombinationsbehandling kan initialt få behandling med enbart bikalutamid.
- Lokal behandling av metastaser bör enbart ske inom ramen för en prospektiv studie.
- Aktuella studier: Den svenska randomiserade studien Hypo-M1/SFUO-4 jämför fraktioneringen 57 Gy i 19 fraktioner (en fraktion varje vardag) med 36,6 Gy i 6 fraktioner (en fraktion varannan dag) mot primärtumören. METRO undersöker tillägget stereotaktisk strålbehandling av 1–3 oligometastaser enligt PSMA-PET-DT-staging i tillägg till standardbehandling hos hormonkänslig prostatacancer vid både de novo och återfall efter robotassisterad laparoskopisk radikal prostatektomi (RALP) eller strålbehandling.
Rekommendationer om uppföljning av män med oligometastatisk prostatacancer
- Efter kompletterande systemisk behandling bör DT buk-torax och skelettskintigrafi utföras efter 6 månader. För övrigt, se Kapitel 17 Uppföljning.
Rekommendationer: Oligometastatiskt återfall
- Handläggningen bör diskuteras på MDK.
- Män med oligometastatiskt återfall som är aktuella för tillägg av systemisk behandling bör genomgå skelettskintigrafi samt skiktröntgen av torax-buk för kartläggning av metastasutbredning (⊕).
- Män med metastaserad prostatacancer som kan vara aktuella för tillägg av systemisk behandling eller strålbehandling bör träffa en uroonkolog (⊕⊕).
- Abirateron (alternativt apalutamid eller enzalutamid om abirateron inte är lämpligt) bör erbjudas i kombination med kastrationsbehandling till patienter i gott allmäntillstånd (ECOG 0–1) (⊕⊕⊕), se avsnitt 12.2 Primär behandling vid fjärrmetastaser (M1, ej oligometastatisk prostatacancer). De som inte bedöms tåla eller som avböjer denna kombinationsbehandling bör få behandling med enbart bikalutamid.
- Lokal behandling av metastaserna bör endast ges inom ramen för forskning.
- Aktuell studie: METRO undersöker tillägget stereotaktisk strålbehandling av 1–3 oligometastaser enligt PSMA-PET-DT-staging i tillägg till standardbehandling hos hormonkänslig prostatacancer vid både de novo och återfall efter RALP eller strålbehandling.
Faktaruta: ECOG
- ECOG 0: Fullt aktiv i ett för individen normalt liv.
- ECOG 1: Kan inte utföra fysiskt krävande uppgifter, men klarar kontorsarbete, dagliga sysslor i hemmet och liknande fysiskt lätt till måttligt arbete.
- ECOG 2: Kan inte utföra ens lätta arbetsuppgifter, men klarar själv av att sköta sin hygien och liknande aktiviteter (aktiviteter i det dagliga livet, ADL). Aktiv och rörlig mer än hälften av dagen.
- ECOG 3: Klarar bara delar av ADL själv. Rörlig mindre än hälften av dagen; sängliggande eller bekvämt sittande större delen av dagen.
- ECOG 4: Klarar inte ADL själv. Helt beroende av daglig omvårdnad. Tillbringar hela dagen i sängen eller bekvämt sittande.
Introduktion
Begreppet oligometastatisk sjukdom introducerades 1995 som ett stadium mellan lokaliserad och fjärrspridd cancersjukdom 454 . Det saknas en allmänt vedertagen definition av begreppet ”oligometastatisk”, men oftast avses upp till 3–5 metastaser 455 . Vi har valt att definiera oligometastatisk sjukdom som ≤ 4 metastaser varav ingen visceral eller utanför axialskelettet. En expertpanel gjorde nyligen en systematisk översikt av området och definierade olika kliniska situationer då oligometastatisk sjukdom kan uppstå 455. Följande avsnitt handlar om patienter som för första gången får konstaterat metastatisk sjukdom och inte tidigare fått systemisk behandling, antingen i samband med prostatacancerdiagnosen (synkron oligometastatisk sjukdom) eller i ett senare skede (> 6 månader från diagnosen = metakron oligometastatisk sjukdom). Nedan berörs aspekter som är specifika för oligometastatisk sjukdom. För information om systemisk behandling vid spridd prostatacancer hänvisas till nästa avsnitt.
Primär spridning till regionala lymfkörtlar (cN1M0)
Det finns inga resultat från randomiserade studier som specifikt studerat effekten av radikal behandling av primärtumören vid regionalt lymfkörtelmetastaserad prostatacancer (cN1M0). Det ter sig dock rimligt att extrapolera resultaten från den metaanalys som visar att strålbehandling av primärtumören som tillägg till hormonbehandling förlänger överlevnaden hos män med ett fåtal skelettmetastaser 273 . En icke-randomiserad jämförelse i STAMPEDE-studien talar för att strålbehandling mot primärtumör och iliakala lymfkörtelstationer som tillägg till hormonbehandling förlänger tiden till återfall med ett par år för män med prostatacancer cN1M0 440 . Även flera observationsstudier talar för en gynnsam effekt av att behandla primärtumören vid regionalt lymfkörtelmetastaserad prostatacancer, antingen med radikal prostatektomi och iliakal lymfkörtelutrymning 370 , 456 457 458 , eller med extern strålbehandling 459 460 , men resultaten kan ha påverkats av selektion.
Både apalutamid och enzalutamid fick 2021 indikationen ”metastaserad hormonkänslig prostatacancer (mHSPC) hos vuxna män i kombination med androgen deprivationsterapi”. Denna indikation omfattar även patienter med cN1M0. Denna patientgrupp ingick i de randomiserade studierna ARCHES, ENZAMET och TITAN som visade lika god effekt av tillägg med apalutamid och enzalutamid vid cN1M0 som vid M1 461 462 463 464 .
Nyligen redovisade resultat från STAMPEDE visar att 2 års tillägg av abirateron plus prednisolon till adjuvant GnRH-agonist (under 3 år) förbättrade behandlingseffekten vid prostatacancer med flera ogynnsamma prognostiska faktorer. Drygt en tredjedel (39 %) av patienterna i studien hade lymfkörtelmetastaser, så resultaten bedöms vara relevanta för denna patientgrupp. Efter 6 år ökade andelen utan påvisad metastasering från 69 % till 82 % och den totala överlevnaden från 77 % till 86 % 394 .
Primär oligometastatisk fjärrspridning (M1)
Majoriteten av studierna av kompletterande systemisk behandling för fjärrmetastaserad prostatacancer har även omfattat patienter med oligometastatisk spridning. Överväganden om kompletterande systemisk behandling för patienter med fjärrmetastaserad prostatacancer gäller därför även undergruppen med oligometastatisk spridning. Således bör patienterna få tillägg av abirateron till kastrationsbehandlingen eller, om det inte är lämpligt, apalutamid eller enzalutamid . Nyligen har data publicerats för darolutamid, resultaten var positiva gällande rPFS men utan signifikant effekt på totalöverlevnad. Det finns ännu inget godkännande från EMA 465 .
För män med nydiagnostiserad oligometastatisk prostatacancer ≤ 4 metastaser, varav ingen visceral eller utanför axialskelettet, ökar tillägg av strålbehandling av primärtumören andelen som lever efter 3 år med 8 procentenheter 273 294 295 . I en av studierna, STAMPEDE 273 , erhöll 18 % av patienterna både kompletterande strålbehandling av primärtumören och docetaxel. Det finns inga motsvarande studier av kombination av apalutamid, darolutamid och enzalutamid med lokal strålbehandling vid begränsad metastasering.
De randomiserade studierna av strålbehandling av primärtumören vid spridd prostatacancer omfattade en predefinierad subgruppsanalys av oligometastatisk sjukdom (1–4 fjärrmetastaser utan visceral metastasering) 294 295 . Definitionen av oligometastatisk sjukdom i dessa studier var arbiträr och avspeglar inte någon biologisk gräns 466 . En senare analys av STAMPEDE talar för att män med enbart lymfkörtelmetastaser (stadium M1a) eller 1–3 skelettmetastaser utan viscerala metastaser är den grupp som får överlevnadsvinst av strålbehandling och därför bör erbjudas lokal strålbehandling mot primärtumören 466 . Man bör notera att definitionen baserades på fynd vid skelettskintigrafi och skiktröntgen. Den kan därför inte direkt överföras till fynd vid PET-DT, som har högre sensitivitet för metastaser (särskilt PSMA-PET-DT). Det finns inga resultat från randomiserade studier av prostatektomi vid fjärrmetastaserad prostatacancer.
I STAMPEDE fick hälften av patienterna kompletterande strålbehandling mot primärtumören (36 Gy i 6 fraktioner med en veckas intervall, eller 55 Gy i 20 fraktioner varje vardag) som tillägg till kastrationsbehandling, med eller utan docetaxel. Efter tre år levde 81 % av de patienter med oligometastatisk sjukdom som fick strålbehandling mot primärtumören och 73 % av de som inte fick det. HORRAD omfattade betydligt färre patienter med oligometastatisk sjukdom, men tilläggseffekten av strålbehandling mot primärtumören (70 Gy i 35 fraktioner eller 57,76 Gy i 19 fraktioner) var densamma som i STAMPEDE 294 295. En metaanalys av dessa båda studier visade att strålbehandling mot primärtumören ledde till en absolut överlevnadsvinst på 7 % efter tre år273. De strålbehandlingsrelaterade biverkningarna var lindriga eller måttliga för de flesta patienterna, men i STAMPEDE rapporterade 5 % biverkningar med grad 3–4 från urinblåsa och tarm 294 295. I HORRAD hade 20 % kvarstående tarmbesvär 2 år efter strålbehandlingen 467 . Den 4-armade studien PEACE1 468 har nu rapporterat även angående strålbehandling. I standardbehandling ingick kastration och docetaxel från och med tidpunkten för den protokolluppdatering som gjorde detta obligatoriskt. Hälften av patienterna har också fått abirateron. När patienterna hade standardbehandling plus abirateron med tillägg av strålbehandling så förlängdes radiologisk progressionsfri överlevnad med en betydande tid liksom även tiden till kastrationsresistens. Däremot kunde man inte påvisa en förlängd total överlevnad med tillägget av strålbehandling, inte ens i gruppen med låg volym av metastaser. Ett annat sekundärt mål var att se på förekomsten av allvarliga genito-urinala händelser; behov av KAD, suprapubisk kateter, inläggning av Jstent, nefrostomi, TURP, senare strålbehandling av primärtumören eller prostatektomi. För både gruppen med låg respektive hög volym av metastaser halverades förekomsten av dessa händelser. Förekomsten av allvarliga biverkningar var lika i båda grupperna med eller utan strålbehandling medan mildare grad av dysuri, pollakisuri och nykturi var ökad i strålbehandlingsgruppen.
Det ses divergerade resultat i de två stora studierna men utifrån att det fanns en så tydlig överlevnadsvinst i STAMPEDE för lågvolymsgruppen, och att det i PEACE-1 visades en rPFS-vinst samt förlängd tid till kastrationsresistens för lågvolym, så väljer vi att ändå rekommendera strålbehandling till lågvolymsgruppen. Medan man för de med mer uttalad spridning kan det vara av värde att diskutera ett möjligt tillägg av strålbehandling i syfte att förlänga tiden till progress och minska behov av senare mer omfattande ingrepp för vattenkastningsproblem.
Oligometastatiskt återfall med lymfkörtelmetastaser (cN1M0)
En betydande andel av patienterna i de randomiserade fas 2-studierna STOMP och ORIOLE hade återfall med enbart regionala lymfkörtelmetastaser (cN1M0) efter radikal prostatektomi eller kurativt syftande strålbehandling (flertalet var opererade). Båda studierna redovisas mer i detalj nedan i avsnitt 12.1.5 Oligometastatiskt återfall med fjärrspridning (M1). Subgruppsanalyser för patienter med cN1M0 i STOMP, såväl enligt ”intention att behandla” som för patienter som behandlades enligt protokoll, visade att behandling av metastaserna med antingen kirurgi eller stereotaktisk strålbehandling förlängde tiden till start av hormonbehandling med nio månader (riskkvoter 0,46 och 0,40, p < 0,05 )469 . Någon motsvarande subgruppsanalys har inte redovisats från ORIOLE. Ingen av studierna har särskilt resultaten för primärt opererade och primärt strålbehandlade patienter.
Det finns flera observationsstudier av iliakal lymfkörtelutrymning vid återfall med enbart regionala lymfkörtelmetastaser efter radikal prostatektomi 470 . I en studie av 189 patienter med upp till 10 års uppföljning fick samtliga patienter någon kompletterande behandling efter lymfkörtelutrymningen 471 . Studierna är heterogena och saknar lämpliga kontrollgrupper; det går därför inte att basera några rekommendationer på dem. Motsvarande finns även observationsstudier av strålbehandling mot återfall i lymfkörtlar 472 . En systematisk översikt med metaanalys av 10 studier omfattande 653 patienter med upp till 5 metastaser enligt PET-DT som fått stereotaktisk strålbehandling mot metastaserna. I de 5 studier i vilka inga patienter fick samtidig hormonbehandling var 33 % utan biokemiskt återfall, 39 % utan radiologisk progress och 52 % utan hormonbehandling efter 2 år. Allvarliga biverkningar var sällsynta 473 .
Ökande användning av PSMA-PET-DT vid prostatacanceråterfall efter kurativ behandling medför upptäckt av flera patienter med återfall bara i regionala lymfkörtlar. Idag finns det inga specifika rekommendationer hur man skall behandla patienter med begränsat återfall i lokoregionala lymfkörtlar. I den randomiserade fas II PEACE-V-STORM-studien jämförde man metastasriktad strålbehandling med och utan elektiv lymfkörtlelbestrålning för patienter med recidiv och PSMA-PET-DT positiva regionala lymfkörtlar 436 . 196 patienter var randomiserade till bara metastasriktad stereotaktisk strålbehandling 10 Gy x 3 eller metastasriktad stereotaktisk strålbehandling med tillägg av strålbehandling mot elektiva lymfkörtlar 1,8 Gy x 25 med SIB boost 2,6 Gy. Alla patienter fick även 6 månaders ADT. Patienterna hade tidigare opererats, strålbehandlats eller genomgått salvage-strålning lokalt. Kombinationen med elektiva fält och metastasinriktad behandling gav längre bPFS, (69 % vs 47 %, p=0,01), färre regionala återfall och en högre metastasfri överlevnad (HR=0,62; CI 0,44-0,86). Biverkningarna var jämförbara mellan armarna, men med en statistiskt icke-signifikant tendens till lite högre grad av både gastrointestinala och genito-urinära symptom i den lymfkörtelbestrålade gruppen. Baserat på dessa resultat, kan man vid begränsat återfall i regionala lymfkörtlar diskutera strålbehandling av regionala lymfkörtlar med 6 månader ADT för att förlänga bPFS och metastasfri överlevnad, med kostnaden av en viss ökad risk för biverkningar 436 474 .
Oligometastatiskt återfall med fjärrspridning (M1)
Majoriteten av studierna av kompletterande systemisk behandling för fjärrmetastaserad prostatacancer har även omfattat män med oligometastatiskt återfall. Överväganden om kompletterande systemisk behandling för patienter med fjärrmetastaserad prostatacancer gäller därför även undergruppen med oligometastatiskt återfall.
Nya bilddiagnostiska metoder med högre sensitivitet, framför allt PSMA-PET-DT, ökar antalet patienter med oligometastatiskt återfall av prostatacancer 203 . Två randomiserade fas 2-studier, STOMP och ORIOLE, har värderat behandling av metastaserna vid oligometastatiskt återfall av prostatacancer 469 475 .
STOMP inkluderade 62 patienter med 1–3 metastaser enligt kolin-PET-DT, varav 21 hade cN1M0. De flesta hade både opererats och genomgått postoperativ strålbehandling mot prostatabädden. Behandling av metastaserna med antingen kirurgi eller stereotaktisk strålbehandling gav vid en första analys en icke-signifikant förlängd tid till insättning av hormonbehandling, jämfört med enbart observation 469. En uppdaterad analys visade frihet från hormonbehandling hos 34 % av patienterna i behandlingsgruppen och hos 8 % i kontrollgruppen (riskkvot 0,57 med 95 % KI 0,38–0,84) 469. ORIOLE inkluderade 54 patienter med 1–3 metastaser enligt DT eller MRT plus skelettskintigrafi, majoriteten med kirurgi som primärbehandling475. Efter stereotaktisk strålbehandling av metastaserna hade 19 % av patienterna progress inom 6 månader, jämfört med 61 % av patienterna i kontrollgruppen (ingen behandling, p = 0,005).
En randomiserad studie (SABR-COMET) inkluderade 99 patienter med oligometastatisk cancer (1–5 metastaser), varav 16 med återfall av prostatacancer 476 . De patienter som fick stereotaktisk strålbehandling av metastaserna hade längre medianöverlevnad än de som enbart fick standardbehandling (50 jämfört med 28 månader, p = 0,006). Resultaten för patienterna med prostatacancer redovisades inte separat. En större andel av patienterna i strålbehandlingsgruppen hade prostatacancer (21 % jämfört med 6 %). Eftersom prostatacancer har en förhållandevis god prognos, kan detta ha bidragit till den längre överlevnaden i strålbehandlingsgruppen.
Primär behandling vid fjärrmetastaser (M1, ej oligometastatisk prostatacancer)
Rekommendationer om utredning och inledande behandling
- Män med nyligen påvisade fjärrmetastaser bör genomgå både skelettskintigrafi och skiktröntgen av torax-buk för kartläggning av metastasutbredning, åtminstone om tillägg av systemisk behandling eller lokal strålbehandling kan bli aktuellt (⊕).
- Män med symtomgivande fjärrmetastasering bör behandlas snarast möjligt. Tidigt insatt behandling minskar risken för komplikationer såsom ryggmärgskompression och uretärobstruktion (⊕⊕⊕) 268 .
- Män som har nyligen påvisade metastaser och kan vara aktuella för tillägg av systemisk behandling eller strålbehandling bör träffa en uroonkolog (⊕⊕).
- Fjärrmetastaserad prostatacancer bör behandlas med kirurgisk kastration eller GnRH-agonist/antagonist (⊕⊕⊕). Patienter med svåra smärtor, obstruktion av övre urinvägar eller neurologiska symtom bör i första hand behandlas med kirurgisk kastration eller GnRH-antagonist (⊕⊕⊕).
- För patienter med genomgången allvarlig kardiovaskulär händelse (t.ex. hjärtinfarkt eller hemorragisk eller ischemisk stroke) bör man överväga GnRH-antagonist (i första hand relugolix då degarelix endast är subventionerat vid behov av snabb kastrationseffekt) vid kastrationsbehandling då det förefaller ge lägre risk för ytterligare kardiovaskulära händelser (⊕⊕).
- ”Flareprofylax” med bikalutamid 150 mg x 1 bör ges under 4 veckor med start en vecka före första injektionen av GnRH-agonist. (⊕⊕). ”Flareprofylax” behövs inte vid behandling med GnRH-antagonist
- För överväganden om progress under behandling med enbart bikalutamid, se rekommendationsrutan i avsnitt 10.4 Primär hormonell behandling vid M0.
- Vid behandling med kirurgisk kastration, GnRH-agonist eller GnRH-antagonist bör risken för osteoporosrelaterade frakturer värderas, och bentäthetsmätning eller osteoporosbehandling övervägas (⊕⊕). Fysisk aktivitet bör rekommenderas, helst inom ramen för professionellt ledda, strukturerade träningsprogram (⊕⊕⊕). Se avsnitt 15.14 Förebyggande av skelettkomplikationer.
Rekommendationer om kompletterande behandling
- Trippelbehandling med docetaxel plus abirateron med prednisolon plus kastrationsbehandling bör erbjudas till patienter med nyligen påvisad utbredd fjärrmetastasering (≥ 4 skelettmetastaser varav någon utanför axialskelettet och/eller visceral metastasering) under förutsättning att de bedöms tåla denna kombinationsbehandling (⊕⊕⊕). Behandling för osteoporos bör ges (⊕⊕).
- När abirateron inte är lämpligt hos patient som ändå är aktuell för trippelbehandling, bör trippelbehandling med docetaxel och darolutamid erbjudas.
- Tillägg av enbart abirateron med prednisolon (alternativt apalutamid eller enzalutamid om abirateron inte är lämpligt), bör erbjudas till patienter i gott allmäntillstånd om ovanstående trippelbehandling inte är aktuell, även till dem med mindre utbredd metastasering (⊕⊕⊕). Behandling för osteoporos bör ges (⊕⊕).
- Strålbehandling mot primärtumören kan diskuteras med patienten även vid mer utbredd fjärrmetastasering (> 4 skelettmetastaser varav någon utanför axialskelettet och/eller visceral metastasering) där syftet är att förlänga tiden till kastrationsresistens och minska risken för senare svåra problem från urinvägarna.
- Lokal behandling av fjärrmetastaser bör enbart ske inom ramen för prospektiva studier.
Rekommendationer om uppföljning av män med metastaserad prostatacancer
- Efter kompletterande behandling med nya hormonellt verkande läkemedel bör DT buk-torax och skelettskintigrafi utföras efter 6 månader. När docetaxel har givits som tillägg bör bilddiagnostiken upprepas några veckor efter avslutad behandling med docetaxel. För övrigt se Kapitel 17 Uppföljning.
- En viss andel av männen i den här situationen får ny progress utan föregående PSA-ökning, varför årlig radiologi med datortomografi kan vara av värde.
Faktaruta: ECOG
- ECOG 0: Fullt aktiv i ett för individen normalt liv.
- ECOG 1: Kan inte utföra fysiskt krävande uppgifter, men klarar kontorsarbete, dagliga sysslor i hemmet och liknande fysiskt lätt till måttligt arbete.
- ECOG 2: Kan inte utföra ens lätta arbetsuppgifter, men klarar själv av att sköta sin hygien och liknande aktiviteter (aktiviteter i det dagliga livet, ADL). Aktiv och rörlig mer än hälften av dagen.
- ECOG 3: Klarar bara delar av ADL själv. Rörlig mindre än hälften av dagen; sängliggande eller bekvämt sittande större delen av dagen.
- ECOG 4: Klarar inte ADL själv. Helt beroende av daglig omvårdnad. Tillbringar hela dagen i sängen eller bekvämt sittande.
Tillägg av docetaxel + abirateron eller darolutamid eller någon av hormonbehandlingarna abirateron, apalutamid eller enzalutamid till kastrationsbehandling förlänger överlevnaden för män med fjärrspridning av prostatacancer. Som nämnts tidigare ger strålbehandling av primärtumören förlängd överlevnad för män med oligometastatisk spridning, särskilt om ingen kompletterande systemisk behandling ges (se avsnitt 12.1 Oligometastatisk prostatacancer (inklusive cN1M0)). I PEACE1-studien sågs även att sådan strålbehandling kunde förlänga tiden till kastrationsresistens och minska frekvensen av svåra lokala komplikationer för män med mer omfattande spridning. En ökad frekvens av grad 1–2 biverkningar förekommer men grad tre besvär var lika mycket i både strålade och icke-strålade patienter, för de utan strålbehandling då relaterade till sjukdomsprogress.
Tillägg av antingen docetaxel (75 mg/m2 var 3:e vecka vid 6 tillfällen, med prednisolon 5–10 mg) eller abirateron med prednisolon 5 mg inom 3 månader efter start av kastrationsbehandlingen förlänger medianöverlevnaden med omkring 1 år eller mer (⊕⊕⊕) 477 478 479 480 481 482 . Överlevnadsvinsten är sannolikt likvärdig för tillägg av docetaxel och för abirateron med prednisolon 483 . En stor genomgång av STAMPEDE-studien avseende abirateron-armen där man i efterhand stratifierade på ”låg-, kontra högrisk” och ”låg-, kontra högvolym”, enligt de kriterier som gällde i LATITUDE- och CHAARTED-studierna, kunde påvisa klar överlevnadsvinst oavsett kategori för tillägget av abirateron 484 . Både apalutamid och enzalutamid godkändes 2021 av Tandvårds- och läkemedelsförmånsverket för subvention på indikationen tillägg till initial kastrationsbehandling vid metastaserad prostatacancer. Efter en ny genomgång av Tandvårds- och läkemedelsförmånsverket gäller subvention endast då dubblett med abirateron inte bedöms vara lämplig.
Tillägg av apalutamid inom 6 månader efter påbörjad kastrationsbehandling ökade andelen vid liv efter 3 år från omkring 55 % till 70 % 463 464. Studien (TITAN) omfattade enbart patienter med gott allmäntillstånd (ECOG 0–1); 37 % av dem hade oligometastatisk sjukdom och 16 % metastatiskt återfall efter tidigare lokal behandling mot primärtumören463 464. Effekten av behandlingen var densamma för dessa grupper. Behandlingseffekt är visad oavsett tumörbörda. Behandlingstiden med apalutamid var i median 39 månader. Snarlika effekter för tillägg av enzalutamid observerades i ARCHES och ENZAMET 461 , 485 486 487 . Någon prospektiv jämförelse med docetaxel, abirateron/prednisolon eller en kombination av dessa finns inte. Nyligen publicerades resultat från ARANOTE-studien 465 som utvärderar effekten av tilläggsbehandling med darolutamid, studien visar signifikant förlängd rPFS men resultaten för OS är inte signifikanta vid detta tillfälle. I studien inkluderades patienter med ECOG-status 0–2. Behandlingsnyttan observerades i alla undersökta subgrupper, inklusive patienter med både låg- och högvolymsjukdom enligt CHAARTED-kriterierna. EMA-godkännande finns men subventionsbeslut från TLV finns inte.
”Trippelbehandling” med docetaxel (75 mg/m2 var 3:e vecka vid 6 tillfällen), abirateron plus prednisolon 5 mg och kastrationsbehandling förlänger överlevnaden jämfört med tillägg av enbart docetaxel, enligt den nyligen presenterade PEACE-1 488 För män med utbredd tumörbörda (≥ 4 skelettmetastaser varav någon utanför axialskelettet och/eller visceral metastasering) var medianöverlevnaden 19 månader längre (totalt 61 månader) (⊕⊕⊕). Längre uppföljningstid behövs för att utvärdera effekten för män med mindre tumörbörda. I studien påbörjades docetaxel och abirateron/prednisolon inom 3 månader efter start av kastrationsbehandling.
ARASENS-studien av trippelbehandling med docetaxel, darolutamid och kastration 489 . Efter 4 års uppföljning levde 63 % av patienterna som fått trippelbehandling och 50 % av dem som fått docetaxel, kastrationsbehandling och placebo. Vinsten med trippelbehandling sågs oavsett tumörvolym. Tandvårds- och läkemedelsförmånsverket har godkänt subventionering av darolutamid på denna indikation med begränsningen ”när behandling med abirateron inte är lämpligt”.
Utifrån dessa båda triplettstudier, som visar att tillägg med hormoner till kastration och docetaxel ger behandlingsvinst, rekommenderar vårdprogramgruppen inte längre en dubblett med enbart docetaxel. Bristen på evidens för jämförelsen mellan triplett (ADT+ARPI+docetaxel) och dubbel (ADT+ARPI) gör det svårt att ge en stark rekommendation för det ena alternativet framför det andra, inklusive för patienter med synkron högvolymssjukdom. Om triplett inte bedöms vara indicerat utifrån allmäntillstånd och tumörsituation rekommenderas en dubblett med kastration och i första hand abirateron, eller om abirateron inte bedöms lämpligt, apalutamid/enzalutamid.
Definitionerna av låg och hög volym av metastaser i de ovan nämnda studierna var arbiträra och avspeglar inte någon biologisk gräns. En sammantagen bedömning av studierna talar dessutom emot att gränsen är av betydelse för om olika typer av kombinerade systemiska behandlingar har effekt eller inte. Valet av tilläggsbehandling för individuella patienter kan därför vara svårt. Man bör notera att definitionerna baseras på fynd vid skelettskintigrafi och DT. För patienter som har utretts med PET-DT, som har högre sensitivitet för detektion av metastaser (särskilt PSMA-PET-DT), kan behandlingsvalet vara särskilt svårt, eftersom de patienter som ingick i de aktuella studierna enbart utreddes med skelettskintigrafi och DT, och deras metastasutbredning ser helt annorlunda på PSMA-PET-DT. I figur 9 presenteras en schematisk sammanställning av behandlingsrekommendationer vid primärt metastatisk sjukdom.
Intresse av att värdera nyttan av dessa behandlingar är stort. Flera analyser av PSA respons vid olika tidpunkter som en surrogatmarkör för effektivitet finns. En stor meta-analys 490 av flera studier inom såväl mHSPC som CRPC området visar att ett omätbart PSA i den hormonkänsliga metastaserade gruppen vid 6 månader var klart kopplat till bättre överlevnad. Detta gällde oavsett vilken ARPI som kompletterade kastrationen.
För patienter med relativt begränsad, icke-symtomgivande skelettmetastasering kan initial behandling med enbart bikalutamid övervägas om patienten önskar undvika de biverkningar som kastrationsbehandling ofta ger. Värdet av kompletterande systemisk eller lokal behandling är inte studerat för män som behandlas med bikalutamid i stället för med kastrationsbehandling.
Figur 9.Schematisk översikt över behandlingsalternativ vid metastaserad sjukdom. Läkemedel i fet stil innebär förstahandsalternativ. Subvention och indikation för övriga läkemedel endast om förstahandsalternativet ej anses vara lämpligt.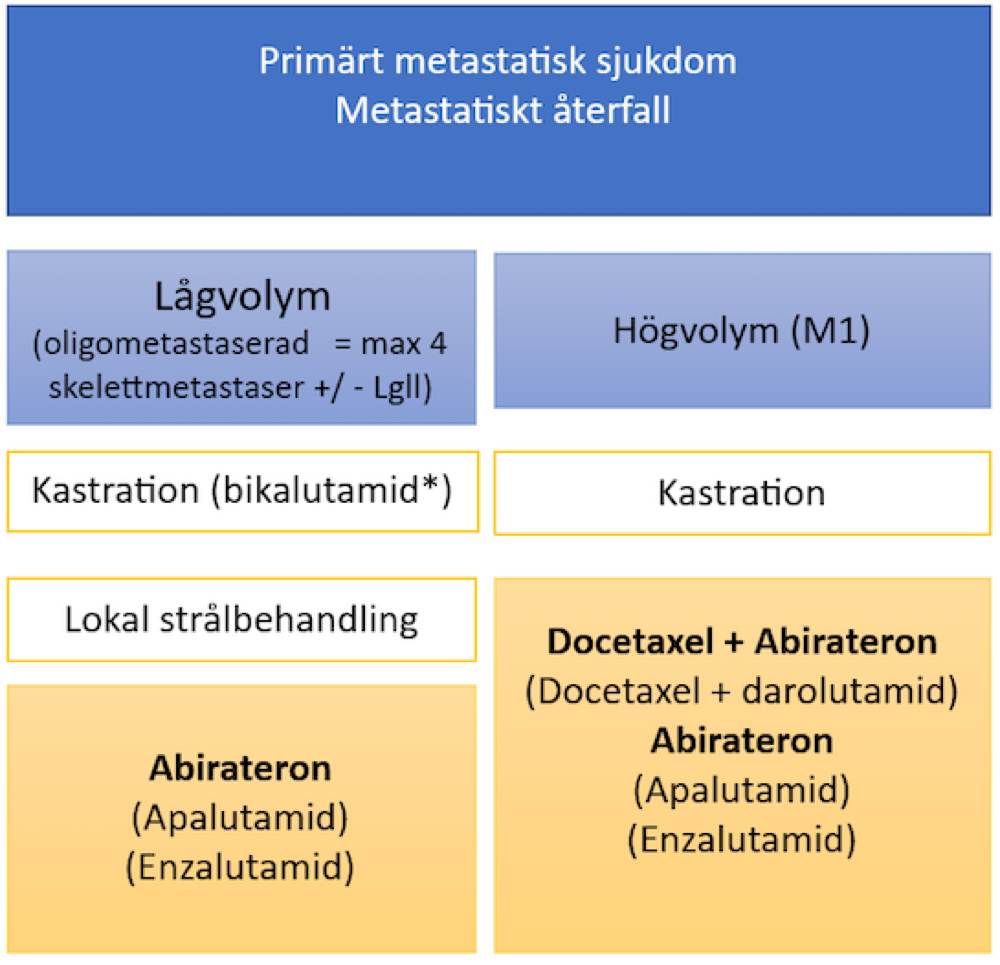
*Bikalutamid kan vara ett alternativ i de fall övrig sjuklighet indikerar kort återstående livslängd och prostatacancern inte ger så mycket symtom.
Bedömning av äldre för onkologisk behandling
- Skattningsverktyg kan användas som stöd inför behandlingsbeslut i både den kurativa och den palliativa situationen.
Behandlingsmöjligheterna för patienter med prostatacancer i palliativ fas, och därmed överlevnaden, har ökat under de senaste åren. Denna patientgrupp utgörs till stor del av en äldre population som ofta är en heterogen grupp med varierande samsjuklighet. Kliniska studier exkluderar ofta patienter med samsjuklighet, kognitiv påverkan och funktionella begränsningar, vilket är vanligt förekommande hos denna population. För att undvika överbehandling, och i värsta fall att skada patienten, är det därför minst lika viktigt att göra en noggrann bedömning av patientens status och skörhet inför palliativ behandling av prostatacancer som inför kurativt syftande behandling. Klassiska performancestatusskalor såsom ECOG kan ge vägledning men är ej tillräckliga för att bedöma tolerans av behandling och överlevnad hos äldre 491 . Åldersassocierad skörhet är vanligt, vilket innebär att patienten har nedsatta fysiologiska reserver och därmed ökad sårbarhet för yttre påfrestningar. Detta leder bl.a. till sämre tolerans för cytostatika och högre dödlighet 492 493 .
Exempel på skattningsverktyg
Det finns flera olika tillgängliga skattningsverktyg. Nedan följer beskrivning av några exempel:
Geriatric-8
Det finns flera olika verktyg för screening av åldersassocierad skörhet, däribland Vulnerable Elders Survey (VES-13), Clinical Frailty Scale och Geriatric-8 (G8). Det senare har i många studier visat sig vara ett av de mest robusta med hög sensitivitet och acceptabel specificitet, och det används ofta inom onkologin 225 226 . Verktyget består av åtta frågor som rör matintag, viktnedgång, aktivitetsförmåga, mental status, BMI, polyfarmaci, egenbedömd hälsostatus och ålder. En poäng mellan 0 och 17 genereras där poäng ≤ 14 betraktas som avvikande och innebär därmed ökad risk för skörhet hos patienten. Dessa patienter behöver ibland utredas vidare ur ett geriatriskt perspektiv, och det kan vara särskilt viktigt att noga överväga behandlingsbeslut. Patienter med poäng ≤ 14 har sämre överlevnad och större risk för toxicitet och avbrott i behandling med taxaner 494 495 496 497 . Låg G8-poäng har även visat sig vara associerat med sämre följsamhet och kortare överlevnad jämfört med patienter med normal G8-poäng vid behandling med abirateron och enzalutamid 498 499 . Det är högst sannolikt att detsamma gäller oavsett typ av androgen receptor pathway inhibitors (ARPi), men data på övriga läkemedel i gruppen saknas i dagsläget.
Minicog
G8 screenar inte för kognitiv nedsättning vilket kan vara viktigt att utvärdera inför behandlingsbeslut. Minicog är ett enkelt och validerat test som screenar för kognitiva funktioner, där patienten ombeds memorera tre ord, rita en klocka och sedan sätta visare på tio över elva 500 . På så sätt kan man fånga upp patienter med kognitiv nedsättning som inte upptäcks genom screening med enbart G8 501 .
Det är förstås viktigt att komma ihåg att screeningmetoder ger en överblick över patientens tillstånd och viss vägledning i beslut om behandling. För att göra en mer omfattande bedömning kan man behöva kartlägga andra faktorer såsom ADL och socialt stöd.
Kardiovaskulär riskbedömning vid antihormonell långtidsbehandling
Förra året publicerades de första riktlinjerna för kardioonkologi av European Society of Cardiology 502 . I dessa fastslås att risken för kardiovaskulär sjukdom, stroke och diabetes mellitus typ 2 ökar vid antihormonell långtidsbehandling. En strukturerad bedömning av patientens totala kardiovaskulära risk, med en kartläggning av alla kardiovaskulära riskfaktorer, är därför ofta motiverad vid denna behandling (se vidare avsnitt 15.12 Biverkningar av antihormonell långtidsbehandling).
Kardiovaskulär riskbedömning inför start av ARPi eller cytostatika
Eftersom behandling med ARPi och cytostatika kan ge upphov till kardiovaskulära biverkningar såsom hypertoni, ischemisk hjärtsjukdom, hjärtsvikt och tromboembolism, bör man inför start göra en kardiovaskulär riskbedömning. En sådan bedömning kan inkludera anamnes, klinisk undersökning, blodprovtagning samt ev EKG och EKO. Risken är särskilt hög hos patienter med redan existerande hjärt-kärlsjukdomar och dessa patienter behöver ibland följas upp via kardiolog. Genom att kartlägga riskfaktorer och identifiera patienter med ökad risk för kardiovaskulär toxicitet kan man vidare arbeta med förebyggande åtgärder och anpassa uppföljningen individuellt (Se bilaga 9 Exempel på Kardiovaskulär riskbedömning inför start av ARPi eller cytostatika vid prostatacancer) för exempel på vad som kan ingå i en kardiovaskulär riskbedömning och hur man kan resonera kring detta. Det är dock viktigt att notera att detta endast är ett exempel, och anpassningar på regional eller lokal nivå kan ofta vara nödvändiga beroende på verksamhetens förutsättningar och rutiner. Patienter som är hjärtfriska eller stabila i sin hjärtsjukdom kan remitteras till primärvården för optimering och uppföljning av blodtryck, HbA1c, blodfetter samt andra kardiovaskulära riskfaktorer. För mer information om bedömning och behandling av biverkningar vid antihormonell långtidsbehandling, se nedan samt avsnitt 15.12 Biverkningar av antihormonell långtidsbehandling.
Olika typer av kastrationsbehandling
Kirurgisk kastration
Ingreppet kan utföras som antingen subkapsulär eller total orkidektomi (ablatio testis). Det ger omedelbar nedgång i cirkulerande testosteron, vilket är en fördel vid hotande ryggmärgskompression. Kostnaden är låg, lägre än för ett års behandling med GnRH-agonist eller GnRH-antagonist. Nackdelarna är att många upplever det som en stympande behandling och att det är ett irreversibelt ingrepp. Om det inte är säkert att kastrationsbehandlingen ska vara livslång ska den därför påbörjas med GnRH-agonist/antagonist.
Medicinsk kastration med GnRH-agonist
Behandling med GnRH-agonister bedöms vara likvärdig med kirurgisk kastration när det gäller såväl effekt på sjukdomen som biverkningar. Det finns flera likvärdiga preparat för depåinjektioner som ges med 1, 2, 3 eller 6 månaders intervall. Kostnaden för ett års behandling är klart högre än för kirurgisk kastration och parenteralt östrogen.
Den initialt ökande insöndringen av testosteron vid den första injektionen kan ge eller förvärra symtomen (”flare”) innan kastrationen nås efter 2 veckor. Behandling med bikalutamid 150 mg dagligen bör därför påbörjas 1 vecka före första injektionen med GnRH-agonist (baserat på halveringstiden 3 dygn) och fortsättas under 4 veckor. Valet av dosen 150 mg baseras på att 50 mg ger otillräcklig receptorblockad vid fysiologiska testosteronnivåer 503 och kan därmed knappast blockera de suprafysiologiska nivåerna vid ”flare”.
Om man efter någon månads behandling med GnRH-agonist inte ser den förväntade nedgången i PSA bör plasmatestosteron kontrolleras. Nivån bör vara < 0,7 nmol/l 504 505, men vad som är en terapeutiskt relevant ”kastrationsnivå” är inte klart definierat.
För att säkerställa fullgod kort- och långtidseffekt av behandling med GnRH-agonist bör plasmatestosteron kontrolleras efter någon månad.
Medicinsk kastration med GnRH-antagonist
Degarelix (Firmagon) finns för närvarande endast som subkutan injektion med 1 månads intervall 506 507 . Degarelix ger kastrationseffekt inom ett dygn utan ”flare” och är därför ett bra alternativ till kirurgisk kastration när snabb effekt önskas vid svåra symtom, t.ex. obstruktion av de övre urinvägarna eller hotande kompression av ryggmärgen.
En peroral GnRH-antagonist, relugolix, godkändes 2022 av EMA, och är sedan oktober 2023 subventionerad av Tandvårds- och läkemedelsförmånsverket. Relugolix jämfördes med leuprolid var 3:e månad i en stor fas 3-studie 508 . En större andel av männen som behandlades med relugolix hade kastrationsnivå för testosteron under 48 veckor (97 % jämfört med 89 %). För den biverkan som klassificerades som ”MACE” allvarlig kardiovaskulär händelse (hjärtinfarkt eller hemorragisk eller ischemisk stroke) var det en skillnad mellan behandlingsgrupperna i incidens. Bland dem som tidigare inte genomgått en sådan händelse hade 2,8 % i relugolixgruppen och 4,2 % i leuprorelidgruppen en sådan händelse, jämfört med 3,6 % respektive 17,8 % bland de män som före starten av kastrationsbehandling hade haft en allvarlig kardiovaskulär händelse. Det indikerar att män med mer allvarlig samsjuklighet kan ha ännu större vinst av att behandlas med GnRH-antagonist. Testosteronnivåerna minskade snabbare efter insättning, och kastrationsnivåer uppnåddes efter 4 dagar och normaliserades snabbare efter utsättning av relugolix. I en annan studie jämfördes relugolix med degarelix som neoadjuvant behandling inför extern strålbehandling. Det framgick att de gav lika snabb minskning av testosteron, men återhämtningen till normala nivåer var snabbare för relugolix 509 . För att säkerställa fullgod kort- och långtidseffekt av behandling med GnRH-antagonist bör även plasmatestosteron kontrolleras efter någon månad. Plasmatestosteron bör vara < 0,7 nmol/l 504 505, men vad som är en terapeutiskt relevant ”kastrationsnivå” är inte klart definierat.
Vid byte från GnRH-antagonist i injektionsform till GnRH-agonist behövs inte flareprofylax med antiandrogen. En liten stegring av S-testosteron över kastrationsnivå kan uppstå under en kortare tid, men detta har sannolikt ingen klinisk betydelse 510 . Det saknas helt evidens för hur en övergång mellan peroral GnRH-antagonist och GnRH-agonist ska gå till. Då den perorala GnRH-antagonistens halveringstid är snabb bör man dock sannolikt ha ett överlapp mellan medicinerna för att slippa ett flarefenomen.
Kombinerad androgen blockad
För att blockera även binjurebarksandrogener kan kastrationsbehandling kombineras med bikalutamid. I en metaanalys var 5-årsöverlevnaden 3 procentenheter bättre vid kastrationsbehandling tillsammans med icke-steroidalt antiandrogen än vid enbart kastrationsbehandling 511. I en senare, japansk studie gav tillägg av bikalutamid till GnRH-agonist ingen fördel för patienter med fjärrmetastaser, men längre överlevnad för patienter utan fjärrmetastaser 512 .
Intermittent behandling med GnRH-agonist/antagonist
Intermittent behandling med GnRH-agonist/antagonist har väsentligen likvärdig effekt som kontinuerlig kastrationsbehandling 513 . Fördelarna är lägre kostnad än vid kontinuerlig behandling med GnRH-agonist/antagonist och att patienterna slipper biverkningar under den tidsperiod som testosteronnivåerna är nära normalvärdet, och därmed får en förbättrad livskvalitet 513. Vanligen utgör emellertid denna tidsperiod en mycket liten andel av behandlingen. En nackdel är att behandlingen kräver mer resurser för uppföljning. Evidensläget för intermittent behandling med GnRH-antagonist är lägre än med GnRH-agonist, men det snabbare återhämtandet av testosteronproduktion som finns dokumenterad bör snarast vara till GnRH-antagonistens fördel.
Östrogenbehandling
En pågående randomiserad studie jämför östrogenplåster med GnRH-agonist för män med avancerad prostatacancer 514 . Studien har rapporterat frekvensen av kardiovaskulär sjuklighet och inte kunnat påvisa någon skillnad i frekvens mellan GnRH-agonist och transdermalt östrogen 515 .
Biverkningar: Östrogenplåster har gynnsammare biverkningsprofil och ger bättre livskvalitet än GnRH-agonist 516 . Parenteral östrogenbehandling minskar libido, men ger inte osteoporos 517 . Svettningar och värmevallningar är sällsynta 516 517 517 . Profylaktisk strålbehandling av brösten bör erbjudas inför behandlingen, för att förebygga tillväxt av brösten. Parenteral östrogenbehandling ger något ökad risk för kardiovaskulär sjuklighet och, efter flera års behandling av män med känd kardiovaskulär sjukdom, något ökad kardiovaskulär dödlighet 517 518 519 .
Nya hormonellt verkande behandlingar – androgen receptor pathway inhibitors (ARPi)
Abirateron med prednisolon
Abirateron blockerar enzymet 17α-hydroxylas och därmed all syntes av testosteron. Abirateron ges tillsammans med prednisolon 5–10 mg dagligen, beroende på indikation.
Indikationer, dosering, biverkningar och uppföljning: se Fass och Nationella regimbiblioteket.
Kommentar om byte av kortikosteroid: Vid långsamt stigande PSA-värden hos patienter som initialt haft god behandlingseffekt av abirateron med prednisolon, kan byte av prednisolon till dexametason (0,5 mg) övervägas (⊕⊕). I en liten fas 2-studie (n = 26) medförde bytet sjunkande PSA-värden hos nästan hälften av patienterna.
Apalutamid, darolutamid och enzalutamid
Apalutamid, darolutamid, och enzalutamid är androgenreceptorblockerare med betydligt kraftigare effekt än bikalutamid.
Indikationer, dosering, biverkningar och uppföljning: se Fass och Nationella regimbiblioteket.
Omvårdnad och rehabilitering för män med spridd sjukdom
Patienten ska erbjudas såväl muntlig som skriftlig information om den hormonella behandlingens duration, verkningsmekanism och biverkningar. Min vårdplan uppdateras i samråd med patienten. Man bör stärka patientens hopp om att få en god livskvalitet trots kronisk cancersjukdom.
Rehabiliteringsbehovet bör återkommande bedömas med hjälp av samtal och strukturerade instrument (enkäter). ”Hälsoskattning för cancerrehabilitering” är ett sådant instrument som rekommenderas för strukturerad bedömning av rehabiliteringsbehov (Regionala cancercentrum/Bedömning av rehabiliteringsbehov), se Kapitel 15 Biverkningar: omvårdnad, rehabilitering och behandling.
Aktiv uppföljning med samtal om biverkningarna kan göra att patienten tolererar och accepterar behandlingen bättre, även om en del av biverkningarna är ofrånkomliga. Det finns ofta alternativ till den pågående behandlingen som kanske ger mindre negativ påverkan på livskvaliteten.
Vid kastrationsbehandling försvinner oftast den sexuella lusten och förmågan, vilket bör diskuteras med patienten och, om möjligt, hans partner. Om mannen har kvar den sexuella lusten kan erektionssvikten behandlas på vanligt vis.
Patienten bör rekommenderas fysisk aktivitet och rökstopp. Det är önskvärt att enheter som behandlar denna patientgrupp kan hänvisa till professionellt ledda, strukturerade träningsprogram 520 . Kastrationsbehandling ger ofta ökad mängd bukfett, minskad muskelmassa, fysisk och mental trötthet (fatigue), samt humörsvängningar och nedstämdhet. Ökad fysisk aktivitet med regelbunden träning kan motverka bukfetman och öka muskelmassan, vilket i sin tur kan leda till mindre trötthet och bättre livskvalitet 521 .
Kontaktsjuksköterskan ansvarar tillsammans med läkaren för att risken för osteoporos och frakturer bedöms och att behandling blir insatt när indikation finns. Det är viktigt att den kontaktsjuksköterska som har en regelbunden kontakt med patienten identifierar riskfaktorer för osteoporos, t.ex. långvarig kastrationsbehandling, kortisonbehandling, rökning, immobilitet, lågt BMI och högt alkoholintag.
De nya behandlingsmetoder som nu kommer för patienter med prostatacancer kräver systematisk uppföljning och kontroll av biverkningar, så att sjukvården får kunskap om vilka omvårdnadsåtgärder som krävs.
