Primär behandling av prostatacancer utan spridning
Val av behandling
|
Rekommenderad riskgruppsindelning |
||
|
1 |
Mycket låg risk |
cT1c*, Gleasonsumma 6, ≤ 8 mm cancer totalt i 1–4 av 8–12 systematiska biopsikolvar, PSA < 10 µg/l och PSA-densitet < 0,15 µg/l/cm3 |
|
2 |
Lågrisk |
cT1–cT2a*, Gleasonsumma 6 och PSA < 10 µg/l som inte uppfyller kriterierna för mycket låg risk |
|
3 |
Gynnsam mellanrisk |
En av följande riskfaktorer: cT2b-cT2c* eller Gleasonsumma 3 + 4 (ISUP 2) eller PSA 10–19 µg/l |
|
4 |
Ogynnsam mellanrisk |
> 1 av ovanstående riskfaktorer eller |
|
5 |
Högrisk |
cT3a eller stark misstanke om extraprostatisk växt på MRT (EPE/SVI 5)* eller |
|
6 |
Mycket hög risk |
2–3 av högriskfaktorerna ovan |
* T-stadium kategoriseras enbart med palpation, men fynd på MRT bör vägas in vid val av behandling, bedömning av prognos och riskgruppsindelning.
Prognosen vid prostatacancer är beroende av cancerns utbredning, som korrelerar till stadium och PSA-nivå, och av dess differentieringsgrad, värderad med Gleasonsumma (se avsnitt 4.3 Naturalförlopp). Obehandlad prostatacancer utan påvisad metastasering delas i detta vårdprogram in i fem riskgrupper enligt ovan (se överväganden i avsnitt 8.2 Riskgruppsindelning för prostatacancer utan känd spridning). För att bedöma den individuella patientens prognos och välja lämplig behandlingsmetod måste man dessutom väga samman palpationsfynd, utbredning av Gleasongrad 4–5 i biopsier, PSA-värde, PSA-densitet och utvecklingstakt av PSA. Patientens samsjuklighet och förväntade kvarvarande livstid utan prostatacancern måste naturligtvis också vägas in i behandlingsbeslutet (se nedan). För att utvärdera eventuell nytta av kurativt syftande behandling för patienter med kortare förväntad kvarvarande livslängd jämförs, i en nordisk randomiserad studie (SPCG19), hormonbehandling enbart, med strålbehandling i kombination med hormonbehandling alternativt operation, vid högrisk prostatacancer för män över 75 år. Enheter som behandlar denna patientgrupp har möjlighet att delta i studien och erbjuda sina patienter deltagande.
Bedömning av förväntad kvarvarande livstid
När man ska avgöra om kurativt syftande behandling är motiverad eller inte måste man ta hänsyn till patientens förväntade kvarvarande livstid utan prostatacancern. Den genomsnittliga kvarvarande livstiden för svenska män i olika åldrar går att få från Statistiska centralbyrån (scb.se). Exempelvis lever 75-åriga män i genomsnitt i ytterligare 11 år. Den förväntade kvarvarande livstiden hos en enskild individ är däremot svår att uppskatta. Den är betydligt längre för män utan allvarliga sjukdomar eller riskfaktorer, t.ex. rökning och övervikt med dålig fysisk kondition. Livstiden i den nära släkten ger också en vägledning om en persons förväntade livstid. Åldern får alltså vägas samman med det allmänna hälsotillståndet samt förekomsten av övriga sjukdomar och andra riskfaktorer för död.
Bedömning av prognos inför kurativ behandling
- Skattningsverktyg kan användas som stöd inför behandlingsbeslut både i den kurativa och i den palliativa situationen.
PREDICT Prostate
Det finns ett antal verktyg som kan användas som kliniskt stöd för att optimera behandlingsval och minska risken för både under- och överbehandling för patienter med lokaliserad sjukdom. Flera olika riskgruppsindelningar har presenterats, varav de flesta dock presenterar risk för återfall av sjukdom och inte dödlighet 221 . Verktyget PREDICT Prostate utvärderar långtidsöverlevnaden hos patienter med lokaliserad sjukdom där valet står mellan kurativ och konservativ behandling 222 . Kliniska variabler såsom PSA, Gleason score i biopsier och kliniskt stadium samt samsjuklighet och ålder hos patienten vägs in i modellen som har utvecklats baserat på data från brittiska män 222 . Modellen är validerad på närmare 70 000 patienter som behandlats i Sverige utifrån data från PCBaSe 223 . I denna studie såg man att överensstämmelsen mellan antalet prognostiserade dödsfall och det faktiska antalet efter 15 år var god både totalt och inom varje behandlingsgrupp. Modellen har även utvärderats som del i patientmötet och visat sig kunna underlätta för patienten vid behandlingsbeslut 224 .
I modellen bedöms radikal prostatektomi och strålbehandling som likvärdiga behandlingar. Att notera är att modellen inte tar hänsyn till nyare utredningssteg såsom MRT eller riktade biopsier. Samsjuklighet bedöms genom en fråga avseende sjukhusvistelse under de senaste två åren före diagnos, och ytterligare kartläggning av patientens samsjuklighet kan vara nödvändig inför behandlingsbeslut.
Geriatric-8 (G8)
Det finns flera andra skalor och skattningsverktyg för att screena och värdera åldersassocierad skörhet. Geriatric-8 (G8) har i många studier visat sig vara ett av de mest robusta verktygen, med hög sensitivitet och acceptabel specificitet 225 226 . Verktyget består av åtta frågor som rör matintag, viktnedgång, aktivitetsförmåga, mental status, BMI, polyfarmaci, egenbedömd hälsostatus och ålder. En poäng mellan 0 och 17 genereras där poäng ≤ 14 betraktas som avvikande och innebär därmed ökad risk för skörhet hos patienten. Dessa patienter behöver ibland utredas vidare ur ett geriatriskt perspektiv och det kan vara särskilt viktigt att noga överväga behandlingsbeslut.
Se G8 Geriatric Screening Tool.
Det är förstås viktigt att komma ihåg att screeningmetoder ger en överblick över patientens tillstånd och viss vägledning i beslut om behandling.
Behandlingsval vid icke spridd prostatacancer
Patientens inflytande
- Patienten ska informeras om tänkbara behandlingsvinster och biverkningar. Han bör få vårdprogrammets patientinformation om tidig upptäckt prostatacancer (Patientinformation: Tidigt upptäckt prostatacancer), lämpligen som en del av sin vårdplan (Min vårdplan prostatacancer).
- När både kirurgi och strålbehandling kan övervägas bör patienten få träffa både en uroonkolog och en urolog som utför radikal prostatektomi.
- Patientens önskemål ska väga tungt vid valet av behandling.
- Patienten ska informeras om att han har rätt till en ny medicinsk bedömning (second opinion) inom eller utom den egna regionen (patientlagen). Om de önskar en sådan bör behandlande läkare skriva en remiss och bifoga kopior av relevanta journalhandlingar, PAD-utlåtande, blodprovssvar och bilddiagnostik (klinisk praxis).
Bedömning av bäckenorganfunktion inför kurativt syftande behandling
Följande bör värderas och dokumenteras i journalen (ett elektroniskt frågeformulär som bland annat omfattar IPSS finns i IPÖ.
Nedre urinvägar: IPSS och residualurin.
Tarm: Funktion och tidigare anorektala sjukdomar.
Sexuell funktion: Erektionsförmåga och dess betydelse för patienten.
Bedömning av tumörens lokala utbredning
Kategorisering av lokalt tumörstadium (T1–4) baseras enbart på palpation, men MRT och ibland även ultraljud kan också ge viktig information om tumörens lokala utbredning som bör vägas in i behandlingsvalet (se avsnitt 8.3.2 Lokalt stadium (T).
Behandling av prostatacancer med låg och mycket låg risk
Mycket låg risk
- Aktiv monitorering rekommenderas om kurativt syftande behandling skulle kunna bli aktuell senare och inte MRT eller andra faktorer talar för samtidig allvarlig cancer.
- Exspektans med eventuell senare hormonbehandling rekommenderas om förväntad livstid är mindre än 10–15 år (⨁⨁⨁).
- Strålbehandling och radikal prostatektomi bör endast övervägas i undantagsfall.
- Hormonell behandling bör inte användas.
- Aktuella studier: SPCG-17.
Övrig lågriskcancer
- Aktiv monitorering: Män med mer än 10–15 års förväntad kvarvarande livstid bör i första hand rekommenderas aktiv monitorering. Kurativt syftande behandling bör dock övervägas för män med lång förväntad kvarvarande livstid och mycket utbredd cancer med Gleasongrad 3, eftersom många av dessa män har en samtidig, oupptäckt cancer med Gleasongrad 4 183 .
- Strålbehandling och radikal prostatektomi bör diskuteras som alternativ till aktiv monitorering.
- Exspektans med eventuell senare hormonbehandling rekommenderas för män med mindre än 10–15 års förväntad kvarvarande livstid (⊕⊕⊕).
- Hormonell behandling bör inte användas.
- Aktuella studier: SPCG-17.
Behandling av mellanriskcancer
Gynnsam mellanrisk
- Strålbehandling eller radikal prostatektomi rekommenderas vid mer än 10–15 års förväntad kvarvarande livstid (⊕⊕⊕).
- Exspektans med eventuell senare hormonbehandling vid påtaglig progress rekommenderas vid mindre än 10–15 års förväntad kvarvarande livstid (⊕⊕⊕).
- Primär hormonell behandling bör inte användas.
- Aktiv monitorering kan rekommenderas i många fall av gynnsam mellanriskcancer, framför allt vid mindre mängd Gleasongrad 4 i frånvaro av andra prognostiskt ogynnsamma faktorer (palpabel eller synlig tumör, hög PSA-densitet, kribriforma mönster och intraduktal cancer). Aktiv monitorering är också aktuellt om det är oklart om kurativt syftande behandling är motiverad eller inte, t.ex. vid förväntad kvarvarande livstid omkring 10–15 år.
- Aktuella studier: SPCG-17 och PRIS.
Ogynnsam mellanrisk
- Strålbehandling eller radikal prostatektomi rekommenderas vid mer än 10–15 års förväntad kvarvarande livstid (⊕⊕⊕).
- Exspektans med eventuell senare hormonbehandling vid påtaglig progress rekommenderas vid mindre än 10–15 års förväntad kvarvarande livstid (⊕⊕⊕).
- Primär hormonell behandling bör inte användas.
Behandling av högriskcancer
- MDK: Handläggningen bör diskuteras på MDK om patienten bedöms ha mer än 5 års förväntad kvarvarande livstid. Kurativt syftande behandling är främst motiverad för män med mer än omkring 10 års förväntad kvarvarande livstid.
- T1–2: Strålbehandling i kombination med hormonbehandling och radikal prostatektomi bedöms vara likvärdiga på gruppnivå (⊕⊕). Individuella faktorer bör styra valet mellan dem.
- T3: Strålbehandling i kombination med hormonbehandling (⊕⊕⊕) rekommenderas, alternativt inklusion i SPCG-15.
- Primär hormonell behandling rekommenderas för patienter med mer än 5 års förväntad kvarvarande livstid som inte är aktuella för kurativt syftande behandling, samt för dem med kortare förväntad kvarvarande livstid som har symtom av cancern.
- Exspektans med eventuell senare hormonbehandling rekommenderas för symtomfria män med mindre än 5 års förväntad kvarvarande livstid.
- Aktiv monitorering rekommenderas inte.
- Aktuella studier: SPCG-15.
Behandling av prostatacancer med mycket hög risk
- MDK: Patienter med mer än 5 års förväntad kvarvarande livstid bör diskuteras på en multidisciplinär konferens (⊕⊕).
- T1-T2: Strålbehandling i kombination med hormonbehandling och radikal prostatektomi bedöms vara likvärdiga på gruppnivå (⊕⊕). Individuella faktorer bör styra valet.
- T3: Strålbehandling i kombination med hormonbehandling (⊕⊕⊕) rekommenderas, eller inklusion i SPCG-15, alternativt SPCG 19 om patienten är ≥75 år.
- T4: Strålbehandling i kombination med hormonbehandling (⊕⊕), eller inklusion i SPCG-15 (om tumören bedöms vara operabel).
- N1: Vid begränsad körtelspridning på PSMA-PET-CT kan kurativ strålbehandling mot prostata och bäckenlymfkörtlar övervägas (+). För behandling vid mer omfattande N1, se avsnitt 12.1 Oligometastatisk prostatacancer (inklusive cN1M0). Hormonbehandling med kastration och abirateron rekommenderas till samtliga N1 (⊕⊕⊕)
- För undergruppen med minst två av följande riskfaktorer: PSA ≥ 40, T3–T4 och Gleasonsumma 8–10, bör strålbehandling kombineras med hormonbehandling, inklusive 2 års abirateron.
- Primär hormonell behandling rekommenderas för patienter med mer än 5 års förväntad kvarvarande livstid som av något skäl inte är aktuella för kurativt syftande behandling, samt för dem med kortare förväntad kvarvarande livstid som har symtom av cancern.
- Exspektans rekommenderas enbart för symtomfria patienter med mycket kort förväntad kvarvarande livstid.
- Aktiv monitorering rekommenderas inte.
- Aktuella studier: SPCG-15/SPCG-19.
Kirurgi eller strålbehandling?
Den enda randomiserade studie som direkt jämfört strålbehandling (extern) med radikal prostatektomi för patienter med lokaliserad prostatacancer visade ingen skillnad i prostatacancerspecifik dödlighet efter 10 år 227 . Det finns ett stort antal jämförande observationsstudier, men deras resultat har sannolikt påverkats av selektion.
Kategoriseringen av lokalt tumörstadium (T1–4) baseras enbart på palpation. MRT och någon gång även ultraljud kan emellertid också bidra med viktig information om tumörens lokala utbredning. Bilddiagnostiska fynd bör också vägas in i valet mellan operation och strålbehandling, t.ex. om det föreligger utbredd extraprostatisk extension eller tumörväxt i anslutning till den externa sfinktern (se avsnitt 8.3.2 Lokalt stadium (T)).
När man väljer behandlingsmetod ska patientens egna synpunkter väga tungt. En önskan om att undvika biverkningar av neoadjuvant och adjuvant hormonell behandling kan tala för operation. Å andra sidan kanske en primär operation följs av postoperativ strålbehandling med andra biverkningar. Risken för biokemiskt återfall är betydligt högre efter kirurgi än efter högdosrat brakyterapi i kombination med extern strålbehandling och hormonbehandling vid utbredd cancer med Gleasonmönster 5 228 .
Argumentet, att det efter strålbehandling inte skulle gå att operera och att det därmed är ett sämre alternativ, är inte underbyggt. Det finns flera möjligheter till kurativ lokalbehandling (prostatektomi, kryo m.fl.). Därtill läggs ju strålfältet vidare än den kirurgiska resektionsranden. Postoperativ strålbehandling har också nackdelar såsom ökad risk för urinläckage.
En nordisk randomiserad studie (SPCG-15) jämför kirurgi med strålbehandling vid lokalt avancerad prostatacancer. Vi rekommenderar att alla enheter som behandlar denna patientgrupp deltar i studien och att samtliga patienter som kan inkluderas erbjuds deltagande.
Följande tillstånd talar för operation och mot strålbehandling (⊕⊕):
- Anorektala sjukdomar, t.ex. ulcerös kolit och fistulerande Crohns sjukdom (stor risk för försämring och svårbehandlade fistlar).
- Betydande infravesikal obstruktion eller residualurin (svår att behandla efter strålbehandling). Neoadjuvant hormonbehandling minskar vanligen prostatavolymen med 20–40 % och kan därmed till viss del minska obstruktion och residualurin.
- Mycket stor prostatavolym (> 70–90 cm3) som är orsakad av benign prostataförstoring (stor strålvolym ökar risken för biverkningar från urinvägar och ändtarm). Neoadjuvant hormonbehandling minskar vanligen prostatavolymen med 20–40 %.
- Proximal uretrastriktur (även om den är åtgärdad, på grund av hög risk för ny striktur).
- Uttalad neuromuskulär funktionsstörning i de nedre urinvägarna eller uttalade trängningsbesvär av andra orsaker (stor risk för biverkningar som är svårare att behandla efter strålbehandling).
- Låg ålder. Vid extern strålbehandling finns på lång sikt en liten men med tiden ökande risk för sekundär malignitet (omkring 0,5 % efter 10 år i en metaanalys) och andra senbiverkningar 229 I den randomiserade SPCG7 diagnostiserades efter 15 år 3 procentenheter fler män med urinblåsecancer i gruppen som fick primär strålbehandling än i gruppen som enbart fick hormonbehandling. De flesta (85 %) av blåstumörerna var ytliga. Det var ingen skillnad i andelen som diagnostiserades med tjock- eller ändtarmscancer 230 . Risken för sekundär malignitet bör vägas in för patienter med förväntad kvarvarande livstid som är mer än 20 år, särskilt vid låg- och mellanriskcancer eftersom risken då är liten för att patienten ska avlida av sin prostatacancer.
Följande tillstånd talar för strålbehandling och mot operation (⊕⊕):
- Utbredd cancer med stor sannolikhet för extraprostatisk växt, särskilt apikalt, nära sfinktern, kan leda till stor risk för cancer i resektionsranden.
- Anestesirisk (t.ex. lung- och hjärtsjukdom).
- Hög risk för tromboembolism, t.ex. APC-resistens (aktiverat protein C).
- Kraftig bukfetma som försvårar kirurgin och ökar risken för urinläckage.
- Vid glaukom eller nylig näthinneavlossning bör försiktighet iakttagas pga. Trendelenburgläget med tippning 30 ° och därmed påföljande högt tryck. Ögonkonsult preoperativt kan vara klokt. Enstaka fall av synpåverkan i samband med långdragen kirurgi har beskrivits 231 232 .
Behandling av män med lokalt avancerad prostatacancer och betydande residualurin
Inte sällan diagnostiseras en lokalt avancerad, icke metastaserad prostatacancer hos män med betydande residualurin, eller hos män som drabbats av urinstämma och försetts med en kvarkateter (KAD). Förstahandsval för cancerbehandlingen som sådan är en kombination av hormonbehandling och strålbehandling, men samtidig residualurin, urinvägsobstruktion eller KAD kräver särskilda överväganden. Det finns emellertid mycket begränsad evidens för dessa överväganden.
Vårdprogramgruppen föreslår, baserat på svag evidens (⊕⊕, om inget annat anges) och klinisk erfarenhet, följande handläggning:
- Diskussion på MDK för planering av behandlingen.
- Urodynamisk utredning kan vara av värde vid misstanke om underaktiv blåsa eller annan neurogen blåsrubbning, t.ex. för diabetiker.
- Radikal prostatektomi: Om lokalstatus (palpation, TRUL och MRT) talar för att tumören är kirurgiskt resektabel, kan radikal prostatektomi vara lämpligt. Patienten bör informeras om att han sannolikt behöver kompletterande behandling efter operationen.
- Behandling med GnRH-agonist minskar ofta tumörstorleken tillräckligt för att patienter med KAD ska bli kateterfria inom 2–3 månader och därefter kunna få kurativt syftande strålbehandling 233 234 . Prostatavolymen har då vanligen minskat med 20–40 % 235 . Tumören och prostatavolymen kan fortsätta att minska i storlek även efter 3–6 månaders behandling, men reduktionen är då mindre uttalad 233 234 . Behandlingen med GnRH-agonist bör i denna situation kombineras med bikalutamid.
- TURP. Om patienten inte blir kateterfri efter några månaders kombinerad androgen blockad, kan en TURP utföras. Strålbehandling kan påbörjas 1–2 månader senare. Strålbehandling efter TURP är förenat med en måttligt ökad risk för biverkningar från urinvägarna 236 237 238 , medan TURP efter strålbehandling ger en betydande risk för urinläckage och därför bör undvikas 239 . Om det är angeläget att påbörja strålbehandlingen tidigt (Gleasonsumma 9–10), kan TURP planeras snarast möjligt efter insatt total androgen blockad och strålbehandlingen ges 1–2 månader senare.
- Suprapubisk kateter: Patienter med urinretention som inte blir kateterfria efter hormonbehandling eller TURP (eller inte är lämpliga för TURP) bör få en suprapubisk kateter inför strålbehandlingen (⊕). Strålbehandlingen ger oftast tillräcklig reduktion av tumörvolymen för att den suprapubiska katetern ska kunna avvecklas efter några månader, men patienten bör förberedas på att katetern kan bli permanent 240 .
- Ren intermittent kateterisering (RIK) är ett alternativ till suprapubisk kateter. RIK kan dock upplevas som obehaglig eller smärtsam under och strax efter strålbehandling ⊕).
- Strålbehandling kan temporärt öka infravesikal obstruktion. Patienter med aktuell residualurin, KAD eller tidigare kateterbehov bör förberedas på att de kan behöva en suprapubisk kateter under och en kort tid efter strålbehandlingen (⊕). KAD i urinröret under strålbehandlingen kan ge svår akut strålreaktion.
- Om kurativt syftande behandling på grund av ålder eller samsjuklighet inte är uppenbart motiverad, kan man inleda med hormonbehandling i 2–6 månader och därefter ta ställning till valet mellan strålbehandling med kurativ intention, strålbehandling för lokal kontroll eller fortsatt hormonbehandling enbart.
Behandlingsmetoder
Aktiv monitorering
Rekommendationer (⊕⊕ om inget annat anges):
Indikationer:
- Aktiv monitorering bör rekommenderas till de flesta män med lågriskcancer.
- Aktiv monitorering bör dock inte rekommenderas utan särskilda skäl vid PSA-densitet > 0,2 µg/l/cm3, EPE eller vesikelinvasion enligt MRT eller i biopsier, BRCA2-mutation, eller ventral cancer hos män med kontraindikation för MRT. Däremot talar inte perineural invasion som enda riskfaktor emot aktiv monitorering av lågriskcancer.
- Vid mellanriskcancer är aktiv monitorering främst aktuell vid låg PSA-densitet, icke palpabel tumör med litet inslag av Gleasonmönster 4 utan kribriforma mönster eller inslag av intraduktal cancer eller perineural invasion , samt för män med så kort förväntad kvarvarande livstid att kurativt syftande behandling endast skulle vara aktuell vid påtaglig progress.
- Kompletterande utredning bör genomföras inom 2–6 månader.
- Efter riktade biopsier utan systematiska biopsier:
- Områden med PI-RADS 4–5 bör ombiopseras om den diagnostiska biopsin inte säkert är representativ.
- Vid PSA-densitet > 0,2 µg/l/cm3 bör dorsala systematiska biopsier tas och ventrala biopsier övervägas.
- Efter riktade plus systematiska dorsala biopsier:
- Områden med PI-RADS 5 bör ombiopseras. Vid PSA-densitet > 0,3 µg/l/cm3 bör även ventrala biopsier tas.
- Om MRT inte kan utföras, bör ventrala biopsier tas vid PSA-densitet > 0,2 µg/l/cm3 (⊕⊕⊕).
Uppföljning allmänt:
Ansvarig för uppföljningen bör vara en urolog.
- PSA-prov bör tas åtminstone halvårsvis.
- Ett enstaka, oväntat ökat PSA-värde bör inte leda till en ny MRT eller behandling, utan följas upp med ett nytt PSA-prov inom någon månad.
- Palpation bör utföras minst årligen (inte nödvändigt vid mycket låg risk och PI-RADS 1–2) (⊕).
- Risken för metastaserad sjukdom ökar påtagligt om inte uppföljningen följer fastlagda riktlinjer, dvs. s.k. ”passiv monitorering”
MRT under uppföljning bör jämföras med föregående undersökningar enligt PRECISE (⊕).
PRECISE 1 = total regress av lesionen
PRECISE 2 = partiell regress av lesionen
PRECISE 3 = oförändrad lesion
PRECISE 4 = progress av lesion eller nytillkommen lesion PI-RADS 3-5
PRECISE 5 = progress av lesion med misstanke om extraprostatisk växt och/eller tillkomst av metastasmisstänkta lymfknute- och/eller benmärgsmetastaser
a) Uppföljning av cancer med Gleasonsumma 6 och PI-RADS 1–3:
Om PSA-densiteten ökat > 0,05 µg/ml/cm3 sedan föregående MRT bör ny MRT utföras (eller en ny TRUL för ny beräkning av PSA-densitet).
b) Uppföljning cancer med Gleasonsumma 7 och/eller PI-RADS 4–5:
Ny MRT bör utföras minst vartannat år. Om PSA-densiteten ökat > 0,05 µg/ml/cm3 sedan föregående MRT bör en ny utföras även om det inte gått 2 år sedan den föregående.
Biopsier:
- Systematisk biopsi med minst 10 systematiska kolvar bör övervägas med
2–3 års intervall och bör utföras om PSA-densiteten ökat > 0,05 µg/ml/cm3 sedan föregående systematiska biopsi. - Riktade biopsier bör tas från nya lesioner på MRT (PI-RADS 3–5) och från en tidigare biopsiverifierad cancertumör med progress enligt MRT (PRECISE 4–5) om inte direkt behandling bedöms vara motiverad (se nedan), samt vid ökning av PSA-densitet > 0,05 µg/ml/cm3 sedan föregående biopsi – även vid oförändrad lesion (PRECISE 3).
- Undvara biopsier:
- Vid PI-RAD 3–5 kan biopsier undvaras om uppföljande MRT visar minskad eller oförändrad lesion (PRECISE 2–3), PSA-densitet < 0,2 µg/l/cm3 och ökning < 0,05 µg/ml/cm3 sedan föregående biopsi.
Kurativt syftande behandling bör rekommenderas vid:
- biopsifynd med Gleasongrad 5 eller mer än några få millimeter Gleasongrad 4, samt vid extraprostatisk extension av cancern (⊕⊕)
- progress av biopsiverifierad cancertumör (PRECISE 4–5) i kombination med stigande PSA om man bedömer att fortsatt aktiv monitorering skulle vara riskabel även vid beskedligt biopsifynd (⊕)
- önskemål från patienten; vid prostatacancer med mycket låg risk utan tecken på samtidig, mer allvarlig cancer bör mannen dock i första hand få upprepad information om att den påvisade cancern inte är farlig
Övergång till exspektans
- När kurativt syftande behandling vid eventuell progress inte längre bedöms vara aktuell ska detta diskuteras med patienten som därefter bör följas upp med exspektans utan kurativ intention. Detta ska dokumenteras i journalen.
Aktiv monitorering innebär uppföljning av en obehandlad prostatacancer med målsättningen att ge botande behandling vid tecken till en mer allvarlig cancer. Aktiv monitorering bör rekommenderas till de flesta män med lågriskcancer. Aktiv monitorering bör dock inte rekommenderas utan särskilda skäl vid PSA-densitet > 0,2 µg/l/cm3 94 99 , BRCA2-mutation eller ventral cancer hos män med kontraindikation för MRT 94 99, 241 samt EPE eller vesikelinvasion i biopsierna 242 . Däremot innebär perineural invasion utan andra riskfaktorer någon ökad risk för ogynnsam tumör vid radikal prostatektomi 175 243 .
Med modern selektion och monitorering är risken för män med lågriskcancer att inom 10 år drabbas av metastaserad sjukdom under 1 % och risken för död i prostatacancer obefintlig 244 245 . Det finns tre studier med 15 års uppföljning. I den mest strikta lågriskgruppen (John Hopkins) hade 0,1 % metastaser och 0,1 % dött i prostatacancer 245 . I en kanadensisk studie, inkluderande även mellanriskcancer (Gleasonsumma ≤ 3 + 4 = 7 och PSA ≤ 20 µg/l), hade sammanslaget 2,8 % metastaser och 1,5 % dött av prostatacancer 246 . I en studie från Göteborg hade efter 15 år ingen av männen med cancer med mycket låg risk, 6 % av män med övrig låg risk och 10 % av män med mellanriskcancer dött av prostatacancer 247 .
Den randomiserade ASIST-studien mellan systematiska biopsier och MRT med riktade och systematiska biopsier visade tydligt fördelarna med införandet av MRT i aktiv monitorering. De som utförde MRT före första rebiopseringen hade efter 2 år 50 % lägre uppgradering till signifikant cancer och signifikant färre avslut av aktiv monitorering. Detta får tolkas som att det finns evidens för att använda MRT vid start som då väljer ut en mer sann lågriskpopulation. Flera studier har visat värde av MRT även vid uppföljning under aktiv monitorering 248 , men det är oklart hur ofta MRT bör utföras. Biopsier kan undvikas vid PI-RADS 3–5 om nya MRT visar PRECISE 2–3, PSAD < 0,15 µg/l/cm3 och ökning < 0,05 µg/ml/cm3 sedan föregående 249 .
PSA-densitet är starkt associerad med sannolikheten för att påvisa cancer med Gleasonsumma 7 250 251 . Om biopsier enbart påvisat cancer med Gleasonsumma 6 hos en man med hög PSA-densitet bör därför nya biopsier tas inför aktiv monitorering, såväl riktade som systematiska. Om PSA-densiteten är mycket hög (t ex > 0,3 µg/l/cm3) kan det vara motiverat att även täcka in de ventrala delarna av prostatan med systematiska biopsier, för att inte fördröja diagnos av en cancer med hög Gleasonsumma. Om MRT inte kan utföras, bör ventrala biopsier tas vid PSA-densitet > 0,2 µg/l/cm3 252 . Långtidsuppföljning av aktiv monitorering har visat att livskvaliteten för patienter under pågående aktiv monitorering är densamma som för friska män utan prostatacancer 246 253 .
Evidensläget är klart sämre än för aktiv monitorering av mellanriskcancer, inte minst vad gäller indikation för behandling 254 255 . Aktiv monitorering av Gleasonsumma 3 + 4 = 7 med < 5 % Gleason 4, uppvisar vid radikal prostatektomi samma pT-stadium, tumörvolym och mängd insignifikant cancer som efter monitorering av Gleasonsumma 3 + 3 = 6 256 .
En prospektiv randomiserad studie (ProtecT) visade efter 15 års uppföljning mycket låg dödlighet oavsett om patienten randomiserats till strålbehandling (2,9 %), kirurgi (2,2 %) eller monitorering (3,1 %) 227 . Monitoreringen var inte speciellt aktiv: endast PSA-prov, utan biopsier och MRT som i modern aktiv monitorering 227 . I en översiktsartikel beskrivs att resultatet på kort och medellång sikt för aktiv monitorering av mellanriskcancer är detsamma som för lågriskcancer, medan resultatet är sämre på längre sikt 257 . Monitorering med MRT och riktade biospier har rapporterats ge lägre andel dödsfall i prostatacancer: 6 % efter 8 år i en kanadensisk kohort 258 och inga efter 10 år i kohort från USA 259 .
Information till patienten. Vid diagnosbesked om lågrisk prostatacancer bör patienten få veta att det som har påvisats i biopsierna inte är farligt. Vid cancer med mycket låg risk bör operation och strålbehandling i normalfallet inte ens diskuteras som alternativ till aktiv monitorering. Däremot bör risken för en oupptäckt, mer allvarlig cancer värderas och diskuteras. Patienten ska få information om vad aktiv monitorering och kurativt syftande behandling innebär.
5-alfareduktashämmare (⊕⊕⊕): Progress av lågriskcancer bromsas av dutasterid 260 , sannolikt även av finasterid. Båda preparaten ökar sensitiviteten för PSA-testning att upptäcka cancer med Gleasonsumma 7–9 261 262 . Vid samtidig benign prostataförstoring kan man därför överväga behandling med 5alfareduktashämmare.
Uppföljning:
PSA-densitet, PI-RADS och indexlesionens storlek vid diagnos är de faktorer som starkast predikterar progression vid aktiv monitorering 249 263 PSA-densitet > 0,15 µg/ml/cm3 är starkare associerat med biopsifynd med Gleasonsumma 7 än tillväxt av lesion på uppföljande MRT 264 . Förändringar över tid av lesioner på MRT bör beskrivas enligt PRECISE 265 som på en skala från 1 till 5 anger utvecklingen av lesionen (se rekommendation ovan).
Indikationer för kurativt syftande behandling: Ju längre patientens förväntade kvarvarande livstid är, desto lägre bör tröskeln vara för att rekommendera kurativt syftande behandling vid fynd av eller tecken på mer allvarlig cancer under monitoreringen. Hos för övrigt friska män under 60 års ålder bör behandling övervägas även vid mycket utbredd Gleasongrad 3, eftersom sannolikheten är stor för oupptäckt Gleasongrad 4 183 . Omvänt kan aktiv monitorering fortsättas även vid nya fynd av Gleasongrad 4 hos män med omkring 10–15 års förväntad kvarvarande livstid. Kurativt syftande behandling bör rekommenderas vid biopsifynd med Gleasongrad 5 eller mer än några få millimeter Gleasongrad 4, eller extraprostatisk extension 241 , vid progress av biopsiverifierad cancertumör (PRECISE 4–5) i kombination med stigande PSA, samt om man bedömer att fortsatt aktiv monitorering skulle vara riskabel även vid beskedligt biopsifynd. Även patientens önskemål spelar naturligtvis in. Vid prostatacancer med mycket låg risk utan tecken på samtidig, mer allvarlig cancer bör mannen dock i första hand få upprepad information om att den påvisade cancern inte är farlig.
Exspektans
Rekommendationer (⊕⊕, om inget annat anges):
- Ansvarig för uppföljningen bör vara en urolog, men kontrollerna kan i många fall utföras av en sjuksköterska vid en urologisk enhet. I vissa fall kan uppföljning i primärvården vara lämpligare, t.ex. vid svår samsjuklighet eller av geografiska skäl. Samråd bör då ske mellan primärvård och närmaste urologiska enhet om åtgärdsgränser och symptom.
- Målet med uppföljningen är att upptäcka lokal progress och metastasering innan sjukdomen ger symtom, så att hormonell behandling då kan påbörjas.
- Uppföljningen bör individualiseras och planeras i samråd med patienten. Vi rekommenderar PSA-prov halvårsvis och palpation årligen för patienter med en palpabel tumör och förväntad kvarvarande livstid mer än 5 år.
- Symtomfria patienter med en icke palpabel lågriskcancer och stabilt PSA-värde, liksom patienter med kortare förväntad kvarvarande livstid än 5 år, behöver inte palperas (⊕). Även dessa män bör erbjudas telefonkontakt med en läkare eller en sjuksköterska med högst 12 månaders intervall.
- Män med en icke palpabel lågriskcancer som följts med expektans utan progress under 10 år, och som har en kort förväntad livslängd (< 3–5 år) kan, efter överenskommelse med patienten, avslutas från uppföljning (⊕). I vissa fall kan uppföljning via primärvården med enbart årliga PSA-prov vara ett alternativ. En specifik gräns bör då anges för PSA, över vilken patienten bör återremitteras till urolog.
Exspektans (engelska: ”watchful waiting”) definieras som uppföljning av obehandlad prostatacancer när kurativt syftande behandling inte bedöms vara aktuell vid senare progress. Orsaken till att man väljer exspektans istället för aktiv monitorering är vanligen att mannens ålder eller samsjuklighet gör det mycket osannolikt att cancern ska hinna utvecklas till en livshotande sjukdom innan mannen dör av någon annan orsak, men en del män väljer exspektans för att slippa biverkningar av en behandling som kanske inte förlänger deras liv. En svensk genomgång av utfallet av expektans som behandling av män med prostatacancer och < 10 års förväntad livslängd visade på låga risker med behandlingen vad gällde risk för progression till hormonbehandling och kastrationsresistent sjukdom 266 . För män med mer än 10 års förväntad kvarvarande livstid bör istället aktiv monitorering övervägas.
För något årtionde sedan innebar exspektans ofta att man avvaktade med behandling tills cancern orsakade symtom (”symtomstyrd behandling”), men numera finns det god evidens för att tidigt insatt hormonell behandling ger längre överlevnad vid lokalt avancerad sjukdom och vid PSA-värden över 3050 µg/l, redan på några års sikt 267 268 269 . Det finns även evidens för att lokal strålbehandling förlänger livet för män med lokalt avancerad och spridd sjukdom 270 271 272 273 . En svensk observationsstudie har visat att dödligheten i prostatacancer är betydande så sent som 15–20 år efter påbörjad exspektans 274 . Samtliga dessa studier talar för att man bör ha en mer aktiv uppföljning av män i exspektans än tidigare, så att man kan upptäcka en lokal progress (ofta förenad med högre Gleasonsumma) och då överväga hormonell behandling, eventuellt i kombination med lokal strålbehandling.
Radikal prostatektomi
Rekommendationer
- Trombosprofylax (⊕⊕): Vid laparoskopisk, okomplicerad radikal prostatektomi hos patienter utan riskfaktorer är risken för tromboembolism så liten att trombosprofylax inte rekommenderas. Vid tidigare tromboembolism, konstaterad trombosbenägenhet (APC-resistens), multipla andra riskfaktorer för tromboembolism, samtidig lymfkörtelutrymning och öppen radikal prostatektomi bör profylax med lågmolekylärt heparin ges i 4 veckor.
- Infektionsprofylax (⊕⊕): Rutinmässig antibiotikaprofylax rekommenderas inte. Inför operationen bör resultat av en urinsticka eller urinodling bedömas. Vid konstaterad eller förmodad bakteriuri (t.ex. vid blåskateter) bör antibiotikabehandling ges, helst enligt resistensmönster från urinodling. Om det inte finns en färsk negativ urinodling bör antibiotikaprofylax övervägas vid riskfaktorer för infektiösa komplikationer (t.ex. diabetes eller immunsuppression).
- Iliakal lymfkörtelutrymning upp till uretärkorsningen kan övervägas vid cancer med mycket hög risk och vid misstänkt lymfkörtelmetastasering.
Radikal prostatektomi utförs vanligen med robotassisterad laparoskopisk transabdominal teknik. Fördelarna jämfört med öppen operation är minskad blodförlust, mindre risk för blodtransfusion, kortare vårdtid, lägre risk för reoperation och kortare katetertid, men operationstiden är längre och kostnaden högre 275 276 .
Kvalitetsaspekter: Många studier har visat att kirurger och sjukhus som utför ett större antal operationer uppnår bättre funktionella och onkologiska resultat än de som utför få 277 278 279 . I en stor, svensk, prospektiv multicenterstudie (LAPPRO) varierade andelen patienter med urininkontinens efter 2 år från 5 % till 30 % mellan de olika deltagande kirurgerna 278 . Det fanns ett samband mellan hög operationsvolym för kirurgen och lägre andel patienter med urinläckage och erektil dysfunktion efter 2 och 8 år 278 279 , men även mellan kirurger med hög operationsvolym fanns betydande skillnader i dessa utfall 278 . En fortsatt förbättring av kirurgens funktionella resultat har i några studier observerats även efter flera hundra operationer 277 279 . En nylig svensk registerstudie kunde dock inte påvisa något samband mellan operationsvolym och inkontinensrisk 280 . Ovanstående studier visar betydelsen av PROM för kontinuerlig utvärdering av enhetens och de enskilda kirurgernas resultat för kvalitetsutveckling och kontinuerligt lärande.
Nervsparande operationsteknik: Cancerns karaktäristika, och i viss mån patientens preoperativa erektionsförmåga, påverkar beslutet om att använda nervsparande operationsteknik eller inte. Detta bör diskuteras med patienten före operationen. Graden av nervsparande (intrafasciellt-, interfasciellt-, semi- eller inte nervsparande, uni- eller bilateralt) bör anges i operationsberättelsen. De flesta patienter kan erbjudas åtminstone unilateralt nervsparande operation. Nervsparande teknik minskar risken för bestående urinläckage 281 ; det finns därför anledning att göra en nervsparande operation även hos män med nedsatt erektionsförmåga. Vid hög risk för extrakapsulär cancerväxt rekommenderas resektion av den neurovaskulära bunten för att minska risken för att lämna kvar cancer. Om detta görs bilateralt får man räkna med bestående erektionssvikt som inte går att behandla med perorala läkemedel.
Iliakal lymfkörtelutrymning ökar risken för komplikationer och för återinläggning inom 90 dagar 208 209 210 . Fynd av multipla lymfkörtelmetastaser kan påverka handläggningen vid återfall, men ingreppet har sannolikt inget terapeutiskt värde 282. En nylig randomiserad singelcenterstudie som jämförde begränsad mot utvidgad lymfkörtelutrymning kunde påvisa en något minskad (10,5 % vs 8 %) andel fjärrmetastaser till förmån för utvidgad utrymning vid 10årsuppföljning 283 . Fjärrmetastaser var en av flera sekundära effektmått i studien, skillnaden i antal lymfkörtlar mellan grupperna var endast två (12 st vs 14 st) och antalet positiva körtlar överlag var få, och emellan grupperna i stort sett lika, varför man får tolka det hela med försiktighet. Därtill skiljde sig inte den endpoint studien var designad för, dvs andelen biokemiskt recidiv mellan grupperna. PSMA-PET-DT har inte använts i studien. Metodologiskt finns det också en hel del invändningar och studien bedöms inte ändra nuvarande rekommendationer 284 . Då lymfkörtelutrymning således inte har visats förbättra det onkologiska utfallet bör sådan därför, utanför studier, bara göras för stadieindelning av lymfkörtlar 206 207 208 . Om man står i valet mellan att använda lymfkörtelutrymning eller PSMA-PET-DT för stadieindelning bör man också välja det sistnämnda.
Biverkningar: Risken för bestående urinläckage ökar med stigande ålder och om operationen utförs utan nervsparande dissektion (ju högre grad av nervsparande, desto lägre sannolikhet för inkontinens) 281 285 . Den är också högre för män med funktionsrubbningar i de nedre urinvägarna. LAPPRO uppgav 21 % av männen att de hade urininkontinens efter 1 år, definierat som 2 eller fler skydd per dygn 286 ; efter 2 år var andelen 19 % 287 och efter 8 år 28 % 279 . Den högre andelen med inkontinens efter 8 år beror sannolikt delvis på att 30 % av männen då hade fått kompletterande strålbehandling 288 . Medianåldern vid operation var 64 år.
Erektionsförmågan försämras efter kirurgi oavsett metod och utförande. Om operationen utförs med nervsparande teknik, kan funktionen förbättras under några år. Risken för bestående erektil dysfunktion varierar mellan 10 och 100 % beroende på ålder, erektionsförmåga före ingreppet och kirurgisk teknik. I LAPPRO hade något färre män erektil dysfunktion 1 år efter robotassisterad (70 %) än efter öppen operation (75 %)286 .
Risken för tromboembolism är, vid laparoskopisk, okomplicerad radikal prostatektomi hos patienter utan riskfaktorer, väldigt låg. Trombosprofylax rekommenderas därför inte för dessa patienter 289 . Vid tidigare tromboembolism, konstaterad trombosbenägenhet (APC-resistens), multipla andra riskfaktorer för tromboembolism, samtidig lymfkörtelutrymning och öppen radikal prostatektomi bör profylax med lågmolekylärt heparin ges i 4 veckor 289 . Även risken för infektion hos patienter med negativ urinodling och utan andra infektionsriskfaktorer är väldigt låg varför rutinmässig antibiotikaprofylax inte rekommenderas
Primär extern strålbehandling
Rekommendationer
- Dosplanering bör baseras på DT eller MRT efter att metallmarkörer implanterats med antibiotikaprofylax (⊕⊕). MRT bör användas för definition av strålvolymen.
- Vid mellanriskcancer rekommenderas ultrahypofraktionerad behandling med 6,1 Gy i 7 fraktioner (⊕⊕⊕). Måttligt hypofraktionerad behandling med 60 Gy i 20 fraktioner (⊕⊕⊕) kan också övervägas.
- Vid högriskcancer (när enbart extern strålbehandling bedöms vara lämpligare än kombination med brakyterapi) rekommenderas 78 Gy i 39 fraktioner (⊕⊕⊕). Måttligt hypofraktionerad behandling (motsvarande EQD2 78 Gy) kan också övervägas (⊕). Ultrahypofraktionerad behandling med 6,1 Gy i 7 fraktioner kan också användas om det inte bedöms nödvändigt att inkludera sädesblåsor (⊕⊕). Vid båda dessa fall måste risken för ökad frekvens av sena biverkningar beaktas.
- Vid mycket hög risk, när enbart extern strålbehandling bedöms vara lämpligare än kombination med brakyterapi, rekommenderas 78 Gy i 39 fraktioner (⊕⊕⊕). Måttligt hypofraktionerad behandling (motsvarande EQD2 78 Gy) kan också övervägas (⊕). Vid T4 kan en helhetsbedömning tala för lägre dos (⊕⊕). Vid T3b bör sädesblåsorna inkluderas i strålvolymen (⊕⊕).
- Extern strålbehandling med fokal boost kan övervägas som alternativ till brakyterapiboost vid cancer med hög eller mycket risk och en korresponderande lesion på MRT (⊕⊕⊕).
- Prerektal spacer kan övervägas för patienter med ökad risk för rektala biverkningar (⊕⊕⊕), inom ramen för ett kontrollerat införande med noggrann uppföljning av resultat och biverkningar via INCA-plattformen (PROM).
- Samtidig strålbehandling mot bäckenlymfkörtlarna (50 Gy i 25 fraktioner) kan övervägas för män med cancer kategoriserad som hög eller mycket hög risk utan påvisade regionala lymfkörtelmetastaser, i första hand utrett med PSMA-PET-DT (⊕⊕⊕). Vid fynd av PSMA-PET-positiva bäckenlymfkörtlar har strålbehandling av bäckenlymfkörtlarna oklart evidensläge men kan övervägas om det bara är ett fåtal (⊕). Det saknas i nuläget evidens för behandling av regionala lymfkörtlar med hypofraktionering.
Beroende på tumörens riskklassificering och N/M-stadium rekommenderas olika former av strålbehandling och fraktionering. I tabell 4 redovisas en sammanfattning av rekommenderad typ av strålbehandling och fraktionering i förhållande till riskgrupp och N/M-stadium.
Tabell 4.Sammanfattning av rekommenderad typ av strålbehandling i förhållande till riskgrupp och N/M-stadie.
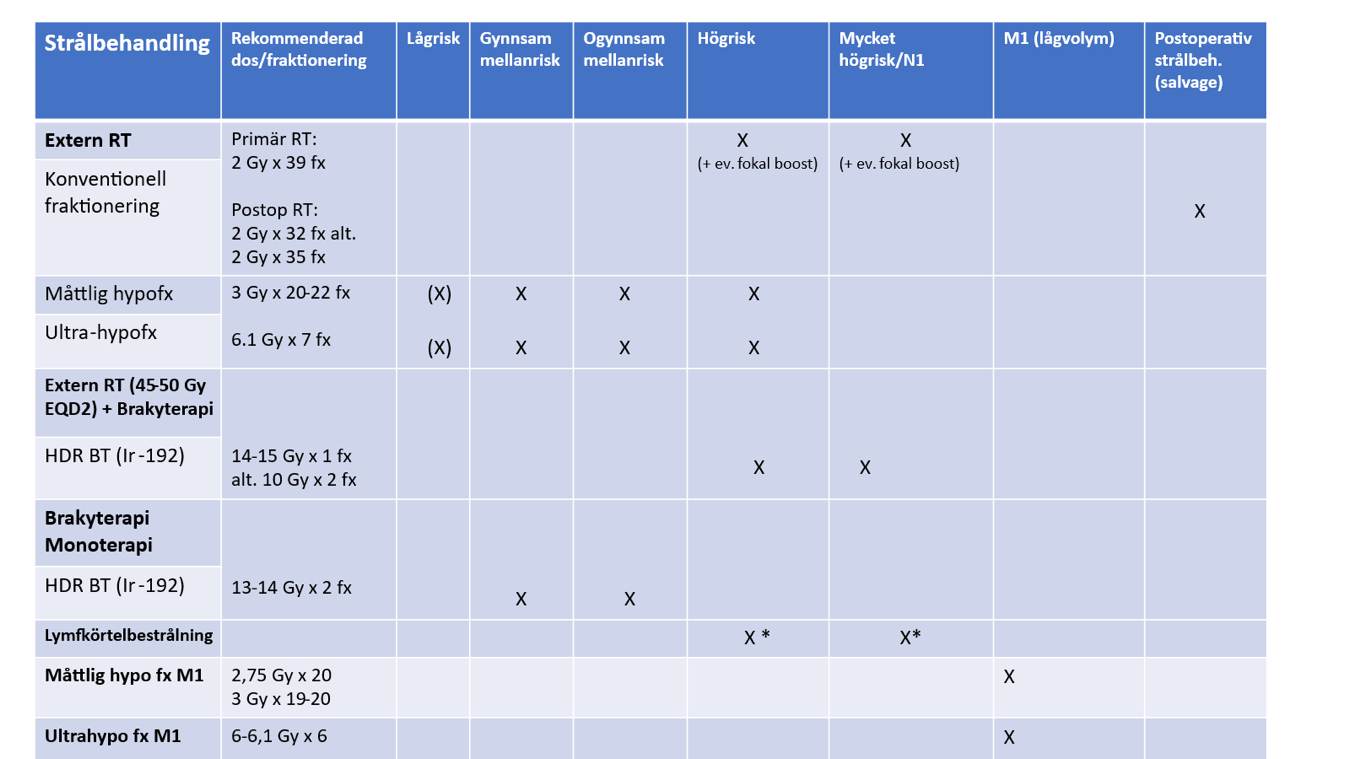
*I POP-RT-studien inkluderades patienter med ≥20 % risk för lymfkörtelinvasion enligt Roach nomogram(2/3xPSA+(Gleasonsumma-6)x10). Medianrisken var dock 38 % och närmare hälften hade risk på över 40 %. För ytterligare detaljer se kapitlet om lymfkörtelbestrålning.
Fyra randomiserade studier har visat att strålbehandling mot primärtumören som tillägg till hormonbehandling minskar dödligheten vid högriskcancer (huvudsakligen T3, en mindre andel T2 och T4) 270 271 272 . Stråldosen som gavs i dessa studier (66-70 Gy) var lägre än dagens standard (> 78 Gy). Extern strålbehandling med doseskalering från nivåerna i dessa studier har i flera randomiserade studier 290 291 292 293 visats ge förbättrad biokemisk/lokal kontroll samt minskad risk för metastasering och prostatacancerspecifik död men ingen totalöverlevnadsvinst har ännu påvisats. Behandlingsbetingad toxicitet var i dessa studier också något ökad vid doseskalerad behandling.
Studierna omfattade några män med T4-tumör, men resultaten för dem har inte redovisats separat. Eftersom andra studier visat att strålbehandling mot primärtumören förlänger överlevnaden vid fjärrmetastaserad sjukdom, oavsett T-stadium 294 295 , förlänger strålbehandling mot primärtumören sannolikt överlevnaden även för män med T4 N0/N1.
Måttlig hypofraktionering med 2,5–3,4 Gy per fraktion (en dos varje vardag i 4–5 veckor) har i flera randomiserade studier visats ha lika god effekt och ge samma grad av biverkningar som standardbehandlingen 78 Gy i 39 fraktioner för män med mellanriskcancer (en liten andel av männen i studierna hade högriskcancer) 296 297 298 299 300 .
Ultrahypofraktionering med 42,7 Gy i 7 fraktioner (en dos varannan vardag under 15–17 dagar) gav i en stor, randomiserad, skandinavisk studie samma effekt och biverkningar efter 5 år för män med mellanriskcancer (en liten andel hade högriskcancer) som 78 Gy i 39 fraktioner 301 . Neoadjuvant eller adjuvant hormonbehandling gavs inte i studien. Ytterligare en stor randomiserad studie på framför allt mellanriskcancerpatienter visade att 36,25 Gy i 5 fraktioner gav lika goda onkologiska resultat efter 5 år som konventionell eller milt hypofraktionerad behandling till priset av något högre frekvens av urinvägsbesvär (26,9 % vs 18,3 % kumulativ incidens av ≥ grad 2 urinvägsbesvär) 302 .
Således finns god evidens för måttlig hypofraktionering och ultrahypofraktionering vid mellanriskcancer och måttlig evidens vid högriskcancer.
Fokal boost mot tumören: I en randomiserad studie (FLAME) 303 var andelen som fick biokemiskt återfall inom 5 år lägre hos män med huvudsakligen högriskcancer som fått en fokal boost mot tumören (definierad med MRT) upp till 95 Gy givet i fraktioner upp till 2,7 Gy som tillägg till behandling med 77 Gy i 35 fraktioner (8 % jämfört med 15 % utan sådan boost). Andelen som fått metastaser inom 5 år var något, men inte statistiskt signifikant, lägre. Studien kommer att rapporteras senare med längre uppföljning. Tillägg av fokal boost gav ingen statistiskt signifikant ökning av biverkningar: Andelen med sena urinvägsbiverkningar grad ≥ 2 var 28 % med och 23 % utan boost, och andelen med sena tarmbiverkningar grad ≥ 2 var 13 % med och 12 % utan boost. De deltagande klinikerna fick själva avgöra om sädesblåsorna skulle behandlas och till vilken dos.
Behandling av sädesblåsor: Vid högriskcancer, och särskilt vid mycket hög risk, finns betydande risk för vesikelinvasion (T3b). Därför har man i de flesta studier och i klinisk praxis inkluderat åtminstone de proximala delarna av sädesblåsorna i strålområdet på patienter med hög risk och mycket hög risk, även de utan klinisk misstanke om T3b. Nomogram baserade på stora operationsserier kan användas som stöd 304 305 . MRT-diagnostik ger ytterligare vägledning i om vesikelinvasion föreligger 306 . Specificiteten för misstänkt vesikelinväxt på MRT är i studier hög, över 90 %. Sensitiviteten är dock lägre 189 307 . Således finns risk för falskt negativa resultat. Sannolikt kan man dock avstå vesikelstrålbehandling på högrisktumörer (inte mycket hög risk) med MRT-mässigt låg sannolikhet för vesikelengagemang (SVI på MRT 1–2/5, se avsnitt 8.3.2 Lokalt stadium (T)) och följaktligen erbjuda ultrahypofraktionerad behandling om det i övrigt bedöms vara lämpligt.
Prerektal hydrogel-spacer minskar förekomsten av sena rektala biverkningar (CTCAE grad > 2) upp till 5 år efter extern strålbehandling för lokaliserad prostatacancer 308 309 310 311 . I en metaanalys hade 1,5 % av patienterna som fått prerektal spacer sena rektala biverkningar grad > 2), medan sådana rapporterades för 5,7 % av dem som inte fått spacer (riskkvot 0,23; 95 % KI 0,06–0,99); självskattad tarmfunktion var också bättre hos män som erhållit spacer 308 . Studierna inkluderade patienter med prostatavolym < 80 ml och lokalt stadium T1–2 som inte tidigare fått strålbehandling eller operation i bäckenet. Spacern läggs in transperinealt i lokalbedövning i samband med guldmarkörimplantation, vilket tar omkring 15 minuter extra. Vårdprogramgruppen bedömer att prerektal spacer kan övervägas för patienter med ökad risk för rektala biverkningar (⊕⊕⊕), inom ramen för ett kontrollerat införande med noggrann uppföljning av resultat och biverkningar via INCA-plattformen (PROM).
Inför en kurativt syftande strålbehandling definieras anatomiska strukturer i närheten som riskerar att skadas av behandlingen. Vid prostatabestrålning rör det sig i första hand om ändtarmen och de nedre urinvägarna enligt ovan. Standardisering av riskorgan inom strålbehandling (STRÅNG) är ett nationellt initiativ som skapar konsensusdefinitioner av riskorgan vid strålbehandling. Riktlinjer för DT och MR-baserad definition av prostatatarget samt riskorgan publicerades av ESTRO (European Society for Radiotherapy and oncology) senast 2018 312 . År 2021 publicerades också riktlinjer från National Radiotherapy Group (NRG) för definition av pelvina lymfkörtlar för de fall där adjuvant körtelbestrålning planeras 313 .
Biverkningar av strålbehandling, allmänt: Biverkningar efter strålbehandling delas in i tidiga (inom 6 månader) och sena (efter 6 månader). De tidiga beror på övergående akut inflammation, och de sena på fibros, kronisk inflammation och ischemi med utveckling av patologiska ytliga kärl (telangiektasier), ibland även nekros med fistelbildning. De akuta och sena biverkningarna graderas ofta av den behandlande läkaren från 1 till 5 enligt RTOG:s definitioner. De flesta moderna studier rapporterar också patientrapporterade biverkningar (PROM). Utvecklingen av strålbehandlingstekniken har medfört att andelen som drabbas av sena biverkningar är mindre än förr 314 315 , men jämförelser mellan olika studier försvåras av att olika graderingssystem för biverkningar har använts.
Tidiga biverkningar från nedre urinvägar: Under den senare delen av behandlingen och de följande månaderna får många patienter övergående irritativa besvär, liknande dem vid överaktiv blåsa: ökad tömningsfrekvens, trängande behov av att tömma blåsan och smärta vid urinering. Många går omedelbart och kissar då de känner en trängning eller går ”för säkerhets skull” före olika aktiviteter, för att undvika trängningar och eventuellt läckage senare. Någon grad av patientskattade (PROM) urinvägsbesvär upplevs av 37–46 % av patienterna vid slutet av strålbehandlingen 316 . Måttliga till uttalade biverkningar (RTOG grad > 2) har rapporterats (av läkare) för 23–49 % av patienterna 296 316 . Besvären är vanligen mest uttalade omkring 1 månad efter strålstart. Den akuta strålreaktionen avklingar sedan vanligen inom 3–4 månader. Strålbehandlingen kan tillfälligt öka infravesikal obstruktion. Patienter med residualurin eller tidigare kateterbehov bör därför förberedas på att de kan behöva en suprapubisk kateter under och en kort tid efter strålbehandlingen.
Tidiga biverkningar från ändtarm och analkanal är ofta ökad gasbildning, lösare avföring, plötsliga trängningar till tarmtömning, smärta eller obehag vid tarmtömning, slembildning eller mindre blödning. Symtomen brukar vara som mest intensiva i slutet av strålbehandlingen och de första veckorna därefter, upp till ett par månader efter strålstart. Den akuta strålreaktionen avklingar sedan vanligen inom cirka 3–4 månader. Någon grad av tidiga biverkningar från tarmen har rapporterats av 21–57 % (PROM) av patienterna 316 317 . Måttliga till uttalade läkarrapporterade besvär (RTOG grad > 2) har rapporterats hos 6–38 %296 301 . Akuta patientskattade tarmbesvär har rapporterats av en större andel patienter efter ultrahypofraktionerad (37 %) än efter konventionellt fraktionerad behandling (21 %) 316 . Strålbehandling mot iliakala lymfkörtlar ger ofta övergående lös avföring 318 .
Sena biverkningar från urinvägarna kan yttra sig som trängningsbesvär, minskad blåsvolym och hematuri. Måttliga eller svåra urinvägsbiverkningar är ungefär lika vanliga som ändtarmsbesvär. Behandling med perorala antikoagulantia medför ökad risk för blödning från urinblåsan efter strålbehandlingen, men transfusionskrävande blödning är sällsynt 319 320 .
Sena biverkningar från ändtarmen och analkanalen är ofta av samma typ som de som kan uppkomma i det tidiga skedet. De kan vara en direkt fortsättning av de tidiga besvären eller uppkomma långt senare. Extern strålbehandling med modern teknik ger måttliga sena ändtarmsbesvär hos 10–20 % av patienterna, medan svåra sena ändtarmsbesvär drabbar 1–10 % 296 297 301 . Besvären kan minska över tid. Patientrapporterade tarmbesvär (PROM) efter 5–6 år har i moderna studier visat att 60–91 % av patienterna har inga eller minimala tarmbesvär, medan 3–5 % har måttliga och 1–2 % har uttalade besvär 316 317 . Måttliga till svåra besvär (RTOG grad > 2) med avföringsläckage eller rektala blödningar efter 5–6 år har rapporterats för 1–4 % av patienterna 296 301 . Sena tarmbiverkningar är lika vanliga efter strålbehandling med konventionell fraktionering, måttlig hypofraktionering och ultrahypofraktionering. Risken för sena ändtarmsbiverkningar är lägre om gel eller annan substans injiceras mellan prostata och rektum (”prerectal spacing”, se ovan) 309 . Behandling med perorala antikoagulantia medför ökad risk för blödning från ändtarmen efter strålbehandlingen, men transfusionskrävande blödning är sällsynt 319 320 .
Sena sexuella biverkningar: Successivt tilltagande erektionssvikt har rapporterats hos 20–80 % av patienterna efter strålbehandling 321 322 323 324 . Risken för erektil dysfunktion ökar med åldern och med ökande samsjuklighet, samt efter neoadjuvant och adjuvant hormonbehandling. De flesta yngre patienter med god erektionsförmåga före strålbehandlingen kan behålla erektionsförmågan, medan män med nedsatt förmåga före behandlingen oftast får svår erektionssvikt efter behandlingen.
Brakyterapi: allmänna principer
Brakyterapi innebär att strålkällan placeras mycket nära eller i tumören, i detta fall i prostatakörteln. Tekniken ger en hög stråldos till prostata, medan dosen till omgivande vävnader, rektum och blåsa, kan hållas låg. Den högre biologiska stråldosen till prostata och urinrör ger en mindre ökning av risken för biverkningar från urinröret, än enbart extern strålbehandling till samma dos. Risken för rektala biverkningar är lägre med brakyterapi 325. I Sverige används för närvarande enbart brakyterapi med högdosrat (HDR).
Allmänna förutsättningar för att brakyterapi ska vara en lämplig behandling för prostatacancer:
- IPSS < 20
- prostatabredd ≤ 50 mm
- ingen stor tertiuslob
- ingen utbredd växt i vesiklar (avancerad T3b).
Stor körtelvolym utgör inget absolut hinder för brakyterapi.
En nyligen genomgången omfattande TURP med kvarstående resektionshåla är en relativ kontraindikation.
Genomförande, HDR brakyterapi: Ultraljud i behandlingsposition bör utföras före behandling för att bedöma risken för interferens med pubisbågen eller andra förhållanden som kan ge tekniska problem vid ingreppet. Vid HDR brakyterpi sätts 15–25 nålapplikatorer i prostata via perineum under vägledning av transrektalt ultraljud. Nålarna förs in genom en matris enligt en specificerad plan. Läget kan kontrolleras med röntgengenomlysning eller MRT. En individuell dosplan utarbetas baserat på applikatorernas position i prostata och förhållande till riskorgan. Med en fjärrstyrd efterladdningsutrustning förs därefter iridium-192 in prostatakörteln under 10–20 minuter. Behandlingen utförs i spinalanestesi eller narkos och tar 2–3 timmar.
Lågdosrat brakyterapi som singelbehandling
Rekommendation
- Lågdosrat (LDR) brakyterapi tillhandahålles för närvarande inte i Sverige, men skulle kunna övervägas för patienter med lågriskcancer eller mellanriskcancer med begränsad volym och utbredning av Gleasongrad 4, god funktion i de nedre urinvägarna och lämplig prostataanatomi (⊕⊕).
Högdosrat (HDR) brakyterapi som singelbehandling
Rekommendation
- Högdosrat brakyterapi (HDR-BT) som singelbehandling kan vara lämpligt i vissa speciella situationer då ingen av standardmetoderna för kurativt syftande behandling är tillgänglig, t.ex. vid bäckenreservoar efter kolektomi, eller när kirurgi av något skäl inte är lämpligt pga. inflammatorisk tarmsjukdom eller njurtransplantat (⊕).
Vid HDR brakyterpi som singelbehandling används företrädesvis fraktioneringen 10,5 Gy i 3 fraktioner eller 13,5 Gy i 2 fraktioner, vilket biologiskt motsvarar cirka 85 Gy respektive 89 Gy givet med 2 Gy-fraktioner (beräknat med α/β = 3 Gy, lineärkvadratiska modellen).
Singelbehandling med HDR brakyterpi har i flera studier visat låg akut toxicitet och god biokemisk kontroll 326 327 328 329 330 331 332 333 , men randomiserade jämförelser med andra strålbehandlingstekniker saknas. En systematisk översikt med metaanalys av resultaten för drygt 2 000 patienter visade god biokemisk kontroll och biverkningsprofil 333 . En europeisk studie med 448 män med låg- och mellanriskcancer visade efter 6,5 års medianuppföljning 98 % biokemisk kontroll och 4,9 % urinvägsbiverkningar av grad 3 men ingen rektaltoxicitet av grad 3 eller 4 334 . I Örebro har metoden avvänts rutinmässigt sedan 2004 för behandling av låg- och mellanriskcancer 335 .
Kombinerad högdosrat brakyterapi och extern strålbehandling
Rekommendationer
- De allmänna förutsättningarna för brakyterapi gäller även för kombinationsbehandling.
- Kombinerad behandling med högdosrat (HDR) brakyterapi och extern strålbehandling bör övervägas vid cancer med hög och mycket hög risk (⊕⊕).
- Samtidig strålbehandling mot bäckenlymfkörtlarna (50 Gy i 25 fraktioner) kan övervägas för män med cancer kategoriserad som hög eller mycket hög risk utan påvisade regionala lymfkörtelmetastaser med PSMA-PET-DT (⊕⊕⊕) eller med ett fåtal sådana metastaser (⊕).
I Sverige har sedan länge HDR brakyterapi givits till 20 Gy i 2 fraktioner tillsammans med extern behandling till 50 Gy med 25 fraktioner. En retrospektiv studie talar för att 15 Gy HDR brakyterapi givet som 1 fraktion ger likvärdig effekt vid mellanriskcancer efter 5 års uppföljning 336 . Total stråldos med kombinationsbehandlingen motsvarar i biologisk dos cirka 102 Gy givet i fraktioner om 2 Gy (beräknat med α/β = 3 Gy, lineärkvadratiska modellen).
En randomiserad studie av Hoskin 325 visade förbättrad biokemisk kontroll med HDR brakyterapi 8,5 Gy i 2 fraktioner kombinerat med extern behandling 2,75 Gy i 13 fraktioner jämfört med enbart extern med 2,75 Gy i 20 fraktioner. Biverkningarna var lika. Den externa behandlingen studien gavs dock i lägre biologisk dos än vad som rekommenderas i dag, motsvarande 63 Gy givet i fraktioner om 2 Gy. En svensk registerstudie visade lägre risk för död i prostatacancer efter extern strålbehandling kombinerad med HDR brakyterpi än efter enbart extern behandling 337 . Skillnaden var mer uttalad vid högriskcancer och vid lågt differentierad cancer. Flera andra observationsstudier med långtidsuppföljning talar för att effekten av kombinationsbehandling med HDR brakyterpi är åtminstone lika god som av extern strålbehandling, och sannolikt bättre vid högriskcancer 338 339 340 340 342 343 .
Kombinerad lågdosrat brakyterapi och extern strålbehandling
Extern strålbehandling kan också kombineras med lågdosrat (LDR) brakyterapi 322 344 345 , men kombinationen används inte i Sverige.
Strålbehandling med protoner
Protoner har fysikaliska egenskaper som kan ge en mer avgränsad stråle (”Bragg peak”) och därmed spara normalvävnad vid behandling. Flera observationsstudier har gjorts vid prostatacancer, och randomiserade studier pågår som jämför protoner med fotonstrålbehandling. Det finns dock inte underlag med publicerade randomiserade studier som kan påvisa en klinisk behandlingsvinst för protoner 346 . I dagsläget behandlas inte prostatacancer vid Skandionkliniken, Sveriges enda behandlingsenhet för protonstrålbehandling.
Strålbehandling av regionala lymfkörtelstationer
År 2021 presenterades en randomiserad studie (POP-RT) som jämförde lokal strålbehandling mot prostata (68 Gy i 25 fraktioner) med eller utan tillägg av strålbehandling mot bäckenlymfkörtlarna (50 Gy i 25 fraktioner) hos män med prostatacancer kategoriserad som hög eller mycket hög risk och > 20 % beräknad sannolikhet för lymkörtelmetastaser enligt Roach formel; hälften hade > 40 % sannolikhet för lymkörtelmetastaser 347 . Omkring 80 % hade genomgått PSMA-PET-DT och de med positiva fynd exkluderades från studien. Alla fick minst 2 års adjuvant GnRH-agonist. Sjukdomsfri överlevnad efter 5 år var 90 % i gruppen som fick strålbehandling mot bäckenlymfkörtlarna och 77 % hos dem som enbart fick strålbehandling mot primärtumören. Motsvarande andelar som var fria från metastaser var 96 % och 89 %. Det var ingen skillnad i total överlevnad efter en medianuppföljning på 6,5 år. Måttliga till svåra tarmbiverkningar (RTOG grad ≥ 2) var något vanligare hos dem som fick strålbehandling mot bäckenlymfkörtlarna: 8,2 jämfört med 4,5 % (inte statistiskt signifikant). Huvudsakligen lindriga biverkningar har även rapporterats från en stor observationsstudie 348 .
Det är dock oklart om studieresultatet gäller även för patienter som är utredda med konventionella metoder. Vi utreder inte alla högriskpatienter med PSMA-PET-DT.
År 2022 presenterades resultaten från en genomgång av överlevnadsdata från National Cancer Register i USA, om prostatacancerpatienter som genomgått lokal kurativt syftande strålbehandling med eller utan tillägg av strålbehandling mot bäckenlymfkörtlarna 349 . Totalt 28 724 prostatacancerpatienter med ogynnsam mellanrisk eller högriskcancer genomgick standardutredning och fick kurativ syftande strålbehandling under 2008–2015. Av dem fick 53 % strålbehandling enbart mot prostata (15 175 patienter) och 47 % mot prostata och bäckenlymfkörtlarna (13 549 patienter). Risk för lymfkörtelmetastasering beräknades med Memorial Sloan Kettering Cancer Center Nomogram. Studieresultatet talar för överlevnadseffekt av lymfkörtelbestrålning i frånvaro av kliniskt påvisad metastasering.
Tillägg av strålbehandling mot regionala lymfkörtlar förlängde signifikant överlevnaden i patientgruppen med Gleasonsumma 9–10 (HR: 0,87 [0,78–0,98], P = 0,02) och/eller risk för lymfkörtelmetastasering > 10 % (HR: 0,93 [0,87–0,99], P = 0,03). Överlevnadsvinst observerades oberoende av hormonell behandling, stråldos till prostata eller ”lymfkörtelriskscore”.
Dessa ”real world”-data stämmer väl överens med resultatet från POP-RT och stödjer indikation för lymfkörtelbestrålning vid högriskprostatacancer.
Fokal behandling
Rekommendation:
- Fokal behandling rekommenderas inte utanför studieprotokoll.
Fokal behandling innebär att endast en del av prostatan behandlas. Syftet är att minska risken för skador på ändtarm, urinvägar och erektionsnerver, jämfört med kirurgi och strålbehandling. Behandlingen utförs i narkos eller ryggbedövning.
Det finns inga randomiserade studier som jämför fokal behandling med kirurgi eller strålbehandling av mellan- eller högriskcancer. De observationsstudier som har redovisats kan inte ge besked om ifall effekten är likvärdig, inte minst eftersom de flesta har kort uppföljning. Det är också oklart hur uppföljningen ska ske och hur återfall efter fokal behandling ska definieras och behandlas. European Association of Urology bedömer att all fokal behandling är experimentell, eftersom långtidsresultat och studier som gör jämförelser med operation eller strålbehandling saknas. Fokal behandling behöver utvärderas i randomiserade kontrollerade studier för att effektivitet och biverkningsprofil ska kunna bedömas. Frånvaron av säkra hållpunkter för effekten av olika former av fokal behandling har inte hindrat marknadsföring som är riktad direkt till patienter.
Fokal behandling med följande tekniker har rapporterats:
- Högintensivt fokuserat ultraljud (HIFU). En ultraljudsstav förs in via ändtarmen och utvecklar värme som riktas mot tumören, samtidigt som ändtarmens slemhinna kyls med vatten. En stor observationsstudie visade låg risk för sjukdomsprogress, metastaser och död i prostatacancer efter 5 år för män med låg- eller mellanriskcancer. Resultatet efter HIFU för högriskcancer var betydligt sämre 350 . En observationsstudie med fokal HIFU inleddes 2020 på Akademiska sjukhuset i Uppsala. Behandlingen ges till män med en unilateral, lokaliserad prostatacancer (T1c–T2a, 1–2 synliga MRT-lesioner) med Gleasonsumma 7 (3 + 3 och 4 + 4 i utvalda fall) och PSA < 20 µg/l. Lesionen får inte vara belägen > 4 cm från rektalväggen (för att tillräckligt hög temperatur i tumören ska kunna uppnås) eller i apex nära sfinktern (för att undvika urininkontinens). Behandlingen vägleds av bildfusionsteknik och ges med 6–7 mm säkerhetsmarginal utanför den på MRT synliga lesionen.
- Irreversibel elektroporation (IRE) innebär att cancern destrueras av korta strömimpulser med likström som genereras mellan elektroder som är placerade i tumören via perineum. Endast ett fåtal studier med mycket kort uppföljning har publicerats 351 . En randomiserad studie som jämför IRE vid mellanriskcancer med radikal prostatektomi och strålbehandling påbörjades i Stockholm under 2022.
- Kryobehandling utförs genom att nålar placeras i målområdet via perineum. Tumörvävnaden fryser sönder under monitorering av temperaturen i urinröret och ändtarmen. I en systematisk översikt av 11 studier var medianuppföljningstiden endast 26 månader, vilket innebär att resultat för överlevnad saknas 351 .
- Fotodynamisk behandling (PDT) verkar genom att en fotosensibiliserare (ett ämne som gör celler ljuskänsliga) tillförs i tablettform, varefter tumörområdet bestrålas med laserljus via nålar i perineum. Fria syreradikaler bildas som leder till att små näraliggande blodkärl proppas igen, så att cancercellerna dör av syrebrist 352 353 .
- Laserinducerad interstitiell termobehandling (LITT) är en fokal laserbehandling som genererar värme i tumören, så att cancercellerna dör. Värmen överförs via laserfibrer som placeras transperinealt eller transrektalt. Metoden är i tidig utvecklingsfas 354 .
- Radiofrekvensablation (RFA) genererar värme med växelström. Elektroder placeras transperinealt i tumören. Långtidsresultat saknas 351 .
- Brakyterapi, såväl lågdosrat som högdosrat, kan ges fokalt. Långtidsresultat saknas 355 .
Neoadjuvant och adjuvant behandling
Hormonbehandling i samband med kirurgi
Rekommendationer
- Neoadjuvant hormonbehandling bör inte ges inför radikal prostatektomi.
- Adjuvant hormonbehandling bör inte ges efter radikal prostatektomi.
Flera randomiserade studier har utvärderat effekten av hormonell behandling inför radikal prostatektomi 356 . Flera av dem visade att neoadjuvant hormonbehandling vid kliniskt lokaliserad sjukdom minskade andelarna med pT3, pN1 och cancer i resektionsranden, men minskade inte risken för kliniskt återfall efter upp till 7 års uppföljning. Neoadjuvant hormonbehandling försämrar dessutom underlaget för att ta ställning till postoperativ strålbehandling genom att påverka PSA-värdet samt den histologiska bedömningen av extraprostatisk extension, resektionsränder och lymfkörtelmetastasering.
En randomiserad studie har visat ökad sjukdomsfri och total överlevnad med adjuvant kastrationsbehandling jämfört med hormonbehandling vid klinisk progress efter att lymfkörtelmetastasering påvisats vid radikal prostatektomi 357 , men det saknas studier som jämför omedelbar hormonbehandling med hormonbehandling vid stigande PSA. Adjuvant behandling med bikalutamid efter radikal prostatektomi ledde inte till förlängd överlevnad, vid vare sig lokaliserad eller lokalt avancerad sjukdom 358 .
Adjuvant strålbehandling efter radikal prostatektomi
Rekommendationer
- Adjuvant strålbehandling 64–70 Gy i 32–35 fraktioner kan övervägas vid utbredd cancerväxt i resektionsränderna (mer än omkring 10 mm totalt) i frånvaro av påvisad lymfkörtelmetastasering (⊕⊕), särskilt vid cancer med Gleasonmönster 5 i resektionsränderna 359 360 361 362 (⊕). I övriga fall bör patienten rekommenderas observation och ställningstagande till strålbehandling vid ett eventuellt återfall (⊕⊕⊕).
- Adjuvant strålbehandling påbörjas tidigast 3–6 månader efter operationen för att läkningen ska hinna avslutas (⊕). För patienter med betydande urinläckage bör man avvakta ännu längre, medan läckaget minskar (⊕).
- Värdet av att bestråla iliakala lymfkörtelstationer är oklart, men detta kan övervägas inom forskningsprojekt vid hög risk för lymfkörtelmetastasering och om 1–2 metastaser har påvisats (⊕). I sådana fall bör även adjuvant bikalutamid 150 mg ges dagligen efter strålbehandling mot brösten (⊕).
Med adjuvant strålbehandling avses strålbehandling som ges vid hög risk för postoperativt återfall hos patienter med PSA < 0,1 µg/l. Strålbehandling vid postoperativt PSA ≥ 0,1 µg/l och vid senare stigande PSA-värde benämns ”salvage”-strålbehandling. Tekniken är densamma.
Adjuvant strålbehandling 60–64 Gy mot prostatabädden har visats minska risken för lokalt och biokemiskt återfall (stigande PSA-värde) med 20 procentenheter för patienter med cancer i resektionsranden eller pT3, utan påvisad lymfkörtelmetastasering 363 364 365 , särskilt vid cancer med Gleasonmönster 5 i resektionsränderna 359 360 361 362 . Risken för fjärrmetastaser minskade med 10 procentenheter och risken för död i prostatacancer med 8 procentenheter efter 10 år i den av studierna som inkluderat störst andel patienter med negativa prognostiska faktorer. I den av de båda andra studierna som har redovisat uppföljning över 10 år påvisades däremot ingen signifikant skillnad i överlevnad 366 . I denna studie sågs en minskad risk för biokemiskt återfall efter strålbehandling enbart om en central omgranskning av PAD kunde påvisa cancer i resektionsranden, då risken för biokemiskt återfall minskade med 30 procentenheter 367 . Studien visar att bedömningen av radikalitet är svår. Många använder i dag högre dos (70 Gy) än vad som getts i de randomiserade studierna (60–64 Gy), eftersom modern teknik medför bättre precision och därmed mindre behandlad volym och mindre risk för allvarliga biverkningar.
Det är oklart vid hur högt postoperativt PSA-värde sannolikheten för metastatisk sjukdom är så stor att kompletterande, kurativt syftande strålbehandling inte kan anses indicerad. I två av de tre randomiserade studierna hade en tredjedel av patienterna PSA ≥ 0,2 µg/l postoperativt 364 365 368 . Även för dessa minskade postoperativ strålbehandling risken för återfall, men man kan ur studierna inte utläsa hur höga PSA-värden de hade.
En metaanalys av tre randomiserade studier visade ingen fördel för adjuvant behandling jämfört med strålbehandling först vid stigande PSA för patienter med riskfaktorer för återfall (huvudsakligen pT3 och/eller cancer i resektionsranden); däremot behandlades många i onödan i den grupp som fick adjuvant strålbehandling 369 .
De randomiserade studierna inkluderade inte patienter med påvisad lymfkörtelmetastasering. Observationsstudier talar för att patienter med 3–4 eller fler lymfkörtelmetastaser har generaliserad sjukdom 370 371 372 som sannolikt inte kan påverkas av strålbehandling, medan strålbehandling i kombination med hormonell behandling möjligen kan vara av värde vid 1–2 metastaser 373 374 375 (⊕). Värdet av att även strålbehandla de iliakala lymfkörtelstationerna är oklart men det kan övervägas inom forskningsprojekt vid hög risk för lymfkörtelmetastasering 376 377 och om 1–2 metastaser har påvisats (⊕). I sådana fall bör även adjuvant bikalutamid 150 mg ges dagligen efter strålbehandling mot brösten.
Biverkningar: Postoperativ strålbehandling ökar risken för permanent erektionssvikt och för kvarstående urinläckage, medan besvärlig strålproktit och strålcystit är ovanligt. Återfall av anastomosstriktur blir ofta svårbehandlat efter strålbehandling. Flera återfall av anastomosstriktur är därför en relativ kontraindikation. Om de regionala lymfkörtlarna inkluderas i strålfältet får patienterna ofta lös avföring 318 .
Hormonbehandling i samband med strålbehandling
Rekommendationer
- Lågriskcancer och mellanriskcancer utan prognostiskt ogynnsamma faktorer: Ingen hormonbehandling (⊕⊕⊕).
- Mellanriskcancer med prognostiskt ogynnsamma faktorer: 6 månaders behandling med GnRH-agonist och bikalutamid bör påbörjas i samband med start av strålbehandlingen (⊕⊕).
- Cancer med hög risk och mycket hög risk (utom undergrupp nedan): 6 månaders behandling med GnRH-agonist och bikalutamid bör påbörjas direkt efter behandlingsbeslutet. Strålbehandlingen bör planeras utan fördröjning (om inte den tumör- eller prostatakrympande effekten av hormonbehandlingen är viktig). Behandlingen med bikalutamid eller GnRH-agonist bör fortsätta i 2–3 år efter strålbehandlingen* (⊕⊕⊕). Bikalutamid är förstahandsval för den adjuvanta behandlingen på grund av lindrigare biverkningar (⊕⊕).
- Mycket hög risk, här vidare definierad som två av faktorerna T3–T4, PSA > 40 µg/l och Gleasonsumma 8–10 eller begränsad N1-sjukdom: Behandling med abirateron och prednisolon under totalt 2 år och med GnRH-agonist under totalt 3 år (⊕⊕⊕). Behandling med GnRH-agonist och bikalutamid bör påbörjas direkt efter behandlingsbeslutet, och bikalutamid byts mot abirateron och prednisolon efter 1–2 månader. Strålbehandlingen bör planeras utan fördröjning (om inte den tumör- eller prostatakrympande effekten av hormonbehandlingen är viktig). Osteoporosprofylax bör ges under behandlingen med abirateron; därefter bör bentäthetsmätning göras för att utvärdera behovet av fortsatt benstärkande behandling (⊕⊕).
- Effekten av GnRH-agonisten bör kontrolleras med blodprov för testosteron och PSA innan strålbehandlingen påbörjas (⊕⊕).
- För hormonbehandling i samband med salvage strålbehandling, se avsnitt 11.1.2 Strålbehandling.
* Långtidsbehandling med bikalutamid/GnRH-agonist kan avstås i utvalda fall med liten, lokaliserad tumör eller hos patient med mycket samsjuklighet.
Två sekundära analyser av randomiserade studier och två observationsstudier talar för att neoadjuvant och konkomitant hormonbehandling förbättrar kliniskt relevanta utfall, främst vid behandling av mellanriskcancer med prognostiskt ogynnsamma faktorer 378379380 381 . I en av dem 380 definierades prognostiskt ogynnsamma faktorer som antingen två mellanriskkriterier (av T2b–c, Gleasonsumma 7 och PSA 10–20 µg/l) eller Gleasonsumma 4 + 3 = 7 eller mer än hälften av systematiska biopsier med cancer. En mycket liten utbredning av cancer med Gleasonsumma 4 + 3 = 7 och multipla fynd av cancer med Gleasonsumma 3 + 3 = 6 är dock var för sig sannolikt inte tillräckligt prognostiskt ogynnsamt för att motivera hormonbehandling.
En sammanslagen analys av två randomiserade studier omfattande sammanlagt drygt 1 000 patienter med prognostiskt ogynnsam mellanriskcancer eller prognostiskt gynnsam högriskcancer visade att 6 månaders konkomitant och adjuvant kombinerad androgen blockad (2 injektioner 3-månaders GnRH-agonist plus 50 mg bikalutamid dagligen) minskade andelen med fjärrmetastasering efter 15 år jämfört med om samma hormonbehandling gavs neoadjuvant och konkomitant (12 % jämfört med 18 %, riskkvot 1,4; 95 % KI 1,00–1,95) 382 . En senare metaanalys av 12 studier med över 7 000 patienter som samtliga fick upp till sex månaders hormonell behandling bekräftade att adjuvant endokrin behandling gav bättre onkologiska utfall än neoadjuvant (definierat som start tidigare än 2 månader innan strålbehandling). Här sågs även en överlevnadsvinst på 6,2 procentenheter efter 10 års medianuppföljning. Orsaken till skillnaden i utfall mellan grupperna är inte känd. För de patienter som fick kort hormonbehandling men med inklusion av bäckenlymfkörtlar i strålområdet sågs snarare en trend till fördel för neoadjuvant behandling. Detta är dock en patientgrupp som i NVP och internationella riktlinjer rekommenderas förlängd endokrin behandling vilket inte studerades i metaanalysen 383 .
Adjuvant GnRH-agonist eller bikalutamid under 2–3 år efter en strålbehandling förbättrar överlevnaden för patienter med högriskcancer och rekommenderas därför 358 368 384 385 386 . Hormonbehandlingen bör under de 6 första månaderna ges i form av GnRH-agonist tillsammans med peroralt antiandrogen (bikalutamid), eftersom denna kombination har använts i de randomiserade studierna 272 , 356 , 382 , 387 388 389 390 391 . Utfallet var sämre för de patienter som inte fick både peroralt antiandrogen och GnRH-agonist under hela den neoadjuvanta behandlingen 392, 393 . Om adjuvant bikalutamid planeras, kan för enkelhetens skull dosen 150 mg ges från ”flare-profylaxen”, en vecka före injektionen med GnRH-agonist, fram till och under den adjuvanta behandlingen. Bröstbestrålning behövs endast inför singelbehandling med bikalutamid, det vill säga inte vid neoadjuvant behandling tillsammans med GnRH-agonist.
Nyligen redovisade resultat från STAMPEDE visar att totalt 2 års tillägg av abirateron plus prednisolon till 3 års total behandlingstid med GnRH-agonist förbättrade behandlingseffekten vid cancer med mycket hög risk och flera ogynnsamma prognostiska faktorer. Efter 6 år ökade andelen utan påvisad metastasering från 69 % till 82 % och den totala överlevnaden från 77 till 86 % 394 . De patienter som ingick i studien hade lymfkörtelmetastaser (39 %) och/eller minst två av faktorerna T3–4, Gleasonsumma 8–10 och PSA > 40 µg/l. Medianvärdet för PSA var 34 µg/l. De flesta hade Gleasonsumma 8–10 (79 %). Medianåldern var 68 år; tre fjärdedelar var yngre än 73 år. Vårdprogramsgruppen bedömer att den förbättrande effekten av kombinationen abirateron/prednisolon plus GnRH-agonist klart överväger de ökade biverkningarna i förhållande till enbart adjuvant bikalutamid eller GnRH-agonist.
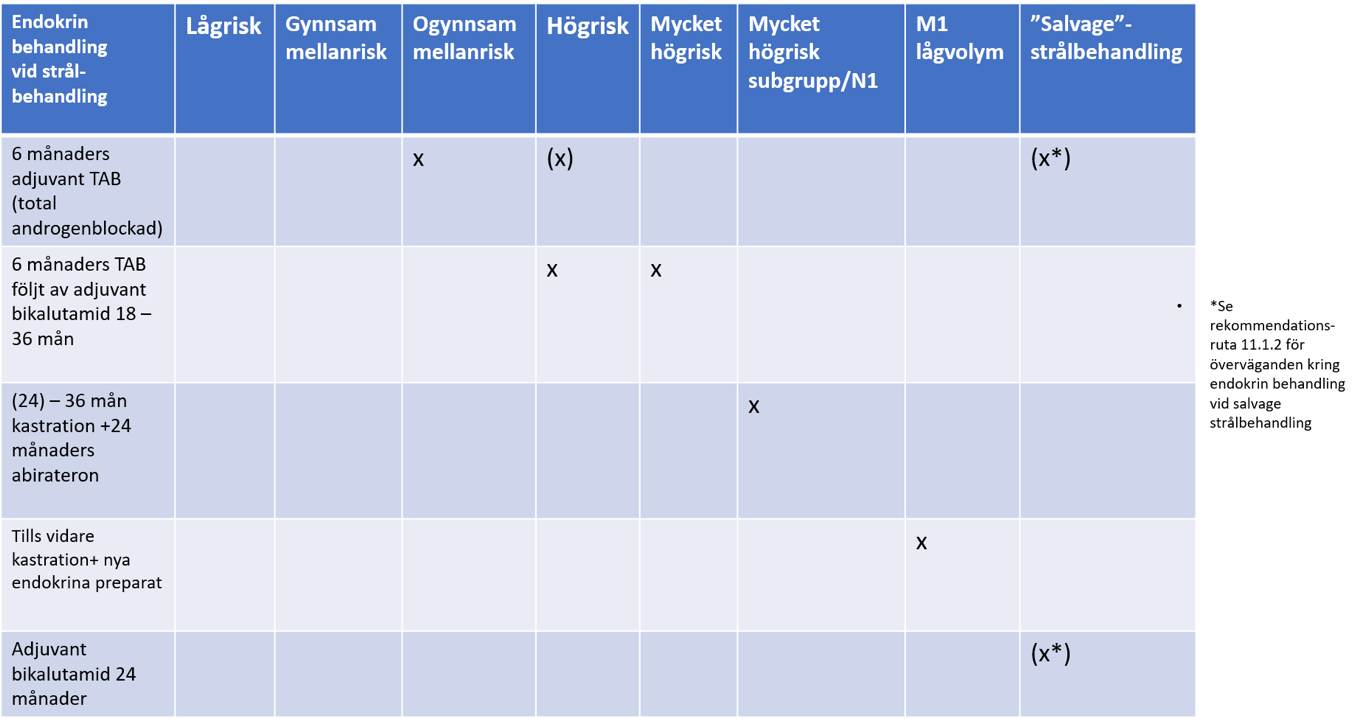
I tabell 5 sammanfattas rekommendationer för neoadjuvant/adjuvant hormonbehandlingsregim vid strålbehandling i förhållande till riskgrupp och N/M-stadie.
Tabell 5.Sammanfattning av rekommendationer för hormonbehandling i samband med strålbehandling i förhållande till riskgrupp och N/M-stadie.
Neoadjuvant och adjuvant behandling med cytostatika
Rekommendationer
- Neoadjuvant eller adjuvant behandling med cytostatika rekommenderas inte (⊕⊕⊕).
Den nordiska randomiserade studien SPCG-12 påvisade ingen effekt av adjuvant docetaxel för män med hög risk för metastatiskt återfall efter radikal prostatektomi 395 .
Två randomiserade studier (SPCG-13 och RTOG 9902) påvisade ingen effekt av att lägga till adjuvant docetaxel eller paklitaxel till neoadjuvant och adjuvant hormonbehandling i samband med extern strålbehandling för män med mellan- eller högriskcancer 396 397 . En annan randomiserad studie (GETUG-12), som enbart inkluderade män med högriskcancer (flertalet med många prognostiskt ogynnsamma faktorer), har efter 9 års medianuppföljning rapporterat något lägre andel med biokemiskt återfall hos patienter som fick tillägg av adjuvant docetaxel och estramustin 398 . En ny rapport med längre uppföljning förväntas inom kort.
Tillägg av adjuvant docetaxel till neoadjuvant och adjuvant hormonbehandling i samband med extern strålbehandling, minskade i en randomiserad studie (RTOG 0521) risken för fjärrmetastaser med 5 procentenheter och risken för återfall med 10 procentenheter efter 6 år för män med högriskcancer (flertalet med flera prognostiskt ogynnsamma faktorer) 399 . Tills vidare talar evidensen för att denna patientgrupp ska erbjudas adjuvant behandling med en kombination av en GnRH-agonist och abirateron plus prednisolon 394 .
En randomiserad studie har rapporterat att neoadjuvant docetaxel (6 cykler med 75 mg/m3) i kombination med GnRH-agonist inför radikal prostatektomi minskade risken för de sekundära effektmåtten metastasering och död hos män med hög risk för återfall 400 . Eftersom så många som en fjärdedel av patienterna fick allvarliga biverkningar, bedömde forskarna bakom studien att behandlingen inte bör användas för rutinbruk; vårdprogramsgruppen delar denna uppfattning.
Annan neoadjuvant och adjuvant behandling
Rekommendationer
- Andra neoadjuvanta och adjuvanta behandlingar bör enbart ges inom ramen för kontrollerade studier.
Primär hormonell behandling vid M0
Rekommendationer
- Låg- och mellanriskcancer bör inte föranleda hormonbehandling (⊕⊕⊕⊕).
- Högriskcancer: I första hand bikalutamid, i andra hand GnRH-agonist/antagonist (⊕⊕⊕⊕). Män med symtom av cancern kan initialt behandlas med GnRH-agonist/antagonist eller kombinerad androgen blockad, för senare byte till bikalutamid (⊕⊕). GnRH-antagonist ger en snabb sänkning av både testosteron- och PSA-värden jämfört med GnRH-agonist. För patienter med genomgången allvarlig kardiovaskulär händelse (tex hjärtinfarkt eller hemorragisk eller ischemisk stroke) kan man överväga GnRH-antagonist vid kastrationsbehandling (⊕⊕). För symtomfria män med mindre än 5 års förväntad kvarvarande livstid är exspektans ett gott alternativ.
- Den initiala behandlingseffekten bör utvärderas med prostatapalpation.
- Kompletterande lokal strålbehandling bör övervägas vid dåligt behandlingssvar och vid senare lokal progress.
Rekommendationer för behandling med enbart bikalutamid
- Symtom som skulle kunna bero på cancern bör medföra prostatapalpation och blodprover, samt och/eller DT buk-torax och/eller skelettskintigrafi snarast möjligt (⊕⊕).
- Vid klinisk progress (symtom som bedöms bero på cancern, palpatorisk progress av primärtumör eller radiologisk progress):
- Byte till GnRH-agonist (bikalutamid ges parallellt i 3 veckor) alternativt GnRH-antagonist(⊕⊕).
- DT buk-torax och skelettskintigrafi (⊕⊕).
- Utvärdering av behandlingseffekt efter 1–3 månader: Blodprover och klinisk bedömning (⊕⊕).
- Vid stigande PSA utan symtom eller radiologisk progress:
- Så länge PSA är < 2 μg/l: Fortsatt behandling med bikalutamid (⊕).
- Vid långsam ökning av PSA > 2 μg/l (dubbleringstid > 10 månader): DT buk-torax och skelettskintigrafi bör utföras då PSA ökat med 5–10 μg/l över det lägsta värdet (⊕). Alternativt byts till GnRH-agonist (bikalutamid ges parallellt i 3 veckor) (⊕). Vid fortsatt behandling med bikalutamid hos patienter med PSA över 5–10 μg/l bör bilddiagnostiken upprepas när PSA ökat med ytterligare 5–10 μg/l (⊕).
- Vid snabb ökning av PSA > 2 μg/l (dubbleringstid < 6 månader): Byte till GnRH-agonist (bikalutamid ges parallellt i 3 veckor) alternativt GnRH-antagonist. Överväg DT buk-torax och skelettskintigrafi (⊕⊕).
- Vid medelsnabb ökning av PSA (dubbleringstid 6–10 månader): Individuell värdering för val mellan ovanstående (⊕).
- Efter byte till GnRH-agonist/antagonist bör behandlingseffekten utvärderas efter 2–3 månader, med blodprover och, vid behov, klinisk bedömning (⊕⊕).
Rekommendationerna baseras i huvudsak på tre stora randomiserade multicenterstudier: EPC 358401, EORTC 402 och MRC 268.
I EPC-studien visades efter 7 års medianuppföljning att bikalutamid förlänger överlevnad och tid till klinisk progress samt minskar risken för metastasrelaterade komplikationer, för män med lokalt avancerad prostatacancer 358. Vid lokaliserad prostatacancer gav däremot bikalutamid något kortare överlevnad. Effekten av behandling med bikalutamid var beroende av PSA-värdet vid randomisering: effekten var negativ vid PSA < 10 µg/l och positiv vid PSA > 30 µg/l401 . I EORTC-studien gav tidig behandling förlängd överlevnad för patienter med en dubbleringstid för PSA < 1 år eller PSA > 50 µg/l 402 . MRC-studien visade liknande resultat 268 .
Sannolikheten för lymfkörtelmetastaser ökar vid höga PSA-värden och hög Gleasonsumma. Lokaliserad högriskcancer har ofta mikrometastaser 203 , så även om en metastasutredning inte påvisar någon spridning kan behandlingsprinciper för lokalt avancerad sjukdom tillämpas. PSA-utvecklingen över tid är en stark prognostisk faktor; en snabb ökning talar för metastasering och tidig hormonell behandling, medan prognosen är betydligt bättre vid en långsam ökning. I det senare fallet är det rimligt att avvakta med behandling även vid höga PSA-värden utan symtom och fjärrmetastaser.
Singelbehandling med antiandrogen (bikalutamid)
Effekt: Bikalutamid hämmar bindning av testosteron vid androgenreceptorn utan att minska testosteronnivån i plasma. Effekten på sjukdomen är likvärdig med den vid kastration vid lokalt avancerad prostatacancer utan fjärrmetastaser, medan medianöverlevnaden vid fjärrmetastasering är 6 veckor kortare vid behandling med bikalutamid än vid kastrationsbehandling 403. För patienter med begränsad, icke-symtomgivande skelettmetastasering är initial behandling med bikalutamid därför ett alternativ till kastration på grund av lindrigare biverkningar. Vid lokaliserad prostatacancer ger behandling med bikalutamid något sämre överlevnad än placebo 404.
Biverkningar: De flesta patienter utvecklar gynekomasti och bröstömhet. Alla patienter bör därför rekommenderas förebyggande bröstbestrålning (12–16 Gy i 1 fraktion) (⊕⊕⊕) 405 406 . Behandlingen med bikalutamid kan påbörjas samma dag som strålbehandlingen ges (⊕⊕⊕). Om det är mycket angeläget att snabbt påbörja behandlingen med bikalutamid, kan den påbörjas någon vecka före strålbehandlingen (⊕). Vid etablerad gynekomasti kan man pröva tamoxifen 20 mg x 1 eller erbjuda en bröstreduktionsplastik 407 408 . Övriga biverkningar, inklusive allvarlig levertoxicitet, är sällsynta. Leverblodprov (ALAT) bör kontrolleras efter 1–3 och 4–6 månader. Singelbehandling med bikalutamid ger inte osteoporos. Sexuell dysfunktion och minskad fysisk och psykisk kapacitet förekommer i betydligt mindre utsträckning än under kastrationsbehandling.
Omvårdnad och rehabilitering i samband med kurativt syftande behandling
Biverkningar
Rekommendationer
- Enheter som utför kurativt syftande behandling bör ha strukturerade rehabiliteringsprogram för biverkningar på sexuell funktion och sexuellt välbefinnande samt från urinvägar, tarm och andra organ. Se även Kapitel 15 Biverkningar: omvårdnad, rehabilitering och behandling.
- Om uppföljningen av en patient med kvarstående rehabiliteringsbehov remitteras till annan enhet än den behandlande, bör den mottagande enheten vara delaktig i rehabiliteringsprogrammet.
Risker för olika biverkningar beskrivs i Min vårdplan prostatacancer och handläggningen av dem i Kapitel 15 Biverkningar: omvårdnad, rehabilitering och behandling.
Rehabiliteringsbehovet bör bedömas återkommande med hjälp av samtal och/eller strukturerade instrument (enkäter). ”Hälsoskattning för cancerrehabilitering” är ett exempel på ett sådant instrument 409 som kan användas som en del i en strukturerad bedömning av patientens problemområden (Bedömning av rehabiliteringsbehov, cancercentrum.se), se Kapitel 15 Biverkningar: omvårdnad, rehabilitering och behandling.
Bäckenbottenträning är viktig för rehabilitering av kontinensen. Alla patienter som genomgår radikal prostatektomi bör få träffa en uroterapeut eller fysioterapeut före och efter behandlingen för information om bäckenbottenträning och träningsinstruktion. Inkontinenshjälpmedel bör anpassas individuellt.
Patienten bör tidigt informeras om sexuell rehabilitering, vilka behandlingar för sexuell dysfunktion som finns att tillgå och om att tidig sexuell aktivitet är bra för återhämtningen. Den sexuella hälsan bör vara ett naturligt inslag i samtalet med läkare och sjuksköterska, och ett sådant samtal ska även kunna erbjudas gemensamt med patientens eventuella partner. Patienten ska kunna diskutera sexualfunktionen vid läkar- och sjuksköterskekontakter och kan erbjudas digitalt program via Stöd och Behandling på 1177. Män som har behov av ytterligare professionell hjälp bör få möjlighet till samtal med en sexologiskt utbildad person.
Information och stöd till patienten
Rekommendationer
- Informationen bör vara både muntlig och skriftlig; patientinformationen som är framtagen i min vårdplan bör användas.
Kontaktsjuksköterskan ansvarar, tillsammans med den behandlande läkaren, för att patienten får information om planerad behandling och om de biverkningar som behandlingen kan medföra. Min vårdplan uppdateras i samråd med patienten. Informationen bör vara både muntlig och skriftlig.
Patienten ska känna till att han har möjlighet att få en ny medicinsk bedömning före behandlingsbeslutet. Patienten bör få rekommendationer om prehabilitering och levnadsvanor. Patienter bör rekommenderas fysisk aktivitet. Patienter som röker bör informeras om att rökning ökar risken för biverkningar och återfall efter behandlingen, samt rekommenderas rökstopp och erbjudas hjälp att sluta röka 410.
Patienten behöver ofta mycket stöd och råd under de första månaderna efter behandling. Kontinuitet och tillgänglighet är viktigt. I detta skede är rehabiliteringsplanen ett viktigt verktyg.
