CAR-T-cellsbehandling vid aggressiva B-cellslymfom
Två CAR-T-cellsbehandlingar, axikabtagen ciloleucel (Yescarta), och lisokabtagen-maraleucel (Breyanzi), rekommenderas av NT-rådet för behandling av diffusa storcelliga B-cellslymfom eller höggradiga B-cellslymfom lymfom i Sverige.
Båda rekommenderas för behandling i andra linjen, för behandling av vuxna patienter med diffust storcelligt B-cellslymfom (DLBCL) och höggradigt B-cellslymfom (HGBL) som recidiverat inom 12 månader efter avslutad, eller är refraktärt till, första linjens kemoimmunterapi 165166. De är även godkända för behandling i tredje linjen eller senare 167168.
De internationella erfarenheterna vid introduktion av CAR-T-celler i sjukvården har i de flesta studier visat effekter i linje med de registreringsgrundande studierna 169170171. I Sverige har vi noterat liknande eller möjligen bättre resultat 172. Alltmer internationell erfarenhet talar dock för att det är av värde att ge behandling för att minska tumörbördan före och/eller efter leukaferes, s.k. bridging, avsnitt 18.3 Bridging-behandling.
Den svenska RCC-CAR-gruppen har regelbundet telemedicin-MDK där alla patienter ska diskuteras.
Kriterier för CAR-T-cellsbehandling
Baserat på inklusionskriterier i studier samt nationella och internationella erfarenheter 173 har nedanstående riktlinjer för behandling med CAR-T utarbetats av den svenska RCC-CAR-gruppen (+).
Till största delen överensstämmer riktlinjerna med inklusionskriterierna i ZUMA-1-studien 174. Ett riktmärke är att allmäntillstånd och organfunktion sammantaget ska motsvara det som man normalt kräver för en autolog transplantation; däremot finns det ingen övre åldersgräns, och nedanstående kriterier bör enbart ses som riktmärken, inte som absoluta kriterier. CAR-T-cellsbehandling ska endast administreras av kvalificerade centrum och föregås av nationell MDK.
OBS! T-cellssupprimerande cytostatikabehandling såsom bendamustin bör undvikas till patienter som övervägs för CAR-T-cellsbehandling. Om bendamustin har getts bör man ha ett intervall på minst 9 månader innan leukaferes ges (+) 175.
Tabell 3. Kriterier för behandling med CAR-T
|
Indikation |
Se ovan, observera att även primärt och sekundärt CNS-lymfom kan behandlas |
|
Hjärtfunktion |
EF > 40 %* |
|
Lungfunktion |
SpO2 ≥ 92 % på luft |
|
ECOG |
0–1 |
|
Infektionsstatus |
Ingen aktiv eller okontrollerad infektion |
|
Neutrofiler |
≥ 1,0 x 109 |
|
Lymfocyter |
> 0,1 x 109 |
|
Trombocyter |
≥ 50 x 109 |
|
Hb |
> 80g/l |
|
Njurfunktion |
GFR ≥ 30 ml/min |
|
Leverfunktion |
ASAT/ALAT < 2,5 x UNL*, bilirubin < 1,5 x UNL** |
* Ingen absolut gräns, patienten allmäntillstånd i helhet bör bedömas.
** UNL = Upper normal limit.
|
Tumörkontroll |
|
|
LD |
≤ 2 x UNL |
|
|
Ej snabbt progredierande sjukdom eller stor tumörbörda |
Remitteringsgång
- Patient bedöms uppfylla kriterier för CAR-T-cellsbehandling.
- Patienten sätts upp på nationell MDK via mail till CARMDK@akademiska.se.
- Fallet diskuteras, och om CAR-T-celler rekommenderas föreslås behandlingsort i första hand på basis av geografisk närhet/regiontillhörighet.
- Ansvarig läkare meddelas och skriver remiss till CAR-T-behandlingssjukhus.
- Patienten kallas för leukaferes.
- Handläggning i väntan på CAR-T-celltillverkning diskuteras (se avsnitt 18.3 Bridging-behandling).
- Lymfodepletion och CAR-T-celler ges på CAR-T-cellssjukhuset.
- Patienten följs upp med avseende på akuta biverkningar.
- Ansvaret överförs till hemsjukhuset då patienten går hem, i samråd med CAR-T-cellssjukhuset (se nedan PM för uppföljning).
- Patienten registreras i EBMT-registret och nationella lymfomregistret av CAR-T-cellssjukhuset.
Bridging-behandling
Mycket talar för att det är fördelaktigt att minska tumörbördan så mycket som möjligt före CAR-T-cellsbehandling. För att åstadkomma detta får patienten s.k. bridging-behandling under tillverkningen av CAR-T-celler. Behandlingen väljs utifrån vad patienten tidigare behandlats med och responderat på. Strålbehandling mot lokaliserad sjukdom är ofta ett bra alternativ 173.
Specifika biverkningar av CAR T-celler
De allvarligaste biverkningarna av CAR‑T-celler är cytokinfrisättningssyndrom (CRS) och neurotoxicitet (immune effector cell associated neurotoxicity syndrome, ICANS) 176.
CRS kommer ofta de första dagarna efter CAR‑T-celler och orsakas av en kraftig immunaktivering. Kardinalsymtomen är feber, hypotension och hypoxi, men alla organsystem kan drabbas. CRS kan ofta behandlas framgångsrikt med anti-IL6‑R-antikroppen tocilizumab (Roactemra) och steroider. En infektion kan driva ett CRS och empirisk infektionsbehandling är ofta nödvändig.
Neurotoxicitet orsakas sannolikt av cytokiner och inträffar någon dag senare än CRS, och kan då ge alla typer av neurologiska symtom. Behandlingen är steroider och neurologisk uppföljning. Dödsfall finns beskrivna för både CRS och ICANS.
En mer ovanlig komplikation till CAR-T-cellsbehandling är hemofagocytisk lymfohistiocytos (HLH), vilket beskrivs närmare i Kapitel 21 Hemofagocyterande lymfohistiocytos (HLH).
Uppföljning och sena biverkningar efter behandling med CAR-T-celler
Rekommendationerna är till stor del hämtade från Hayden et al., European Hematology Association (EHA)/European Society for Blood and Marrow Transplantation (EBMT)/ European Society for Medical Oncology (ESMO) consensus guidelines och Rejeski et al. , och sedan anpassade till svenska förhållanden.
Bakgrund
Patienter som behandlats med CAR-T-celler har efter den akuta fasen risk för återfall i grundsjukdomen och biverkningar i form av infektioner och långdragna cytopenier och infektioner. Långdragna cytopenier efter CAR T-behandling defnieras nu som en egen entitet Immune effector cell–associated hematotoxicity (ICAHT) 177.
Risken för ICAHT
Risken för att utveckla en ICAHT kan bedömas med CAR-Hematotox score baserat på perifera blodvärden tagna före start av lymfodepletion.
Figur 5. CAR-Hematotox score
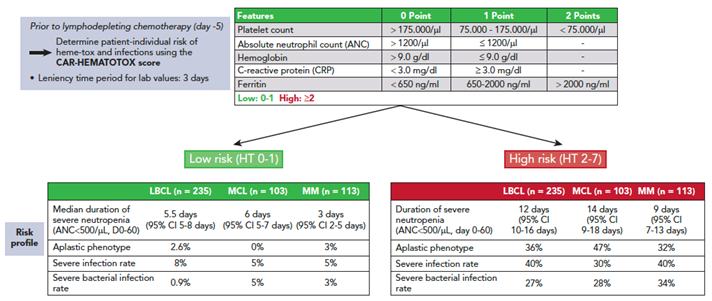
Källa: 177
Patienter som behandlats med CAR T-celler har även en långvarig immunsuppression då persisterande CAR‑T‑celler eliminerar CD19-positiva normala B‑celler (nästan alla B‑celler). Vuxna kan dock ha kvar långlivade plasmaceller som ger ett visst skydd mot infektioner. De flesta patienter är även T‑cellsdefekta med låga nivåer av T‑celler under lång tid, troligen orsakat av lymfodepletionen som ges före CAR-T-celler och/eller immunaktiveringen av CAR‑T-cellerna.
Läkemedelsmyndigheterna kräver uppföljning i 15 år eftersom CAR‑T är nya läkemedel och dessutom klassas som genetiskt modifierad organism (GMO).
Uppföljningsprogram
Uppföljningen anpassas efter kliniskt behov och allvarlig toxicitet, se nedan.
Tabell 4. Uppföljning efter CAR-T-cellsbehandling
|
Åtgärd |
Dag 30–100 |
Månad 3–24 |
År 3–15 |
|
Klinisk kontroll eller telefonkontakt |
Varje månad |
Var 3:e månad |
Varje år |
|
FDG-PET eller DT |
Dag 30 och dag 100 |
Enbart vid klinisk indikation |
Enbart vid klinisk indikation |
|
Blodstatus P-CRP El-status Lever-status Immunglobuliner CAR-T-celler* |
Varje månad |
Varje återbesök |
Varje återbesök |
* CAR-T-celler i blod kan mätas i Stockholm och Lund. Det görs inte rutinmässigt i hela landet ännu. Rekommenderas vid oklar klinisk bild. Ofta avspeglas kvarvarande CAR-T-cellsaktivitet av låga immunglobulinnivåer.
Från utskrivningen till dag 100
Klinisk kontroll och blodprovstagning – besök eller telefon
Vanliga besvär efter CAR-T-cellsbehandling är uttalad trötthet, som är delvis immunologiskt betingad. Även infektioner och cytopenier är vanligt (se nedan).
Utvärdering av behandlingsresultat
- FDG-PET-DT dag 30 (FDG = fludeoxyglukos).
- Radiologi dag 100 enligt lokala rutiner.
- Vid progressiv sjukdom dag 30 eller dag 100 finns i dag inga specifika rekommendationer. CD20-riktade bispecifika antikroppar eller strålbehandling kan övervägas.
Hantering av biverkningar
Patienter kan få sena manifestationer av CRS och ICANS även om det är ovanligt. Dessa behandlas i så fall enligt lokalt PM för akuta biverkningar.
Cytopenier (ICAHT)
Cytopeni definieras som förlängd cytopeni om den kvarstår dag 30. Tillståndet kan drabba en eller flera linjer. Cytopenier är vanliga och oftast associerade med kvarstående immunreaktion och med bättre resultat av CAR-T-cellsbehandlingen.
Obs! Cytopenier kan vara bifasiska, dvs. patienten kan skrivas ut med normala värden, men nivåerna kan senare sjunka i någon eller alla poeser.
Nyligen publicerades riktlinjer för hematologisk toxicitet efter CAR-T-celler 177 där man föreslår termen ”Immune effector cell-associated hematotoxicity”, ICAHT.
Man fokuserar på neutropeni och föreslår nedanstående gradering.
Tabell 5. Gradering av ICAHT
|
Gradering |
1 |
2 |
3 |
4 |
|
Tidig ICAHT (dag 0–30) |
||||
|
ANC ≤ 500/µL |
<7 d |
7–13 d |
≥14 d |
Aldrig över 500/µL |
|
ANC ≤ 100/µL |
- | - | ≥7 d | ≥14 d |
|
Sen ICAHT (efter dag 30) |
||||
|
ANC |
≤1500/µL |
≤1000/µL |
≤500/µL |
≤100/µL |
Källa: 177
Grad 1: Följ varje månad.
Grad 2: Följ var 14:e dag.
Grad 3 följ varje vecka, ge G-CSF.
Grad 4: Följ 2–3 gånger i veckan, ge G-CSF. Överväg infusion av hematopoetiska stamceller om sådana finns tillgängliga. Kontakta CAR-T‑cellscentrum.
Transfusioner
Bestrålade produkter rekommenderas från 14 dagar före CAR-T-cellsbehandling till 3 månader efter för att undvika transfusionsrelaterad cytokinaktivering och graft-versus-host-reaktion. Här kan lokala rekommendationer vara något olika och då tillämpas de lokala.
Infektioner
Infektioner är vanliga efter CAR-T-cellsbehandling, och kan orsakas av både virus och bakterier. Typiskt är bakteriella luftvägsinfektioner.
Vid bakteriell infektion, kontrollera immunglobulinnivåer. Om de är låga (kvarvarande CAR-T-cellaktivitet) föreslås immunglobulin-substitution.
Antibiotikaprofylax
Trimetoprim/sulfametoxazol rekommenderas i 1 år.
Valaciklovir rekommenderas i 1 år.
Vid långdragen neutropeni tillämpas lokala rekommendationer för antibiotikaprofylax.
Vaccinationer
På grund av B-cellsaplasi blir effekten av vaccin sämre hos dessa patienter.
Patienterna rekommenderas dock covid-19-vaccin och influensavaccin. De bör inte vaccineras med levande vaccin.
Fortsatt uppföljning efter dag 100
Patienterna följs upp enligt tabellen ovan. Det är oftast bättre att skjuta på vaccinationer till immunrekonstitution (normala immunglobulinnivåer).
