Bilaga 2. Riktlinjer för volymer och teknik vid strålbehandling av bröstcancer
Version 6
Dokumentet reviderades av styrgruppen för SBRG:
Sara Alkner, Onkolog, Skånes universitetssjukhus Lund
Cecilia Björksund, Dosplanerare, Centrallasarettet Växjö
Maria Hällje, Dosplanerare, Sahlgrenska universitetssjukhuset Göteborg
Sofia Kopf Bäckström, Sjukhusfysiker, Västmanlands sjukhus Västerås
Dan Lundstedt, Onkolog, Sahlgrenska universitetssjukhuset Göteborg
Karin Nygård, Sjukhusfysiker, Akademiska sjukhuset Uppsala
Camilla Wendt, Onkolog, Södersjukhuset Stockholm
2024-11-13
Syfte
Svenska bröstradioterapigruppen (SBRG) arbetar för en ökad kvalitet vid strålbehandling av bröstcancer genom att skapa en gemensam standard och utveckling av riktlinjer för volymer och behandlingstekniker.
Inledning
Primärt är riktlinjerna utarbetade för strålbehandling med fotoner och de omfattar följande:
- Strålbehandling mot bröst eller thoraxvägg
- Partiell bröstbestrålning (PBI)
- Lokoregional strålbehandling efter bröstbevarande kirurgi eller efter mastektomi
Riktlinjerna är ett komplement till det nationella vårdprogrammet och för mer information vid nedanstående frågeställningar hänvisas dit [1].
- Inklusion av regionala körtlar
- PBI
- Fraktioneringsscheman och slutdoser
- Boostdos mot operationsområdet
- Ledtider för strålbehandling
Allmänna överväganden
- Asymptomatiska serom i bröst eller thoraxvägg är inget hinder för strålbehandling.
- Bröstprotes är inte hinder för strålbehandling, men kan på sikt innebära ökad risk för skrumpning eller fibrosbildning [2].
- Expanderprotes med påfyllnadsdosa i metall bör undvikas i strålfälten.
- Samma doskriterier bör användas oavsett val av dosberäkningsalgoritm (ex. Collapsed cone, AAA, Acuros, Montecarlo). Hänsyn kan behöva tas till algoritmens egenheter.
- Andningsstyrd behandling rekommenderas för att reducera dosen till riskorgan. Riktlinjer för andningsanpassad strålbehandling finns i Appendix 1.
- Möjlighet att ge samtidig bilateral behandling får bedömas på individuell nivå med hänsyn till lung- och hjärtdos, eventuell komorbiditet samt allmäntillstånd.
- VMAT och IMRT-tekniker kan övervägas där en acceptabel dosplan inte kan erhållas med konventionella tekniker, antingen i fallet med otillräcklig dos till CTV eller för hög dos till det organ som är i riskzonen. VMAT och i vissa fall IMRT ger en större volym lågdosbestrålning till hjärta, ipsilaterala lungan samt det kontralaterala bröstet och lungan. Det saknas långtidsobservationer efter användning av dessa dynamiska tekniker med hänsyn till risken för sekundär cancer och andra sena biverkningar. Valet att använda sådana tekniker bör därför göras efter en grundlig bedömning av risk/nytta för strålbehandlingsplanen.
- Protonstrålbehandling kan övervägas framför allt vid speciella kliniska fall; t.ex. rebestrålning, skoliosis, pectus excavatum, hjärt/kärl-sjukdom och bilaterala bröstproteser.
Target och riskorgan
Definition av target
Benämning av target följer nationell standard för nomenklatur inom strålbehandling [3]. xx i tabell 1 motsvarar ordinerad dos i Gy [4].
Tabell 1. Benämning och definition av target.
|
Benämning |
Definition |
|
GTV_xx |
Gross Tumor Volume |
|
CTV_xx
|
Clinical Target Volume Den vävnadsvolym man avser att behandla. Eventuellt uppdelat i bröst (CTV_xx) och körtlar (CTVN_xx). |
|
CTVN_xx(IMN) |
Ritas enligt ESTRO guidelines till och med revbensinterstitie 3. |
|
PTV_xx |
Planning Target Volume CTV med lämplig marginal för patientrörelser, teknik och variation i patientpositionering för att garantera att CTV ligger inom behandlat område. |
|
CTVT_xx |
Området där tumören suttit med lämplig marginal, gäller vid bröstbevarande kirurgi. |
|
PTVT_xx |
Planning Target Volume vid boost mot CTVT. CTVT med lämplig marginal för patientrörelser, teknik och variation i patientpositionering för att garantera att CTVT ligger inom behandlat område. |
|
CTV_xx(PBI) |
CTVT med 15 mm marginal inom bröstparenkym (motsvarande CTV för helbröst) [5] |
|
PTV_xx(PBI) |
PTV enligt ovan. |
Figur 1. Exempel med CTVT, PTVT, CTV bröstkörtelvävnad och lymfkörtlar med PTV inritat.
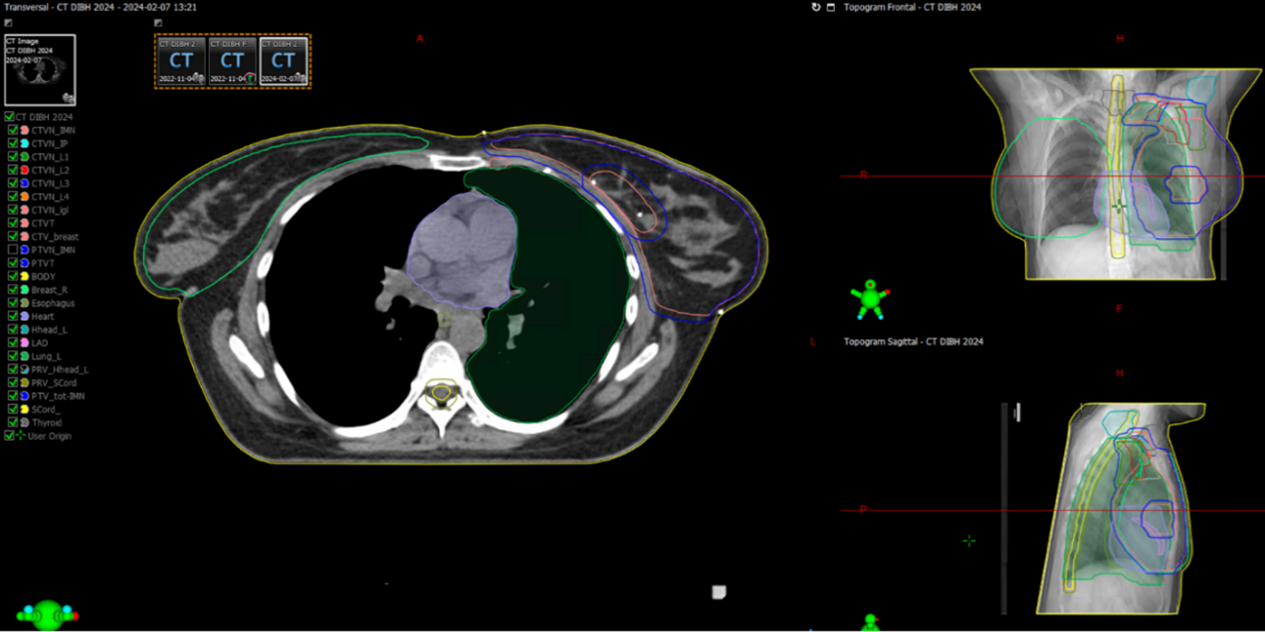
Figur 2. CTV enligt ESTRO consensus guideline [4]. Targetvolymen innehåller all bröstkörtelvävnad. Röntgentät tråd kan användas vid CT-undersökningen för att markera kvarvarande bröst, ärr efter sektorresektion/mastektomi eller området där bröstet suttit efter mastektomi.
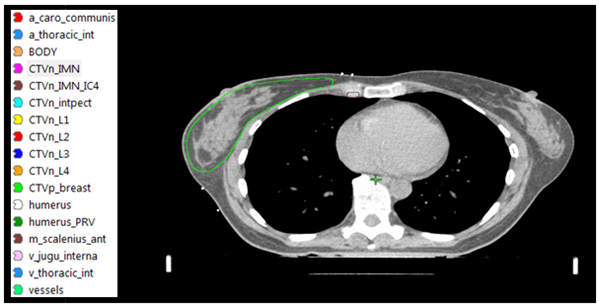
Figur 3. CTVN enligt ESTRO consenus guideline [4]. Inritningen av lymfkörtelvolymerna underlättas genom att vissa landmärken i form av vener och artärer definieras.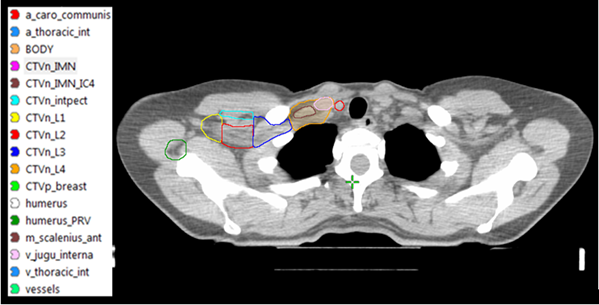
Definition av riskorgan
Benämning av riskorgan följer nationell standard för nomenklatur inom strålbehandling [3]. Följande riskorgan, tabell 2, ritas då det är befogat.
Tabell 2. Benämning och definition av riskorgan.
|
Benämning |
Definition |
|
Heart |
Hjärtat definieras som hjärtats ytterkontur, inklusive de stora kärlen, upp till och med aorta ascendens början där kranskärlsavgångarna finns [6-8] |
|
A_CoronaryD_L |
Vänstra främre kranskärlet ritas om möjligt fr.o.m. avgång från aorta och distalt så långt kärlet kan anas [9]. Diameter ca 6 mm rekommenderas p.g.a. osäkerhet i inritning och för bättre dosberäkning. |
|
Lung_L alt. Lung_R |
Lungvolymen definieras som hela höger respektive vänster lunga, ej hilusstrukturer [10, 11]. |
|
SpinalCord |
Medulla spinalis. |
|
Breast_L alt. Breast_R |
Kontralateralt bröstparenkym indraget 5 mm från huden. |
|
Esophagus |
Esofagus ytterkontur i hela dess längd. |
|
Thyroid |
Tyroideas ytterkontur |
|
HumeralHead_L alt. HumeralHead_R |
Ytterkontur av ipsilateralt humerushuvud |
|
BrachialPlexus_L alt. BrachialPlexus_R |
Plexus brachialis från avgången från medulla så långt nerverna kan visualiseras [12]. |
Förberedelser och verifikation
Uppläggning
Patienten placeras normalt i ryggläge med båda armarna ovan huvudet. Vanligen används en standardiserad bröstbräda med valbara nackkuddar. Vid patienter med stora bröst kan det vara fördelaktigt att använda en vinklingsbar bröstbräda där man vinklar upp överkroppen något och på så sett hindrar bröstet från att falla mot hakan. För att öka reproducerbarheten i patientens längsled kan rumpstopp och en fot- och benfixation med individanpassade inställningar användas.
I vissa fall kan individuell vakuumform användas.
Sträva alltid efter att bröstkorgen får ett bra och reproducerbart behandlingsläge med avseende på patientens anatomi och fysiska förutsättningar.
Figur 4. Exempel på fixationsutrustning. Från vänster: Wing-Step, Monarch, C-Qual Breastboard och ProSTEP.
Datortomografi
CT-undersökning med snittavstånd max 3 mm. Hela lungvolymen ska inkluderas för korrekt beräkning av dos-volymhistogram. Röntgentät tråd kan användas vid CT-undersökningen för att markera kvarvarande bröst, ärr efter sektorresektion/mastektomi eller området där bröstet suttit efter mastektomi.
Bolus
Bolus används vid behov [13]. Om bolus används efter mastektomi kan detta läggas på ärret med 3 cm marginal inom forna bröstområdet.
Verifikation
Kontrollbilder av positionering och fältverifikation för att säkerställa täckning av bröstet tas enligt lokal rutin, dagligen eller enligt särskilt protokoll. Kontroll av positionering kan med fördel kombineras med ett verifierat ytskanningsystem. Operationsclipsen kan användas vid PBI/boost-matchning.
Utvärdering av positionsavvikelser samt dosimetrisk verifikation utförs i enlighet med klinikens gängse rutiner.
Begreppsförklaringar
Dos-volymbegrepp
Exempel:
V105% ≤ 15% Volymen som erhåller en dos ≥ 105% ska vara ≤ 15%.
V16Gy ≤ 20% Volymen som erhåller dosen ≥ 16Gy ska vara ≤ 20%.
Dmedel ≤ 16Gy Medeldos i volymen ska vara ≤ 16Gy.
D98% ≥ 95% Dosen som 98% av volymen erhåller ska vara ≥ 95%. ”Near-minimum dose”.
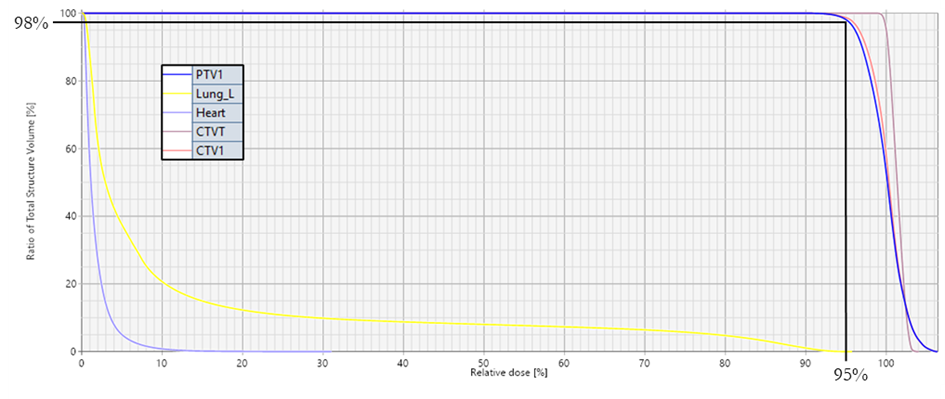
Figur 5. Exempel på dos-volymhistogram. Dostäckningen för target och riskorgan visas. D98% = 95% för PTV är markerat.
Strålbehandling mot bröst
Fraktionering
Primärbehandling
- Hypofraktionering enligt START B [14] 40,05 Gy, 2,67 Gy/dag, 5 dagar/vecka till PTV_40
- Hypofraktionering enligt Fast Forward [15, 16] 26 Gy, 5,2 Gy/dag, 5 dagar/vecka till PTV_26
Boostbehandling
Se nationellt vårdprogram avseende indikation [1]. Boosten ges i första hand som simultant integrerad boost (SIB) men sekventiell boost kan ges som alternativ.
- Högre boostdos:
- SIB: 48,0 Gy, 3,20 Gy/dag, 5 dagar/vecka till PTVT_48 [17]
- Sekventiell boost: 16 Gy, 2 Gy/dag, 5 dagar/vecka till PTVT_56
- Lägre boostdos:
- SIB: 45,75 Gy, 3,05 Gy/dag, 5dagar/vecka [18]
- Sekventiell boost: 10 Gy, 2 Gy/dag, 5 dagar/vecka till PTVT_55.8 Gy
Teknik
Primärbehandling
Behandling med 3DCRT kan ges med två tangentiella fält, se exempel i figur 6 och 7 under fältexempel och beams eye view på dosplaner, samt eventuella tilläggsfält.
Tabell 3. Dosfördelning / prioritetsordning vid behandling mot bröst (40.05Gy/15 fraktioner). Kriterierna gäller även vid boost (summaplan vid sekventiell boost).
|
Prio |
Volym |
Endpoint |
Restriktion |
|
|
1 |
CTVT_xx |
Lokal tumörkontroll |
D99,9% ≥ 95%* Dmedel ≥ 100% |
|
|
CTV_40 |
vid lobulär ≥T2 resp. multifokal cancer |
D98% ≥ 95%* |
||
|
PTV_40 |
D98% ≥ 93%* |
|||
|
2 |
Heart |
Hjärtmorbiditet inom 20 år |
Hjärtdosen ska minimeras** Dmedel < 4Gy (riktvärde 1,6Gy) V17Gy ≤ 5% |
|
|
3 |
Lung_L/R (ipsilateral) |
Pneumonit Lungcancer |
Lungdosen ska minimeras** V16Gy ≤ 20% (riktvärde 10%) Dmedel ≤ 8Gy (riktvärde 4Gy) |
|
|
4 |
CTV_40 |
Lokal tumörkontroll |
D98% ≥ 95%* |
|
|
PTV_40 PTVT_xx |
D98% ≥ 93%* För att reducera dosen till riskorganen (hjärta/lunga) ned mot riktvärden kan D90% ≥ 93% accepteras. Området med lägre dos bör placeras på största möjliga avstånd från CTVT. |
|||
|
5 |
Breast_R/L (kontralateralt) |
Sekundär cancer |
Begränsa dosen, särskilt hos yngre. I vissa fall kan visst överslag accepteras för att reducera dosen till riskorganen ned mot riktvärden. |
|
|
6 |
Body |
|
V108% bör vara ≤ 1cm3 Vid SIB: D0,1cm3 < 108% (% relativt SIB-dos) |
|
PTV-täckning utvärderas för en hjälpvolym som är beskuren 5mm innanför ytterkonturen.
* Undantag ytligt belägen min-dos.
** Observera att rökning ger riskökning [19].
Tabell 4. Dosfördelning/prioritetsordning vid behandling mot bröst/partiellt bröst (26Gy/5 fraktioner)
|
Prio |
Volym |
Endpoint |
Restriktion |
|
| 1 |
CTVT_26 |
Lokal tumörkontroll |
D99,9% ≥ 95%* Dmedel ≥ 100% |
|
|
CTV_26 |
vid lobulär ≥ T2 eller multifokal cancer |
D98% ≥ 95%* |
||
|
PTV_26 |
D98% ≥ 93%* D95% ≥ 95%* |
|||
| 2 |
Heart |
Hjärtmorbiditet inom 20 år |
Hjärtdosen ska minimeras**
V1,3Gy ≤ 25% V6,5Gy ≤ 5% |
|
| 3 |
Lung_L/R (ipsilateral) |
Pneumonit Lungcancer |
Lungdosen ska minimeras** V7,8Gy ≤ 17% (riktvärde 15%) |
|
| 4 |
CTV_26 |
Lokal tumörkontroll |
D98% ≥ 95%* |
|
|
PTV_26 |
D98% ≥ 93% Området med lägre dos än 93% placeras på största möjliga avstånd från CTVT D95% ≥ 95%* (D90% ≥ 95% kan accepteras) V105% ≤ 7% (riktvärde 5%) V107% ≤ 2% Dmax ≤ 110% |
|||
| 5 |
Breast_R/L (kontralateralt) |
Sekundär cancer |
Begränsa dosen |
|
| 6 |
Z_Body – PTV_26 |
|
Dmax ≤ 110% (riktvärde 105%) |
|
I Fast Forward-studien har PTV-täckning utvärderats för en hjälpvolym som är beskuren 5mm innanför ytterkonturen och 5 mm från lungan.
* Undantag ytligt belägen min-dos.
** Observera att rökning ger riskökning [19].
Partiell strålbehandling mot bröst
Partiell bröstbestrålning ges mot tumörbädden, CTVT_xx, med 15mm marginal dvs mot CTV_xx(PBI) enligt Import Low [5]. Vid partiell bröstbestrålning är det av extra vikt att clips finns för att lokalisera CTVT.
Fraktionering
- Hypofraktionering enligt START B [14] 40.05 Gy, 2.67 Gy/dag, 5 dagar/vecka till PTV_40
- Hypofraktionering enligt Fast Forward [15, 16] 26 Gy, 5,2 Gy/dag, 5 dagar/vecka till PTV_26.0
Teknik
Behandling med 3DCRT ges oftast med två tangentiella fält samt eventuella tilläggsfält.
Tabell 5. Dosfördelning/prioritetsordning vid behandling mot partiellt bröst (40.05Gy/15 fraktioner) (OBS! Vid fraktionering 26Gy/5 fraktioner se tabell 4)
|
Prio |
Volym |
Endpoint |
Restriktion |
|
1 |
CTVT_40 |
Lokal tumörkontroll |
D99,9% ≥ 95%* Dmedel ≥ 100% |
|
2 |
Heart |
Hjärtmorbiditet inom 20 år |
Hjärtdosen ska minimeras** Dmedel < 4Gy (riktvärde 1,6Gy) V17Gy ≤ 5% V35Gy ≤ 1% |
|
3 |
Lung_L/R (ipsilateral) |
Pneumonit Lungcancer |
Lungdosen ska minimeras**
V16Gy ≤ 20% (riktvärde 10%) Dmedel ≤ 8Gy (riktvärde 4Gy) |
|
4 |
CTV_40(PBI) |
Lokal tumörkontroll |
D98% ≥ 95%* |
|
5 |
PTV_40(PBI) |
Lokal tumörkontroll |
D98% ≥ 93%* Dmax ≤ 110% V105% < 2cm3 |
|
6 |
Breast_R/L (kontralateralt) |
Sekundär cancer |
Begränsa dosen, särskilt hos yngre. I vissa fall kan visst överslag accepteras för att reducera dosen till riskorganen ned mot riktvärden. |
|
7 |
Body |
|
V108% bör vara < 1cm3 |
PTV-täckning utvärderas för en hjälpvolym som är beskuren 5mm innanför ytterkonturen.
* Undantag ytligt belägen min-dos.
** Observera att rökning ger riskökning [19].
Strålbehandling mot bröst eller bröstkorgsvägg och regionala lymfkörtlar
Fraktionering
Primärbehandling
- Hypofraktionering enligt START B [14] 40,05 Gy, 2,67 Gy/dag, 5 dagar/vecka till PTV_40
Boostbehandling
Se nationellt vårdprogram avseende indikation [1]. Boosten ges i första hand som simultant integrerad boost (SIB) men sekventiell behandling ges som alternativ.
- Högre boostdos:
- SIB: 48,0 Gy, 3,20 Gy/dag, 5 dagar/vecka till PTVT_48 [17].
- Sekventiell boost: 16 Gy, 2 Gy/dag, 5 dagar/vecka till PTVT_56
- Lägre boostdos:
- SIB: 45,75 Gy, 3,05 Gy/dag, 5dagar/vecka [16].
- Sekventiell boost: 10 Gy, 2 Gy/dag, 5 dagar/vecka till PTVT_55.8 Gy
Teknik
Primärbehandling
Behandlingen med 3DCRT kan delas upp i en kraniell och en kaudal del med isocenter i skarven. Behandling mot den kraniella delen kan ges med ett fotonfält snett framifrån (oftast 6MV) och ett närmast motstående, lägre viktat fält med högre energi. Behandling mot den kaudala delen av bröstet/bröstkorgsväggen, kan ges med två tangentiellt ställda strålfält (oftast 6MV) samt eventuella tilläggsfält. Strålfälten anpassas till PTV och riskorgan med lämpligt val av gantryvinkel, kollimatorvinkel och avskärmning. Se exempel i figur 8–11 under fältexempel och beams eye view på dosplaner. För att erhålla låg lungdos bör skarven mellan den kraniella och kaudala delen placeras så kraniellt som möjligt. Risken för heterogen dosfördelning, speciellt underdosering, i skarvområdet ska beaktas. Om VMAT används ska lågdosområden beaktas.
Tabell 6. Dosfördelning/prioritetsordning vid behandling mot bröst eller bröstkorgsvägg och regionala lymfkörtlar (40.05Gy/15 fraktioner). Kriterierna gäller även vid boost (summaplan vid sekventiell boost).
|
Prio |
Volym |
Endpoint |
Restriktion |
|
|
1 |
CTVT_xx |
Lokal tumörkontroll |
D99,9% ≥ 95%* Dmedel ≥ 100% |
|
|
CTV_40 |
vid lobulär >T2 resp. multifokal cancer |
D98% ≥ 95%* |
||
|
PTV_40 |
D98% ≥ 93%* |
|||
|
2 |
Heart |
Hjärtmorbiditet inom 20 år |
Hjärtdosen ska minimeras** Dmedel < 4Gy (riktvärde 1,6Gy) V17Gy ≤ 10% (riktvärde ≤ 5%) |
|
|
3 |
Lung_R/L (ipsilateral) |
Pneumonit Lungcancer |
Lungdosen ska minimeras** V16Gy ≤ 35% (riktvärde 20%) Dmedel ≤ 16Gy (riktvärde 8Gy) V5Gy ≤ 70% (riktvärde 55%)*** |
|
|
Lung_L/R (kontralateral) |
|
Dmedel < 2Gy*** |
||
|
4 |
CTV_40 |
Lokal tumörkontroll |
D98% ≥ 95%* |
|
|
PTV_40 PTVT_xx |
D98% ≥ 93%* V105% ≤ 20% (riktvärde 10%) SIB-dosnivåer ska endast finnas i höjd med PTVT D90% ≥ 93% kan accepteras för att reducera dosen till riskorganen (hjärta/lunga) ned mot riktvärden. Området med lägre dos bör placeras på största möjliga avstånd från CTVT. |
|||
|
5 |
CTVN_40(IMN) |
Lokal tumörkontroll |
D98% ≥ 90% Dosbegränsningar för hjärta samt lunga enligt ovan bör respekteras. Vid behov minskas targettäckning till IMN kaudalt och successivt uppåt tills dessa uppnås. Full dos behöver dock ej eftersträvas i den mest kraniella delen av IMN, bakom sternoklavikularleden. |
|
|
6 |
Breast_R/L (kontralateralt) |
Sekundär cancer |
Dmedel < 4Gy (riktvärde 2Gy) [20]*** Begränsa dosen, särskilt hos yngre. Som riktvärde gå ej mer än 5 cm från medellinjen in i kontralateralt bröst (mäts från mitten på sternum längs ytterkonturen till 50% isodos). |
|
|
7 |
Esophagus |
|
V9Gy < 5cm3 [21]*** V18Gy < 2cm3*** |
|
|
Thyroid |
|
Dmedel < 20Gy (riktvärde 15Gy) [22]*** |
||
|
SpinalCord |
|
D0,1cm3 < 16Gy |
||
|
Body |
|
V110% bör vara < 1cm3 Vid SIB: D0,1cm3 < 108% (% relativt SIB-dos) |
||
|
8 |
HumeralHead_R/L |
|
Begränsa dosen. |
|
PTV-täckning utvärderas för en hjälpvolym som är beskuren 5mm innanför ytterkonturen.
* Undantag ytligt belägen min-dos.
** Observera att rökning ger riskökning [19].
*** Aktuellt vid VMAT- och IMRTdosplaner.
Fältexempel och beams eye view (BEV) på dosplaner
Konventionella planer mot enbart bröst
Figur 6. Exempel på dosplan med tangentiella strålfält.
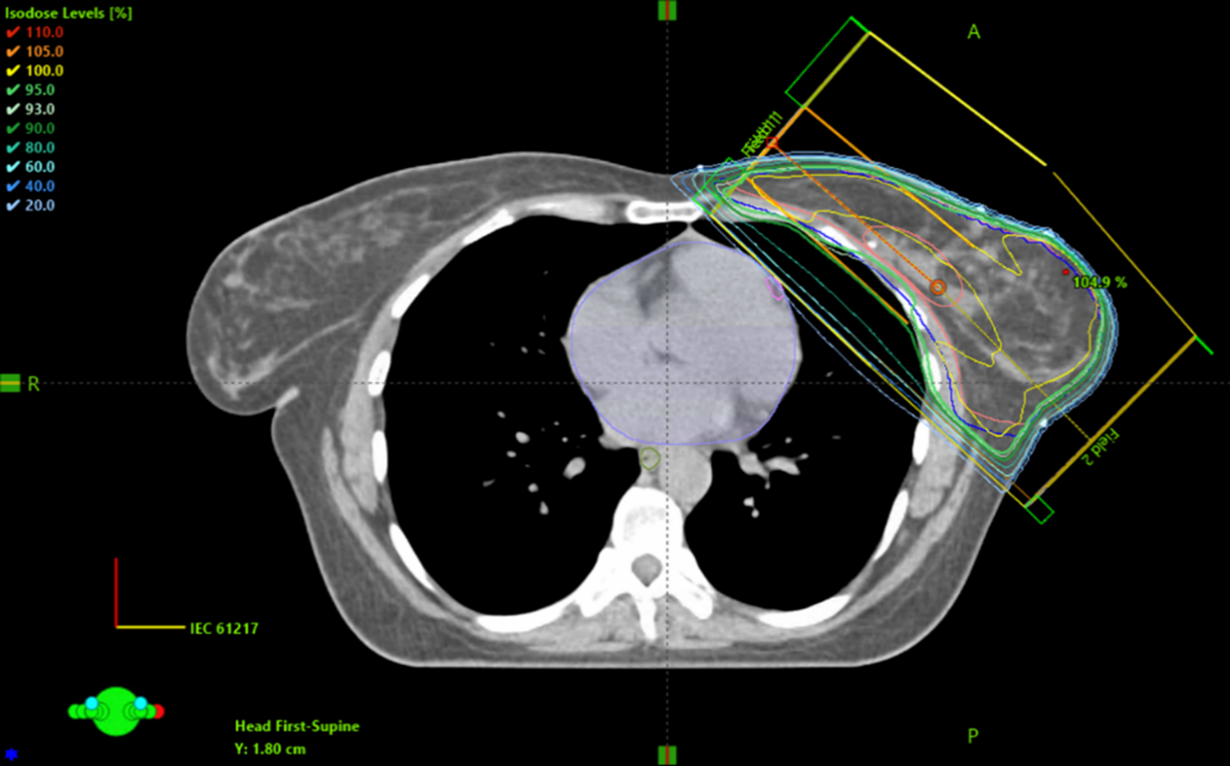
Figur 7. Exempel på BEV för ett tangentiellt strålfält.
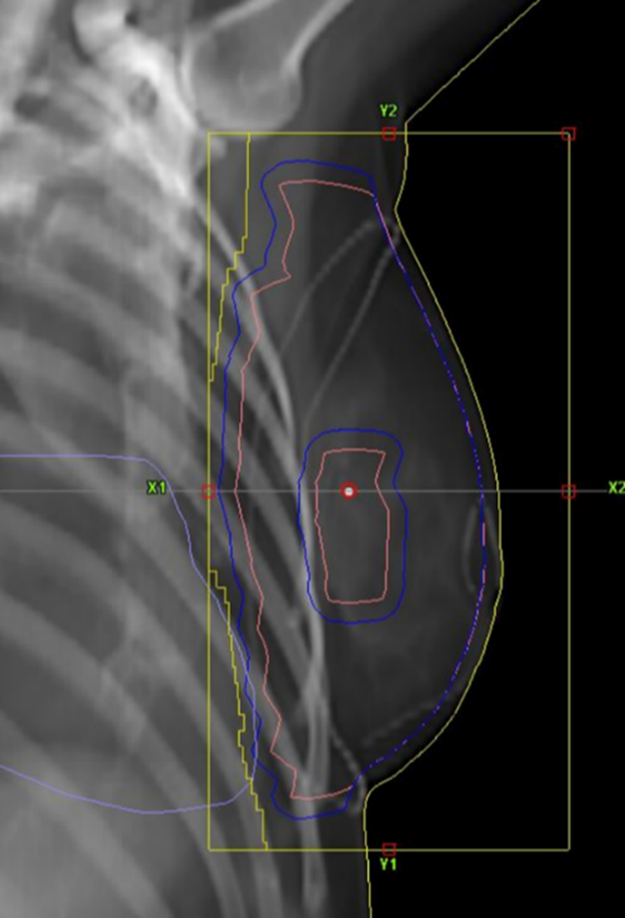
Konventionella planer mot bröst eller bröstkorgsvägg och regionala lymfkörtlar
Figur 8. Exempel som visar placeringen av isocenter och CT-snittet för övergången mellan tangentiella strålfält över brösttarget och strålfälten över körteltarget.
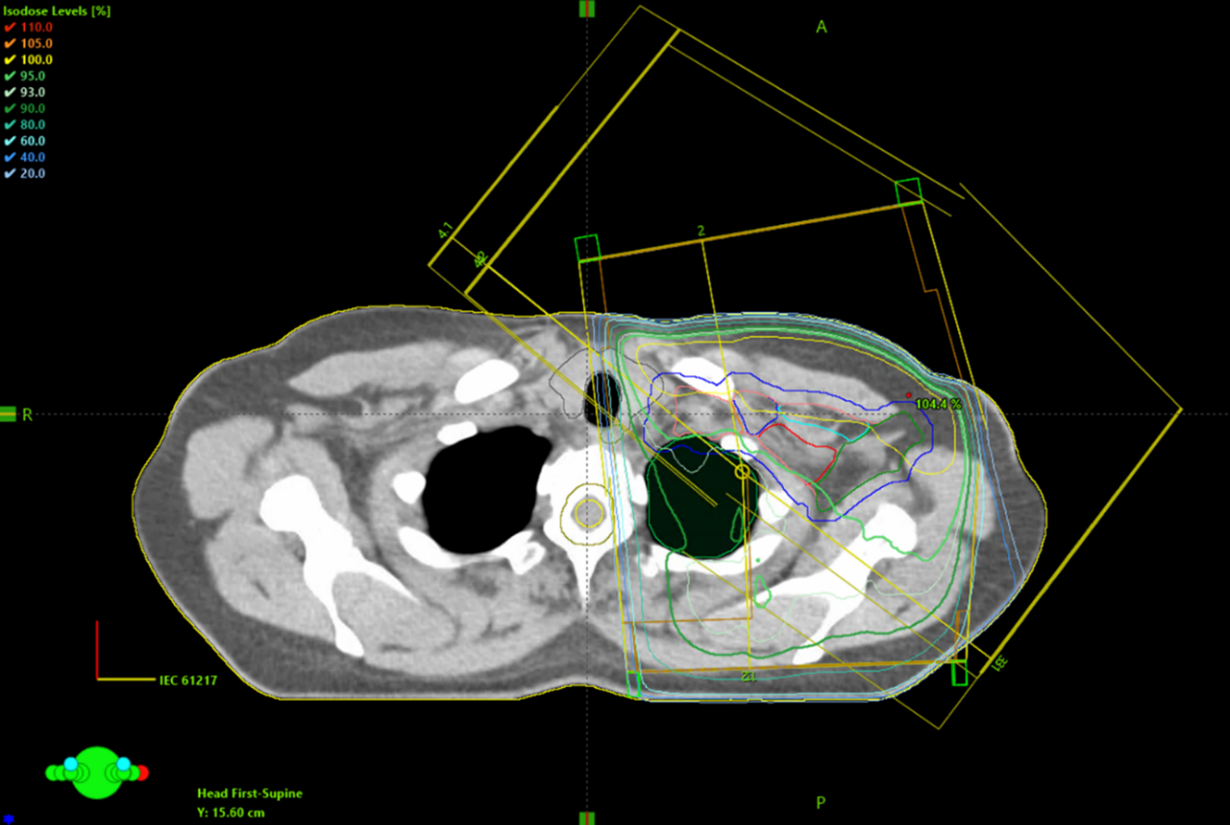
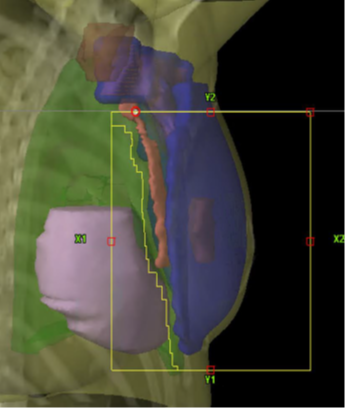
Figur 9. Exempel på BEV för strålfält över körtelvolymen.
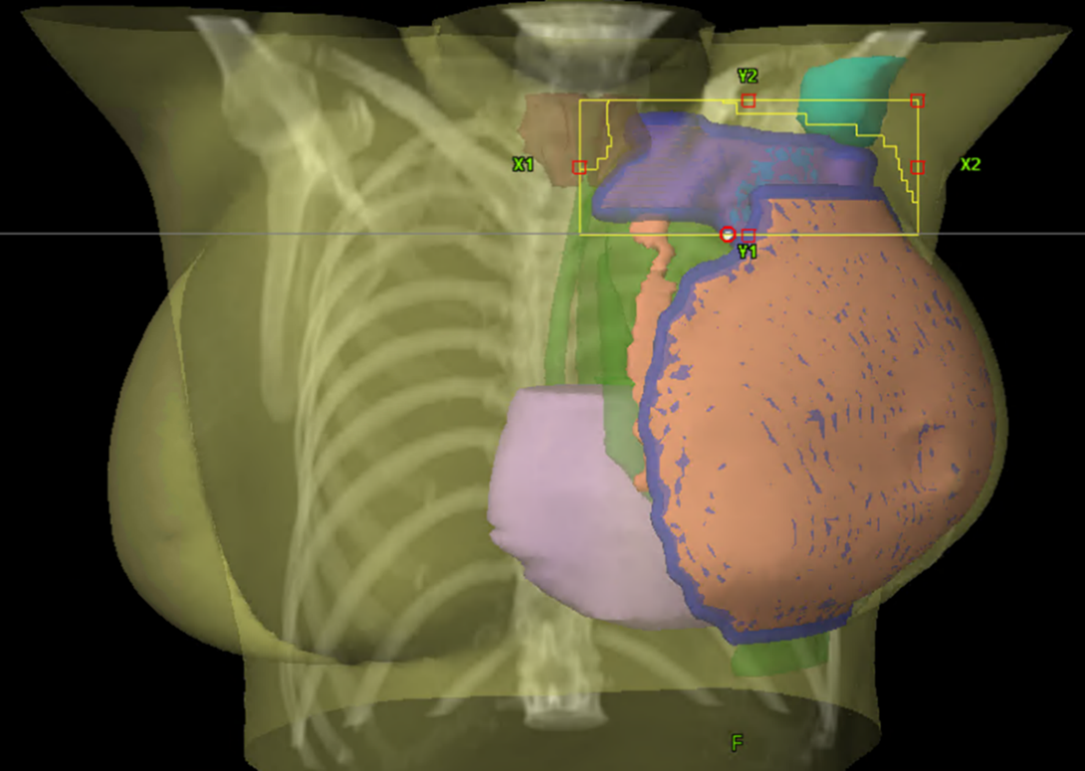
Figur 10. Exempel på dosplan med strålfält över bröstkörtelvolymen.
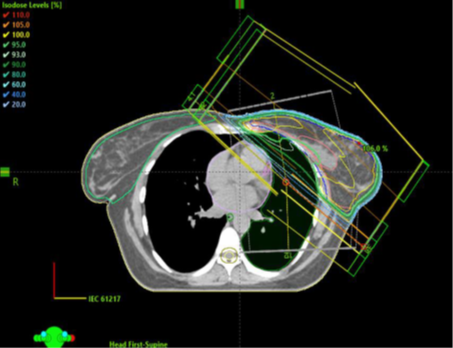
Figur 11. Exempel på BEV för tangentiella fält vid behandling med körtlar.
Referenser
- SweBCG. Bröstcancer, Nationellt vårdprogram.
- Liljegren A, Unukovych D, Gagliardi G, Bjohle J, Wickman M, Johansson H, et al. No difference in dose distribution in organs at risk in postmastectomy radiotherapy with or without breast implant reconstruction. Radiation oncology (London, England). 2014;9:14.
- SSM_rapport_2016:18. En standardiserad svensk nomenklatur för strålbehandling. www.stralsakerhetsmyndigheten.se. 2016.
- Offersen BV, Boersma LJ, Kirkove C, Hol S, Aznar MC, Sola AB, et al. ESTRO consensus guideline on target volume delineation for elective radiation therapy of early stage breast cancer, version 1.1. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2016;118(1):205-8.
- Coles CE, Griffin CL, Kirby AM, Titley J, Agrawal RK, Alhasso A, et al. Partial-breast radiotherapy after breast conservation surgery for patients with early breast cancer (UK IMPORT LOW trial): 5-year results from a multicentre, randomised, controlled, phase 3, non-inferiority trial. Lancet. 2017;390(10099):1048-60.
- Duane F, Aznar MC, Bartlett F, Cutter DJ, Darby SC, Jagsi R, et al. A cardiac contouring atlas for radiotherapy. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2017;122(3):416-22.
- Feng M, Moran JM, Koelling T, Chughtai A, Chan JL, Freedman L, et al. Development and validation of a heart atlas to study cardiac exposure to radiation following treatment for breast cancer. International journal of radiation oncology, biology, physics. 2011;79(1):10-8.
- Gagliardi G, Constine LS, Moiseenko V, Correa C, Pierce LJ, Allen AM, et al. Radiation dose-volume effects in the heart. International journal of radiation oncology, biology, physics. 2010;76(3 Suppl):S77-85.
- Nilsson G, Holmberg L, Garmo H, Duvernoy O, Sjogren I, Lagerqvist B, et al. Distribution of coronary artery stenosis after radiation for breast cancer. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2012;30(4):380-6.
- Marks LB, Bentzen SM, Deasy JO, Kong FM, Bradley JD, Vogelius IS, et al. Radiation dose-volume effects in the lung. International journal of radiation oncology, biology, physics. 2010;76(3 Suppl):S70-6.
- Lind PA, Wennberg B, Gagliardi G, Fornander T. Pulmonary complications following different radiotherapy techniques for breast cancer, and the association to irradiated lung volume and dose. Breast cancer research and treatment. 2001;68(3):199-210.
- Hall WH, Guiou M, Lee NY, Dublin A, Narayan S, Vijayakumar S, et al. Development and validation of a standardized method for contouring the brachial plexus: preliminary dosimetric analysis among patients treated with IMRT for head-and-neck cancer. International journal of radiation oncology, biology, physics. 2008;72(5):1362-7.
- Nichol A, Narinesingh D, Raman S, Germain F, Chan EK, Tran E, et al. The Effect of Bolus on Local Control for Patients Treated With Mastectomy and Radiation Therapy. International journal of radiation oncology, biology, physics. 2021;110(5):1360-9.
- Haviland JS, Owen JR, Dewar JA, Agrawal RK, Barrett J, Barrett-Lee PJ, et al. The UK Standardisation of Breast Radiotherapy (START) trials of radiotherapy hypofractionation for treatment of early breast cancer: 10-year follow-up results of two randomised controlled trials. The lancet oncology. 2013;14(11):1086-94.
- Murray Brunt A, Haviland JS, Wheatley DA, Sydenham MA, Alhasso A, Bloomfield DJ, et al. Hypofractionated breast radiotherapy for 1 week versus 3 weeks (FAST-Forward): 5-year efficacy and late normal tissue effects results from a multicentre, non-inferiority, randomised, phase 3 trial. Lancet. 2020;395(10237):1613-26.
- Fast Forward, Planning pack: https://d1ijoxngr27nfi.cloudfront.net/docs/default-source/default-document-library/fast-forward-planning-pack.pdf?sfvrsn=b5052169_0
- Coles CE, Haviland JS, Kirby AM, Griffin CL, Sydenham MA, Titley JC, et al. Dose-escalated simultaneous integrated boost radiotherapy in early breast cancer (IMPORT HIGH): a multicentre, phase 3, non-inferiority, open-label, randomised controlled trial. Lancet. 2023;401(10394):2124-37.
- Danish Breast Cancer Cooperative Group The SKAGEN Trial 1: https://www.dbcg.dk/PDF%20Filer/SKAGEN%20Trial%201_%20protokol.pdf.
- Taylor C, Correa C, Duane FK, Aznar MC, Anderson SJ, Bergh J, et al. Estimating the Risks of Breast Cancer Radiotherapy: Evidence From Modern Radiation Doses to the Lungs and Heart and From Previous Randomized Trials. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2017;35(15):1641-9.
- Travis LB, Hill DA, Dores GM, Gospodarowicz M, van Leeuwen FE, Holowaty E, et al. Breast cancer following radiotherapy and chemotherapy among young women with Hodgkin disease. JAMA : the journal of the American Medical Association. 2003;290(4):465-75.
- Yaney A, Ayan AS, Pan X, Jhawar S, Healy E, Beyer S, et al. Dosimetric parameters associated with radiation-induced esophagitis in breast cancer patients undergoing regional nodal irradiation. Radiotherapy and oncology : journal of the European Society for Therapeutic Radiology and Oncology. 2021;155:167-73.
- Wang J, Yang Z, Hu W, Chen Z, Yu X, Guo X. Intensity modulated radiotherapy with fixed collimator jaws for locoregional left-sided breast cancer irradiation. Oncotarget. 2017;8(20):33276-84.
Appendix 1 Rekommendationer vid andningsanpassad strålbehandling av bröstcancer (Gating)
Dokumentversion 2013-08-01 har tagits fram av följande arbetsgrupp;
Sofie Ceberg, sjukhusfysiker, Skåne Universitetssjukhus, Malmö/Lund
Anna Karlsson Hauer, sjukhusfysiker, Sahlgrenska Universitetssjukhuset, Göteborg
Karin Uttman, sjukhusfysiker, Centralsjukhuset, Karlstad
Joakim Jonsson, sjukhusfysiker, Norrlands Universitetssjukhus, Umeå
Jesper Lindberg, sjukhusfysiker, Sahlgrenska Universitetssjukhuset, Göteborg
Andning
Andningskurva
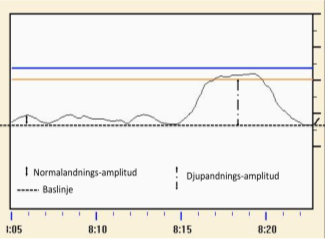
Fyra begrepp som beskriver patientens andningskurva (figur 1).
Baslinje
Baslinjen motsvarar bröstkorgens lägsta nivå vid avslappnad andning.
Normalandnings-amplitud
Avståndet mellan baslinjen och maxnivå under avslappnad andning.
Gatingfönster
Det amplitudintervall inom vilken ”beam-on” tillåts.
Djupinandnings-amplitud
Avståndet mellan baslinjen och upp till nedersta linjen på gatingfönstret.
Figur 1. Baslinje, normalandnings-amplitud, gatingfönster och djupinandnings-amplitud.
Andningsteknik
Två olika sätt att andas förekommer vid andningsanpassad strålbehandling av bröstpatienter;
- kontinuerlig djupandning (Enhanced Inspiration Gating) eller
- djup inandning följt av att hålla andan (Deep Inspiration Breath Hold).
Behandling sker för båda teknikerna kring ”inandningstoppen” på andningskurvan. De flesta patienterna klarar av att hålla andan 15 sekunder utan problem.
Guidning
Till hjälp för patienterna att uppnå en reproducerbar andning kan man erbjuda guidning, vilken kan vara muntlig och/eller visuell. Visuell guidning där patienten kan följa sin andningsnivå på t.ex. en monitor är att rekommendera. De får då lättare att nå den önskvärda nivån på andningsamplituden varje gång de andas in djupt.
Gatingfönster
Placering av gatingfönster – djupinandnings-amplituden
Ett riktvärde är att placeringen för gatingfönstrets nedre del (djupinandnings-amplituden) bör vara på minst 10 mm höjd över baslinjen, men maximalt 20 mm. Observera att dessa tal endast är riktvärden.
Vid fastställande av patientens djupinandnings-amplitud bör man också utgå från amplituden för patientens avslappnade andning, s.k. normalandnings-amplitud. En regel är att placera gatingfönstrets nedre kant på ett avstånd från baslinjen som är väsentligt större än normalandnings-amplituden. Det är dock viktigt att patientens djupinandnings-amplitud inte ska vara större än att patienten klarar av att andas in djupt på ett stabilt och reproducerbart sätt. Det är mycket viktigt att patientens andningskurva kommer ner till baslinjen mellan tillfällena för beam-on.
Storlek på gatingfönster
Även storleken på gatingfönstret är kopplat till patientens normalandnings-amplitud då gating inte ska introducera en större rörelse under behandlingen än den konventionella behandlingstekniken. Ett riktvärde för gatingfönstrets storlek är ca 3 mm med visuell guidning och ca 4 mm utan. Om patientens normalandnings-amplitud är > 4 mm bör gatingfönstret inte utökas om inte speciella skäl föreligger.
Dosplanering
Kilade fält
Det är vanligt att patienten upplever det krävande att hålla andan längre än 15-20 s, vilket i sin tur ökar risken för att det tar lång tid innan patienten återgår till baslinjen efter behandlat fält vid djup-inandningstekniken. Då fält med kil tar längre tid att behandla pga. låg dosrat bör detta undvikas. Vid tillfälle då det inte går att undvika fält med kil kan fältet delas upp i två, ett med- och ett utan kil, så att patienten har möjlighet att hämta andan. Tilläggsfält kan i de flesta fall ersätta behovet av strålfält med kil.
Inre referenspunkt
Om inre referenspunkt används bör denna vara placerad långt ifrån rörelseområdet, förslagsvis i nivå med nedre delen av sternum i kranio-kaudalled, samt djupt ner i patienten i vertikalled.
Yttre referenspunkt
Om yttre referenspunkt används bör två CT-set upptas; ett under normalandning och ett under djupandning och gating. Eftersom patienten andas normalt under set-up vid behandling bör även referenspunkten i gatingplanen vara placerad i patientens normalandningsläge. I TPS kan båda CT-studierna överlagras. Referenspunkten kan sedan placeras, i det CT-set med gating, utifrån placeringen av markörerna under normalandnings-CT.
CT-sessionen under normalandning kan förslagsvis upptas med lägre upplösning och över mindre område för att minimera absorberad dos till patient.
Kvalitetssäkring (QA)
Maskin- och systemspecifik QA
- Kontrollera att bordshäng på CT är inom toleransen. Vidta ingen överkompensation.
- Kontrollera att beam-on endast sker i gatingfönstret.
- Utvärdera att beam-on samt beam-off sker utan fördröjning då behandlingsmaskin får signal från gatingsystemet.
- Utvärdera att beam-on samt beam-off sker utan fördröjning för gatead (kV och MV) bildtagning.
- Kontrollera att amplituden visas lika stor för alla kamerasystem genom att använda ett stabilt rörelsefantom med exakt amplitud.
- Kontroll av brus i systemet, dvs registrerad signal över tid med stillastående markör. Den ska vara max 1mm (drift i systemet).
- Kontrollera symmetri, flatness och doslinjäritet för acceleratorn.
- Kontrollera ackumulerad absorberad dos från en gatingbehandling.
Patientspecifik QA
- Kontrollera att alla parametrar som bestäms individuellt vid referenssessionen (CT) är identiska vid första behandlingen (accelerator). Dessa parametrar är bl.a. nivåer för nedre- och övre gräns för gatingfönster, samt tider för eventuell audio-guidning.
- Vid första fraktionen rekommenderas att använda ”integrated image” för fälten om möjligt, utöver konventionell bildtagning.
- Kontrollera andningskurvans utseende efter första fraktionen. Observera eventuellt skift i baslinje samt jämförbar rörelse i gatingfönstret mot referenssessionen.
- Vid introduktion av gating bör antal bilder utökas för att utvärdera eventuella systematiska avvikelser. Rekommendationen är bildtagning minst två ggr/vecka.
- När bröstgating är implementerad i kliniken och all berörd personal utbildad, bör stickprov beträffande kontroll av skift i baslinjen genomföras för alla patienter någon gång under behandlingen.
Utbildning
- Kontinuerlig utbildning av personal är nödvändig.
- Ett Gating-körkort eller liknande är att rekommendera.
Övrigt
- En andningstränings-session före patientens CT-undersökning rekommenderas för att minska tidsåtgången vid densamma.
- För dubbelsidig mam-patient rekommenderas att både vänster- och höger sida behandlas med andningsanpassad strålterapi. För RPMÔ-systemet* rekommenderas en referensfil (CT), men två sessioner (höger respektive vänster) vid behandlingen.
- Cirka 5 minuters längre time-slot vid behandling för gatingpatienter är att rekommendera.
* Real-time Positioning Management™ (RPM), Varian Medical Systems.
