Bilaga 1 Blinatumomab i primärterapi vid Ph-neg B-ALL
EMA och NT-råds godkännande för användande av blinatumomab i konsolidering vid primärbehandling
Rational
NT-rådet rekommenderar, efter genomförd hälsoekonomisk bedömning, från 19 december 2025 Blinatumomab som tillägg till primärterapi för vuxna patienter med Philadelphia-negativ ALL i konsolidering i enlighet med godkännande från EMA. EMA godkännandet baseras i huvudsak på den randomiserade ECOG-ACRIN studien E1910(1) som visat signifikant överlevnadsvinst för patienter som erhållit add-on behandling (till cytostatikaterapi) med 4 cykler Blinatumomab i konsolidering av behandling. EMA godkännande finns sedan tidigare gällande MRD positiv sjukdom.
Svenska vuxen ALL gruppen har valt starta Blinatumomab i konsolidering efter induktion (enligt studien SUBLIME) då studien E1910, med senare behandlingsstart, hade ett stort bortfall innan patienterna skulle erhålla Blinatumomab (på grund av toxicitet, relaps och avbruten studie). Vi har också eftersträvat att behandlingsstrukturen för vuxna patienter i Sverige med Blinatumomab ska bli likartad, oavsett ålder och behandlingsprotokoll.
Rekommendation Blinatumomab i primärbehandling för Philadelphia-negativ, CD19-positiv B-ALL, som del i konsolideringsbehandling
Vad är nytt i de uppdaterade riktlinjerna
- För patienter med Ph-negativ, CD-19 positiv, B-ALL i komplett remission ges 4 kurer Blinatumomab som tillägg till nu rekommenderad behandling
- Vid behandling enligt NOPHO ALL 2008 med dosreduktioner används inte längre SR arm utan de patienterna allokeras till IR behandling
Hur skall Blinatumomab ges
- 18-45 år – enligt optional treatment recommendation (OTR) i A2G1 för patienter i SR och IR-high riskgrupper. Se separat dokument ALLTogether1, Blinatumomab OTR 18-45y som finns tillgängligt på alla universitetssjukhus som behandlar patienter enligt ALLTogether. HR patienter behandlas sedan tidigare enligt HR alternative treatment guidelines.
- 45-(65)70 år – enligt NOPHO ALL 2008 med dosreduktioner. Här kommer inte längre SR protokollet användas, samtliga patienter behandlas enligt IR eller HR protokoll med integration Blinatumomab i IR protokollet
- >(65)70 år Nationellt behandlingsprotokoll Ph-neg ALL med integration Blinatumomab
Generella regler för NOPHO ALL2008 och nationellt behandlingsprotokoll >70år Ph-neg B-ALL
- Blinatumomab (Blin) startdos 9 µg/dygn dag 1-7 därefter 28 µg/dygn dag 8-28 om MRD 0.1-5% vid start
- Blin startdos 28 µg/dygn dag 1-28 om MRD 0-0.1% vid start, liksom efterföljande kurer
- Observera att alternativ dosering finns i FASS om patient väger mindre än 45 kg
- Överväg startdos 9 µg/dygn dag 1-7 även för patienter med (oavsett MRD):
- Känd epilepsi eller tidigare enstaka epileptiska anfall
- Strukturell CNS avvikelse (t.ex. efter tidigare stroke)
- Högre risk för neurotoxicitet enligt behandlande läkare
- Överväg Keppraprofylax individuellt för varje patient
- Startkriterier ANC>0.75, TPK>75, eller enligt individuellt övervägande
- Intratekal terapi (IT) (singel MTX eller trippel beroende på CNS status) ges dag 15 och 28 i varje cykel. Leukovorin ges 24 h efter IT för patienter >45år. Totalt antal IT behandlingar är oförändrat, för detaljer se Bilaga 1 Dosreduktion av NOPHO ALL 2008 Ph-negativ ALL, dosreduktioner patienter 45-70 år samt nedan gällande patienter >70 år
- Överväg IvIG substitution och övervaka IgG nivåer även efter avslutad Blin. Viss ökad infektionsbenägenhet kan förväntas, relaterat hypogammaglobulinemi.
Vem bör erhålla Blinatumomab i konsolidering som del i NOPHO ALL2008 och nationellt behandlingsprotokoll >70år Ph-neg B-ALL
- CD19 pos Philadelphia-negativ B-ALL.
- Kan ges som del i konsolidering för patienter i första remission utan transplantationsindikation
- Kan starta då remission med MRD <5%
Eller
- Som brygga till transplantation (indikation sedan tidigare, ingen förändring)
När kan Blina ej startas trots att MRD <5% efter induktion?
- Vid extramedullär sjukdom inkl testis (förutom CNS) som ej nått remission dag 28. Fortsätt med konsolidering 1 och utvärdera därefter (utgör inte högrisk kriterie om remission nås dag 78/85). Om komplett respons d 78/85 kan behandling fortsättas enligt IR arm med försenad start Blinatumomab, se flödesschema 2.
- CNS slow response (= kvarstående blaster i LP nr 4 dvs efter 1 MTX och 2 tripplar, alternativt kvarstående sjukdom vid MRT utvärdering om ej initialt blaster vid LP).
- CNS slow response utgör ett event och föranleder HSCT om patient aktuell för detta. Som alternativ till allo-hSCT vid CNS-sjukdom överväg NOPHO-IR+Blina och CNS-bestrålning 18Gy
- Patienter som EJ kan starta Blin1 ska fortsätta enligt Consolidation I
(med sedvanlig utvärdering dag 78/85 och sedvanliga transplantationsindikationer)
Hur definieras behandlingssvikt efter Blinatumomab
- ≥1 log ökning av MRD under behandling oavsett tidpunkt
- Stigande MRD d 15 i cykel Blin1 (oavsett nivå om bedöms metodmässigt säkerställt)
- MRD ≥0.01% efter Blin1
- MRD ≥0.01% efter Blin2. Vid denna tidpunkt bör MRD vara omätbart. Vid mätbar eller kvarstående MRD signal som ej är kvantifierbar rekommenderas diskussion med regionalt ansvarig ALL kollega eller i SVALL gruppen gällande val fortsatt behandling
- Behandlingssvikt i form av extramedullär sjukdom under pågående behandling
Vid konstaterad behandlingssvikt avslutas behandling med Blinatumomab och individuellt ställningstagande sker gällande fortsatt behandling
Vilka är de aktuella allo hSCT indikationerna när Blina ges vid Ph-neg B-ALL dosreducerad NOPHO 45-70 år
Gäller de patienter som man bedömer, givet samsjuklighet och AT, potentiellt vara aktuella för allo hSCT
Sedan tidigare gäller oförändrat:
- MRD>5% efter induktion
- Extramedullär sjukdom inkl testis (förutom CNS) som ej nått remission dag 78/85
- CNS slow response (= kvarstående blaster i LP nr 4 dvs efter 1 MTX och 2 tripplar eller kvarstående radiologisk förändring). Som alternativ till allo hSCT vid CNS-sjukdom kan NOPHO-IR+Blina och CNS-bestrålning totaldos 18Gy övervägas.
Justerade indikationer när behandling med Blinatumomab ges:
- MRD efter första eller andra Blin ≥ 0.01%. Om kontraindikation allo hSCT och gott initialt svar kan cytostatikadel av IR protokoll övervägas. Vid mätbar men ej kvantifierbar MRD efter andra Blin individuell bedömning (och omkontroll av MRD efter Cons I)
- KMT2A med negativ MRD– enligt individuell bedömning där svar både på induktion och blinatumomab bör tagas med i övervägandet. Vetenskapligt stöd för huruvida kemoterapi/blinatumomab eller allo hSCT ger högst möjlighet sjukdomsfri överlevnad för denna grupp som tidigt når MRD negativitet saknas
- T(17;19) utgör transplantationsindikation oavsett MRD
- Låg hypodiploidi och övrig genetik föreslås följa MRD indikationer
Ph-neg B-ALL 45-70 år, CD19 pos sjukdom, IR-arm
- OBS : IT ges dag 15 och 28 i varje Blin-cykel
Flödesschema 1: Grundschema för patienter utan extramedullär sjukdom.
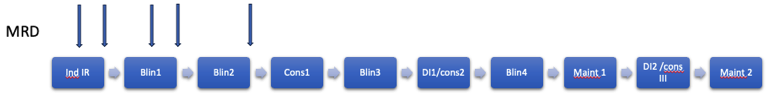
Flödesschema 2: Endast för patienter med extramedullär sjukdom enligt ovanstående definitioner som behandlas enligt IR schema
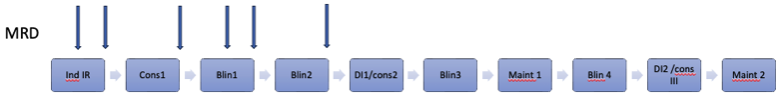
Ph-neg B-ALL 70-80 år, CD19 pos sjukdom
Gäller även i denna åldersgrupp MRD d 29 <5%, se ovan gällande MRD och extramedullär sjukdom samt utvärdering under behandling
OBS : IT ges dag 15 och 28 i Blin 1 och 2, samt dag 15 i Blin 3 och 4
Totalt antal IT = 12 om CNS1 föreligger
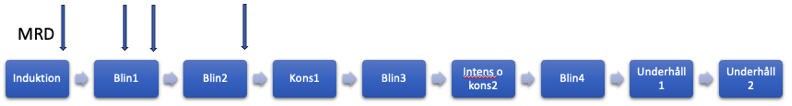
Startkriterier Blin1: Start ca dag 30 om MRD <5% och ANC>0.75, TPK>75 (Oncaspar ges ej innan start).
Startkriterier Blin2: Start 14 dagar efter avslut Blin2 om MRD <0.01% och ANC>0.75, TPK>75.
Start Kons 1: 7 dagar efter Blin2s avslut. Börjar med dag 30 oncaspar. Dag 85 oncaspar ges ej innan Blin3
Startkriterie Blin3: dag 92 om ANC>0.75, TPK>75
Start Intensifiering/kons2 ca 7 dagar efter Blin3s avslut. Start med oncaspar d 85. IT dag 92 och 127 ges ej.
Startkriterie Blin4: dag 148 om ANC>0.75, TPK>75. D 148 Rituximab ges ej och ersätts ej.
Maintenance 1 startar ca 7 dagar efter Blin4s avslut
OBS angivelse av dagar hänvisar till urprungliga behandlingsdagar i behandlingsprotokollet
Referens:
1. Litzow MR, Sun Z, Mattison RJ, Paietta EM, Roberts KG, Zhang Y, Racevskis J, Lazarus HM, Rowe JM, Arber DA, Wieduwilt MJ, Liedtke M, Bergeron J, Wood BL, Zhao Y, Wu G, Chang TC, Zhang W, Pratz KW, Dinner SN, Frey N, Gore SD, Bhatnagar B, Atallah EL, Uy GL, Jeyakumar D, Lin TL, Willman CL, DeAngelo DJ, Patel SB, Elliott MA, Advani AS, Tzachanis D, Vachhani P, Bhave RR, Sharon E, Little RF, Erba HP, Stone RM, Luger SM, Mullighan CG, Tallman MS. Blinatumomab for MRD-Negative Acute Lymphoblastic Leukemia in Adults. N Engl J Med. 2024 Jul 25;391(4):320-333. doi:10.1056/NEJMoa2312948. Cited in: Pubmed; PMID 39047240.
