Ph-positiv ALL
Rekommendationer
- < 60 år utan samsjuklighet behandlas enligt ABCDV + TKI.
- 60-75 år eller yngre med samsjuklighet* behandlas enligt SVALL/EWALL + TKI.
- > 75 år behandlas med steroider + TKI +/- lågintensiv cytostatikabehandling.
- Allo-HSCT bör eftersträvas för patienter upp till 60-65 års ålder om ingen samsjuklighet eller annan kontraindikation föreligger.
- CNS-profylax ges med totalt 10 intratekala behandlingar (< 75 år), profylax till patienter > 75 år bör individualiseras.
- Tidigt byte till nästa linjes TKI rekommenderas vid otillräckligt behandlingssvar.
- Inför varje TKI-byte utförs BCR::ABL1-mutationsanalys, om möjligt.
* data finns med goda behandlingsresultat med något mindre intensiv cytostatika + TKI varför SVALL/EWALL kan övervägas vid samsjuklighet även hos yngre patient.
Förekomst av Philadelphiakromosomen (Ph), det vill säga BCR::ABL1 (t(9;22) (q34;q11)), ökar med stigande ålder och återfinns huvudsakligen hos patienter med B-ALL. Ph-positiv ALL är ovanlig hos barn, men förekommer hos 26 % av vuxna med ALL och 34 % av B-ALL-fallen 1 med högst incidens i gruppen 50–59 år. Förekomst av mutationer i IKZF1-genen tillsammans med mutationer i CDKN2A/B- och/eller PAX5-genen (IKZF1 plus) är vanligare hos patienter med Ph-positiv ALL (ca 60 %) och har i en del kliniska studier varit associerad med sämre överlevnad oavsett om patienterna har genomgått allo-HSCT 25262728. Liknande effekt har dock inte kunnat visas i en analys av data från den engelska UKALL14-studien där drygt 600 patienter har inkluderats 29. Då flertalet studier visat prognostisk betydelse rekommenderas analys av IKZF1 plus enligt avsnitt 7.3.2 Benmärgsundersökning.
Prognosen vid Ph-positiv ALL har förbättrats betydligt sedan imatinib lades till i standardbehandlingen 1 och är enligt svenska registerdata i dag jämförbar med Ph-negativ ALL för yngre patienter som kan genomgå allo-HSCT. För patienter över 60 år medför den målriktade TKI-behandlingen en bättre prognos jämfört med patienter med Ph-negativ ALL (ALL-registerrapport nr 6). I Sverige har för närvarande endast imatinib indikation för primärbehandling av Ph-positiv ALL.
Hög remissionsfrekvens kan uppnås med steroider i kombination med TKI. De senaste åren har man även kunnat visa att andra och tredje generationens TKI i kombination med mindre intensiv cytostatikabehandling eller immunterapi kan ge hög grad av komplett molekylär remission och låg toxicitet 283031. GRAALL-gruppen har visat att mindre intensiv cytostatikabehandling tillsammans med TKI som induktionsbehandling ger minskad frekvens av tidig död och signifikant högre frekvens av komplett remission 32. Detta är bakgrunden till den begränsade dosreduktionen av cytostatika för patienter under 60 år som infördes 2017 för ABCVD. Eftersom byte av TKI sannolikt är mer effektivt än cytostatika rekommenderas nu även dosreducerad konsolideringsbehandling (mini-VABA) även för de patienter som ej når ett gott behandlingssvar efter induktionsbehandling och mer lågintensiv cytostatikabehandling vid efterföljande konsolideringar.
Internationellt finns icke-randomiserade data som visar långtidsöverlevnad utan HSCT då primärbehandling ges med senare generationers TKI, ofta i kombination med antikroppsbaseradterapi och cytostatika (kombinationer av läkemedel som inte ännu rekommenderas enligt NT-rådet i Sverige för denna indikation). I väntan på ytterligare vetenskapligt underlag och godkännande av senare generationers TKI i primärbehandling rekommenderas därför alloHSCT för yngre patienter upp till 60–65 år utan samsjuklighet. För något äldre patienter får ett individuellt ställningstagande göras, där svar på initial behandling, samsjuklighet och riskbedömning gällande transplantations relaterad mortalitet får vägas samman. I denna situation kan även förekomst av IKZF1 plus vägas in i den totala bedömningen.
Primärbehandling av Ph-positiv ALL
Rekommendationer
Primärbehandling Ph-positiv ALL med hänsyn tagen till biologisk ålder och samsjuklighet.
Figur 6. Under 60 år och utan samsjuklighet
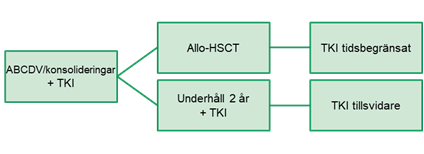
Figur 7. Under 60 år med samsjuklighet eller ålder 60–75 år
 Över 75 år
Över 75 år
TKI samt steroider +/- lågintensiv cytostatikabehandling
TKI-behandling (samtliga åldrar):
- Imatinib 600 mg x 1 ges som första linjens behandling. Vid intolerans eller svikt rekommenderas tidigt byte till andra generationens TKI, i första hand dasatinib 140 mg.
- Längre uppehåll under cytopenifasen bör undvikas.
- För interaktioner och val av understödjande behandling, se kapitel Kapitel 18 Understödjande vård.
- För detaljerad beskrivning av olika TKI-preparat, biverkningar och TKI-specifik uppföljning, se det nationella vårdprogrammet för KML.
Patienter med biologisk ålder under 60 år
Rekommendationer
Figur 8 Behandling av patienter med Ph-positiv ALL och biologisk ålder under 60 år.
8a) Gott initialt svar på terapi, HSCT planeras

8b) Gott initialt svar på terapi, behandlingsförslag om HSCT ej lämpligt eller möjligt
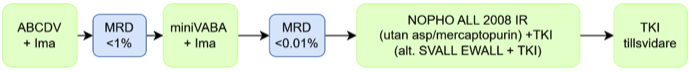
8c) Inadekvat initialt svar på terapi
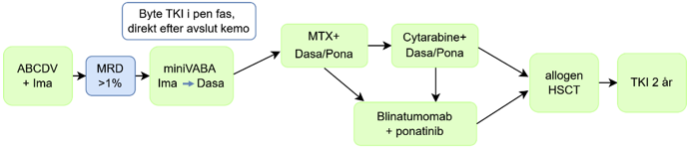
CNS-profylax: injektion metotrexat 12 mg intratekalt (10 behandlingar vid CNS1)
För behandlingsprotokoll, se bilaga 6 Ph-positiv ALL Behandlingsprotokoll yngre patienter.
Allogen stamcellstransplantation kvarstår som målsättning för flertalet patienter under 60 år, men individuellt ställningstagande kan behöva göras givet samsjuklighet, möjlighet finna donator med god matchgrad samt svar på initial behandling, där MRD med flödescytometri < 0,01 % efter mini-VABA kan vara riktmärke och MRD negativitet både med flöde och RQ-PCR BCR::ABL1 sedemera bör uppnås om man överväger avstå från allogen HSCT. Så snart BCR::ABL1 påvisats startas kontinuerlig behandling med imatinib. Behandling i fulldos (det vill säga 600 mg x 1) bör eftersträvas och uppehåll under cytopenifasen bör undvikas, framför allt under den initiala behandlingsfasen 33.
MRD <1% efter induktion med Imatinib+ ABCDV (fig 8a och 8b)
Allo-HSCT kan planeras till efter 2–4 kurer, det vill säga induktion och 1–3 konsolideringar (fig 8a). Notera att rekommenderat antal intratekala behandlingar också bör hinna ges. Patienter som inte planeras genomgå allo-HSCT bör i normalfallet få fortsatt tillsvidarebehandling med TKI även när underhållet med cytostatikabehandling har avslutats. Den fortsatt konsoliderande kemoterapin kan vara samma som för patienter > 60 år (SVALL/EWALL), men för yngre patienter där man t.ex. pga svårigheter finna välmatchad donator och samtidigt gott molekylärt svar väljer avstå från allogen HSCT bör man överväga att i stället ge cytostatika enligt NOPHO ALL 2008 IR men utan asparaginase och utan mercaptopurin i underhåll (fig 8b).
MRD >1% efter induktion med Imatinib+ABCDV (fig 8c)
Vid avsaknad av remission, > 1 % leukemiska blaster, inte har uppnåtts efter Imatinib + ABCDV bör man starkt överväga att byta TKI föregånget mutationsanalys, se även avsnitt 12.2 Remissionsbedömning samt MRD-monitorering vid Phpositiv ALL. Bytet rekommenderas direkt efter avslut av miniVABA kemoterapi (t.ex. i pen fas) då data saknas för kombinationsbehandling med andra TKIer än imatinib vid denna cytostatikakombination. Om behandlingssvikt vid utvärdering efter mini-VABA (MRD med flödescytometri > 0,01 %) bör sviktbehandling vanligen med byte till ponatinib vid behov tillsammans med blinatumomab ges som brygga till transplantation, för vidare information se avsnitt 17.6.1 Behandlingssvikt vid ålder upp till 75 år.
CNS-profylax vid ålder < 60 år
Riskfaktorer för senare CNS-återfall är bland annat hyperleukocytos och högt LD vid diagnos, faktorer som är vanligare hos patienter med Ph-positiv ALL. Även vilken systemisk cytostatikabehandling som är given och val av TKI-behandling påverkar sannolikt risken. I en nyligen publicerad studie har patienter med Ph-positiv ALL som behandlats med 12 intratekala behandlingar haft betydligt lägre risk för CNS-återfall jämfört med patienter som har fått 8 behandlingar oavsett genomgången allo-HSCT 34. Antal förebyggande intratekala behandlingar ökas därför till 10 oavsett om allo-HSCT planeras. Att 10 behandlingar (och inte 12) rekommenderas hänger samman med att det svenska protokollet ABCDV/miniVABA innehåller högdos cytarabin som har god CNS-penetrans.
Som CNS-profylax ges alltid vid den diagnostiska lumbalpunktionen injektion metotrexat 12 mg intratekalt. Därefter ges ytterligare 9 intratekala (IT) injektioner för patienter som inte har CNS-leukemi. Injektionerna bör initialt ges en gång per vecka; observera att trombocyter bör hållas > 50 x 109/l vid denna behandling. För patienter som planeras för HSCT bör man eftersträva att hinna ge samtliga intratekala injektioner innan transplantationen, annars bör patienten få resterande injektioner efter genomgången allo-HSCT, avsnitt 15.6 Kompletterande CNS-profylax. Ingen profylaktisk strålbehandling ges mot CNS. Information om patienter med CNS-leukemi finns i bilaga 9 CNS-leukemi.
Tidpunkt för allo-HSCT
Allo-HSCT bör genomföras så fort som patienten nått en mycket god remission med MRD minst < 0,01 % med flödescytometri, vanligen efter 1–2 konsolideringar. Observera att viss diskordans kan finnas mellan flödescytometri och RT-PCR BCR::ABL, beroende på vilka celler som härbärgerar Philadephiakromosomen. Se även Kapitel 15 Allogen stamcellstransplantation (allo‑HSCT).
Patienter med biologisk ålder 60–75 år
Rekommendationer
Figur 9 Behandling av patienter med Ph-positiv ALL och biologisk ålder 60–75 år.

- SVALL/EWALL + kontinuerlig behandling med TKI.
- TKI-uppehåll görs dag 1–3 under HDMTX och asparaginaskonsolideringar.
- För enskilda patienter kan allo-HSCT övervägas.
I en utvärderande studie jämfördes det tidigare European Working Group for Adult ALL (EWALL)-protokollet, som infördes 2009, med det tidigare ABCDV/VABA-protokollet. Resultatet visade en fortsatt hög toxicitet utan någon överlevnadsvinst. Den höga toxiciteten inkluderade hög dödlighet under behandlingens första 60 dagar 35. Detta ledde till att man 2016 införde ett modifierat och dosreducerat protokoll enligt Svenska ALL-gruppen SVALL/EWALL för patienter över 60 år med Ph-positiv ALL. Behandlingen består av en förbehandling och induktionsbehandling följt av 6 konsolideringar. Reinduktionskurer fortsätter sedan varannan månad i 2 år. Imatinib sätts in så snart som BCR::ABL1 har detekterats och fortsätter som tillsvidarebehandling.
Om morfologisk remission med MRD < 1 % inte uppnås efter induktion används de 2 första konsolideringarna som fortsatt induktionsbehandling och en ny remissionsutvärdering görs efter den första konsolideringskuren. BCR::ABL1-mutationsanalys och tidigt byte till nästa linjens TKI rekommenderas i dessa fall. Protokollet finns i bilaga 7 Ph-positiv ALL Behandlingsprotokoll äldre patienter – SVALL/EWALL.
Uppehåll med TKI görs dag 1–3 under högdos metotrexat/asparaginaskonsolideringarna. Kombinationen av TKI och asparaginas kan orsaka levertoxicitet, och då bör man göra ett individuellt övervägande om att till exempel utesluta asparaginas i kommande kurer. Vid bedömning av till exempel levertoxicitet bör man observera att effekten av givet PEG-asparaginas kan kvarstå i 14–21 dagar.
För enskilda patienter kan allo-HSCT övervägas, varvid antalet konsolideringar kan minskas. Se även avsnitt 12.1.1.2 Tidpunkt för allo-HSCT.
CNS-profylax vid ålder 60–75 år
Som CNS-profylax ges metotrexat 12 mg intratekalt, vilket är obligatoriskt vid den diagnostiska lumbalpunktionen. Därefter ges intratekal behandling enligt cytostatikaschemat, vilket innebär ytterligare 9 intratekala injektioner. Ingen profylaktisk strålbehandling ges mot CNS. Information om patienter med CNS-leukemi finns i bilaga 9 CNS-leukemi.
Patienter med biologisk ålder över 75 år
Rekommendationer
- Kontinuerlig behandling med TKI + steroider intermittent.
- Tillägg av vinkristin enligt EWALL-protokollet kan övervägas.
Vid Ph-positiv ALL i denna åldersgrupp kan man kortsiktigt få goda behandlingsresultat med TKI, i första hand imatinib i kombination med steroider 36. Imatinib 600 mg x 1 kombineras med steroider i samma dosering som beskrivs i bilaga 7 Ph-positiv ALL Behandlingsprotokoll äldre patienter – SVALL/EWALL. Tillägg av vinkristin enligt samma protokoll kan övervägas, liksom ytterligare cytostatika enligt protokollet om patientens allmäntillstånd så tillåter. Individualiserad behandling får eftersträvas med syfte att skapa balans mellan effekt och risk för toxicitet. Vid refraktär sjukdom bör man överväga att byta till andra och tredje generationens TKI (se kapitel 17 Handläggning av återfall och refraktär sjukdom). Inför ett behandlingsbyte rekommenderas en mutationsanalys.
CNS-profylax vid ålder över 75 år
CNS-profylax kan behöva individualiseras för denna patientgrupp, men som alltid ges metotrexat 12 mg intratekalt vid den diagnostiska lumbalpunktionen. Om patienten uppnår remission, och om det är medicinskt rimligt, föreslås fortsatt intratekal behandling vid motsvarande tidpunkter för cytostatikaschemat för SVALL/EWALL, vilket innebär ytterligare 9 intratekala injektioner. Ingen profylaktisk strålbehandling ges mot CNS. Information om patienter med CNS-leukemi finns i bilaga 9 CNS-leukemi, men även här kan behandlingsschemat behöva individualiseras.
Remissionsbedömning samt MRD-monitorering vid Ph positiv ALL
Rekommendationer
- Vid remissionssyftande behandling utförs benmärgsundersökning inklusive prov för MRD inför start av konsolideringsbehandling. Vid långdragen peni bör benmärgsundersökning inklusive MRD göras senast dag 30.
- Som MRD-markör används både RT-PCR för BCR::ABL1 och flödescytometri.
- Under primärbehandling enligt ABCDV-protokoll utförs MRD på benmärgsprov
– vid remissionsbedömning (MRD1)
– inför start av konsolidering 2 (MRD2)
– inför start av konsolidering 3 (MRD3)
– inför eventuell allo-HSCT. - MRD-tidpunkter under behandling enligt SVALL/EWALL, se bilaga 7 Ph-positiv ALL Behandlingsprotokoll äldre patienter – SVALL/EWALL.
- För patienter som får underhållsbehandling bör man överväga fortsatt MRD-monitorering på blodprov med 2–3 månaders intervall. Om nivån stiger eller kvarstår högt (> 0,01 %) bör man komplettera med MRD-analys med både PCR för BCR::ABL1 och flödescytometri och byta TKI vid bekräftat återfall eller refraktär sjukdom.
- Mutationsanalys (BCR::ABL1 + T315I) bör utföras vid behandlingssvikt och inför behandlingsbyte om tekniskt möjligt, för närvarande vid nivå BCR::ABL cirka > 0,1 %. Diskutera med laboratoriet vid låga BCR::ABL-nivåer.
Vid remissionssyftande behandling utförs benmärgsundersökning, inkluderande prov för MRD-undersökning, inför start av konsolideringsbehandling, motsvarande dag 25–29 (MRD1) efter cytostatikabehandlingens start. Vid hypoplasi utförs en ny undersökning efter en vecka.
Om komplett morfologisk remission, det vill säga < 1 % leukemiska blaster, konfirmerat med flödescytometri, inte har uppnåtts inför första konsolideringsbehandlingen och TKI har givits utan större uppehåll bör man starkt överväga att byta TKI. Mutationsanalys av BCR::ABL1 samt PCR för T315I rekommenderas 3738, men det är inte nödvändigt att invänta svaret innan byte av TKI. Däremot rekommenderas att bytet sker efter avslut av mini-VABA (t.ex. i pen fas) då data saknas för kombinationsbehandling med andra TKIer än imatinib vid denna cytostatikakombination.
För övriga tidpunkter för MRD-monitorering hänvisas till rekommendationsrutan ovan. För patienter som behandlas med SVALL/EWALL är tidpunkten för MRD2 densamma som starten av andra konsolideringen med högdos metotrexat.
MRD-monitorering (benmärgsprov) rekommenderas med RT-PCR BCR::ABL1 och flödescytometri; det sistnämnda analyseras åtminstone tills MRD-negativitet med flödescytometri uppnåtts. Vid stigande MRD med RT-PCR för BCR::ABL1 i senare analyser bör återfall uteslutas med förnyad RT-PCR för BCR::ABL1 och flödescytometri från benmärg.
Under underhållsbehandlingen rekommenderas fortsatt MRD-monitorering, i första hand på perifert blod med 2–3 månaders intervall.
Efter avslutat underhåll då fortsatt TKI-behandling ges är det svårt att ge några generella rekommendationer, men även här bör monitorering i blod övervägas med 2–3 månaders intervall. Stigande nivåer av RT-PCR för BCR::ABL1 kan föranleda byte till andra och tredje generationens TKI. Inför ett behandlingsbyte rekommenderas mutationsanalys.
Information om MRD-monitorering efter allo-HSCT finns i Kapitel 15 Allogen stamcellstransplantation (allo‑HSCT).
Åtgärder vid kvarstående MRD
Vid kvarstående höga (> 0,01–0,001) eller stigande MRD-nivåer (även från lägre nivåer) under konsolidering eller underhållsbehandling bör konfirmerande prov utföras med både RT-PCR för BCR::ABL1 och flödescytometri från benmärg och byte till andra (dasatinib) eller tredje generationens TKI (ponatinib) starkt övervägas. Mutationsanalys bör utföras enligt ovan, för närvarande möjligt vid nivåer av BCR::ABL > cirka 0,1 %. Vid morfologiskt återfall (MRD > 1 %) bör även annan återfallsbehandling övervägas, och CNS-riktad behandling ges. Viss individuell anpassning kan behöva göras, fr.a. vid palliativt inriktad behandling. Se Kapitel 17 Handläggning av återfall och refraktär sjukdom.
